Väärisgaasid
Väärisgaasid (vananenud nimetusega inertgaasid) on sarnaste omadustega keemiliste elementide rühm: nad on standardtingimustel lõhnatud, värvitud, monoaatomilised gaasid, millel on madal reaktsioonivõime.
Kuus looduses esinevat väärisgaasi on heelium (He), neoon (Ne), argoon (Ar), krüptoon (Kr), ksenoon (Xe) ja radoon (Rn). Kõiki neid leidub vähesel määral Maa atmosfääris ja heelium on universumis levikult teine element. Aastal 2002 avastasid teadlased sünteetilise väärisgaasi oganessooni,[1] mille füüsikalisi ega keemilisi omadusi pole võimalik otseselt määrata väga lühikese poolestusaja (0,89 ms[2]) tõttu.
Väärisgaasid kuuluvad keemiliste elementide perioodilisussüsteemi 18. ehk VIIIA rühma. Looduslikud väärisgaasid on tüüpiliselt väga madala reaktsioonivõimega, välja arvatud ekstreemsetes tingimustes. Inertsuse tõttu saab neid kasutada keskkondades, kus soovitakse vältida keemilist reaktsiooni.
Väärisgaaside omadused on hästi seletatavad tänapäevaste teooriatega aatomistruktuuri kohta. Nende elektronkatte väliskihis on 8 (heeliumil 2) elektroni ehk välimine elektronkiht on "täis". Seetõttu on neil vähe kalduvusi keemilistes reaktsioonides osalemiseks. Väärisgaase sisaldavaid ühendeid on suudetud valmistada vaid mõnisada. Väärisgaaside sulamis- ja keemistemperatuuride vahe on väga väike, erinevus on alla 10 °C. See tähendab, et nad on vedelas olekus väga väikeses temperatuuride vahemikus.
Neooni, argooni ja ksenooni saab toota õhust gaasi vedeldamise ja fraktsioneeriva destillatsiooni teel. Heeliumit eraldatakse tavaliselt maagaasist ja radooni raadiumi radioaktiivse lagunemise laguproduktidest. Väärisgaase kasutatakse tööstuses valgustites, keevitamise juures ja kosmosetööstuses. Heeliumi-hapniku hingamisgaasi kasutavad tihti tuukrid, kes peavad sukelduma sügavamale kui 55 meetrit. Sellega välditakse kõrgest rõhust põhjustatud hapnikumürgitust ja lämmastikunarkoosi. Pärast vesiniku tuleohtlikkusest tulenevate riskide ilmnemist hakati selle asemel õhupallides ja aerostaatõhulaevades kasutama heeliumit.
Ajalugu[muuda | muuda lähteteksti]
Sõna "väärisgaas" tuleb saksakeelsest nimisõnast Edelgas, mille Hugo Erdmann 1898. aastal kasutusele võttis.[3] Termin tähistas gaaside madalat reaktsioonivõimet ja sellel on teatud analoogia terminiga "väärismetall" (Edelmetalle), mis tähistab metalle, millel on samuti madal reaktsioonivõime. Väärisgaase on nimetatud ka inertgaasideks, kuid see termin on vananenud, sest tänapäevaks on teada mitmeid väärisgaase sisaldavaid ühendeid.[4] Neid on nimetatud ka haruldasteks gaasideks,[5] kuid see on samuti ebatäpne, sest argoon moodustab olulise osa Maa atmosfäärist (0,94% mahust ja 1,3% massist).[6]

Pierre Janssen ja Joseph Norman Lockyer avastasid uue elemendi 1868. aastal, kui nad vaatlesid Päikse kromosfääri, ja nimetasid selle heeliumiks kreekakeelse sõna ήλιος (ílios või helios) järgi, mis tähendab Päikest.[7] Siis polnud keemiline analüüs võimalik, kuid hiljem selgus, et heelium on väärisgaas. Henry Cavendish oli enne neid, 1784. aastal, avastanud, et õhk sisaldab väikeses koguses ainet, mis on veel väiksema reaktsioonivõimega, kui lämmastik.[8] Lord Rayleigh avastas 1895. aastal, et õhust võetud lämmastikuproovid ja keemilistest reaktsioonidest saadud lämmastikuproovid on erineva tihedusega. Koos šoti teadlase William Ramsayga oletas ta, et õhust saadud lämmastik on segunenud mingi teise gaasiga.[8] See viis eksperimendini, mille käigus õnnestus eraldada uus element argoon, mille nimetus tuleb kreekakeelsest sõnast αργός (argós) ehk "mitteaktiivne".[8] Selle avastuse valguses taipasid nad, et perioodilisustabelist puudub terve klass gaase. Argooni otsimise käigus õnnestus Ramseyl esimest korda mineraali kleveiiti kuumutades eraldada heelium. Dmitri Mendelejev, nõustunud tõenditega argooni ja heeliumi olemasolu kohta, lisas väärisgaasid oma elementide süsteemi 1902. aastal 0-rühmana.[9] Tema süsteemist sai hiljem perioodilisussüsteem.[9]
Ramsey jätkas väärisgaaside otsimist, kasutades vedela õhu komponentideks lahutamiseks fraktsioneerivat destillatsiooni. Ta avastas 1898. aastal elemendid krüptoon, neoon ja ksenoon ning nimetas need kreeka sõnade "peidetud" (κρυπτός, kryptós), "uus" (νέος, néos) ja "võõras" ( ξένος, xénos) järgi. Radooni avastas Friedrich Ernst Dorn 1898. aastal[10] ja sellele pandi nimetuseks radium emanation, kuid seda ei peetud väärisgaasiks enne 1904. aastat.[11] Siis avastati, et see sarnaneb omaduste poolest teiste väärisgaasidega.[11] Rayleigh ja Ramsay said 1904. aastal väärisgaaside avastamise eest Nobeli auhinna, vastavalt füüsikas ja keemias.[12][13] Rootsi Kuningliku Akadeemia toonane president J. E. Cederblom ütles oma kõnes, et terve uute elementide klassi leidmine on unikaalne sündmus keemia ajaloos.[13]
Väärisgaaside avastamine aitas kaasa teadmiste arenemisele aatomimudeli kohta. Prantsuse keemik Henri Moissan üritas ebaõnnestunult reageerima panna fluori, kõige elektronegatiivsemat elementi, ja argooni, ühte väärisgaasidest. Teadlastel ei õnnestunud argooniühendeid valmistada enne 20. sajandi lõppu, kuid katsed selleks aitasid arendada uusi teooriaid aatomi struktuuri kohta. Taani füüsik Niels Bohr oletas 1913. aastal eksperimentidele toetudes, et elektronid aatomis on organiseeritud kihtidena, mis ümbritsevad tuuma, ja kõigil väärisgaasidel, välja arvatud heelium, on väliskihis alati kaheksa elektroni.[11] Gilbert Newton Lewis formuleeris 1916. aastal oktetireegli, mis ütleb, et kaheksa elektroni väliskihis on iga aatomi jaoks kõige stabiilsem olukord. Selline paigutus põhjustas väärisgaaside väikese reaktsioonivõime, kuna nad ei vajanud oma elektronkatte väliskihi täitmiseks enam rohkem elektrone.[14]
Neil Bartlet avastas 1962. aastal esimese väärisgaasiühendi, ksenoonheksafluoroplaatina.[15] Varsti pärast seda avastati ka teisi väärisgaaside ühendeid: 1962. aastal radoondifluoriid (RnF2)[16] ja 1963. aastal krüptoondifluoriid (KrF2).[17] Teade esimesest stabiilsest argooniühendist saabus 2000. aastal, kui temperatuuril 40 K (−233,2 °C) valmistati argoonfluorohüdriidi (HArF).[18]
Detsembris 1998 valmistasid Venemaal Dubna linnas paikneva Tuumauuringute Ühendatud Instituudi teadlased ühe aatomi 114. elementi flerooviumi (Fl), pommitades plutooniumit kaltsiumiga[19].[20] Esialgsed katsed vihjavad, et tegemist võib olla esimese üliraske elemendiga, mis näitab väärisgaasile tüüpilisi omadusi, kuigi kuulub perioodilisustabeli 14. rühma.[21]
Aastal 2002 avastasid Vene teadlased sünteetilise väärisgaaside hulka loetava radioaktiivse oganessooni, mille kolm aatomit moodustusid kaliforniumi pommitamisel kaltsiumiioonidega 1080 tunni jooksul. Oganessooni füüsikalisi ega keemilisi omadusi pole võimalik otseselt määrata väga lühikese poolestusaja (0,89 ms) tõttu. Alfalagunemise käigus moodustub oganessoonist livermoorium. Kuna oganessooni on õnnestunud sünteesida vaid mõni üksik aatom, piirdub elemendi kasutamine vaid teaduslike uurimistöödega.[2]
Füüsikalised omadused[muuda | muuda lähteteksti]
| Omadus[11][22] | Heelium | Neoon | Argoon | Krüptoon | Ksenoon | Radoon |
|---|---|---|---|---|---|---|
| Tihedus (g/dm³) | 0,1786 | 0,9002 | 1,7818 | 3,708 | 5,851 | 9,97 |
| Keemistemperatuur (K) | 4,4 | 27,3 | 87,4 | 121,5 | 166,6 | 211,5 |
| Sulamistäpp (K) | 0,95 | 24,7 | 83,6 | 115,8 | 161,7 | 202,2 |
| Aurustumissoojus (kJ/mol) | 0,08 | 1,74 | 6,52 | 9,05 | 12,65 | 18,1 |
| Lahustuvus vees 20 °C (cm3/kg) | 8,61 | 10,5 | 33,6 | 59,4 | 108,1 | 230 |
| Aatomnumber | 2 | 10 | 18 | 36 | 54 | 86 |
| Aatomi raadius (arvutuslik) (pm) | 31 | 38 | 71 | 88 | 108 | 120 |
| Ionisatsioonienergia (kJ/mol) | 2372 | 2080 | 1520 | 1351 | 1170 | 1037 |
| Alleni elektronegatiivsus[23] | 4,16 | 4,79 | 3,24 | 2,97 | 2,58 | 2,60 |
| Märkused | ^a Rõhul 25 bar | |||||
Väärisgaasidele on omased nõrgad aatomitevahelised jõud, mistõttu neil on madalad sulamis- ja keemistemperatuurid. Standardtingimustel on nad üheaatomilised gaasid. See kehtib ka nende elementide kohta, millega sarnase aatommassiga ained oleksid tavaliselt tahked.[11] Heeliumil on võrreldes teiste elementidega mitmeid unikaalseid omadusi: selle sulamis- ja keemistemperatuurid on madalamad kui ühelgi teisel tuntud ainel, see on ainus teadaolev element, mille juures ilmneb ülivoolavus. See on ainus element, mida ei saa standardtingimustel tahkesse olekusse viia: heeliumi tahkestamiseks tuleb temperatuuril 0,95 K rakendada rõhku 25 atm (2500 KPa, 370 psi). Väärisgaasidel kuni ksenoonini on mitu stabiilset isotoopi. Radoonil stabiilseid isotoope ei ole: pikima elueaga isotoobi 222Rn poolestusaeg on 3,8 päeva ning see laguneb heeliumiks ja polooniumiks, mis omakorda laguneb pliiks.[11]

Väärisgaaside aatomi raadius kasvab rühmas sujuvalt ülalt alla, nagu ka teiste rühmade elementide puhul. Aatomi suurus on seotud mitmete omadustega, näiteks ionisatsioonipotentsiaal väheneb raadiuse kasvades, kuna valentselektronid on suurte aatomite puhul tuumast kaugemal ja seetõttu hoiab tuum neid nõrgemini kinni. Väärisgaasidel on iga perioodi elementidest kõige suurem ionisatsioonienergia, mis väljendub nende elektronkonfiguratsiooni stabiilsuses ja reaktsioonivõime suhtelises puudumises.[22] Mõne raskema väärisgaasi ionisatsioonipotentsiaal on siiski piisavalt madal, et olla võrreldav teiste elementide või molekulidega. Teadmine, et ksenooni ionisatsioonipotentsiaal on võrreldav hapniku molekuli ionisatsioonipotentsiaaliga, viis katseni ksenooni plaatina heksafluoriidiga oksüdeerida. Tegemist on hapnikuga reageerimiseks piisavalt tugeva oksüdandiga.[15] Väärisgaasid ei saa stabiilsetelt anioonidelt elektrone vastu võtta, mis tähendab, et nende elektronafiinsus on negatiivne.[24]
Väärisgaaside makroskoopilised füüsikalised omadused jäävad nõrkade aatomitevaheliste van der Waalsi jõudude varju. Tõmbejõud kasvavad koos aatomi suurusega kuna kasvab polariseeritavus ja väheneb ionisatsioonipotentsiaal. See põhjustab rühmas süstemaatilisi trende: liikudes 18. rühmas ülalt alla, kasvavad aatomi raadius ja aatomitevahelised jõud, mistõttu kasvavad ka sulamistemperatuur, keemistemperatuur, aurustumis entalpia ja lahustuvus. Tiheduse kasv tuleneb aatomi massi suurenemisest.[22]
Väärisgaasid on standardtingimustel peaaegu ideaalsed gaasid, kuid nende kõrvalekalded ideaalse gaasi seadusest annavad vihjeid molekulidevaheliste vastasmõjude uurimiseks. John Lennard-Jones lõi 1924. aastal argooniga tehtud katsete andmete põhjal Lennard-Jonesi potentsiaalina tuntud matemaatilise mudeli, mida kasutati molekulidevaheliste vastasmõjude kirjeldamisel enne kvantmehaanika leiutamist.[25]
Keemilised omadused[muuda | muuda lähteteksti]

Väärisgaasid on standardtingimustes värvitud, lõhnatud, maitsetud ja mittesüttivad. Neid nimetati kunagi perioodilisustabeli 0-rühmaks, kuna arvati, et nende valents on 0 ehk nende aatomid ei saa teiste elementidega ühendeid moodustada. Hiljem avastati, et teatud väärisgaasid siiski moodustavad ühendeid, ja see nimetus pole enam käibel.[11]
Nagu ka teiste rühmade puhul, järgivad väärisgaaside elektronkonfiguratsioonid ühtset mustrit, eriti elektronkatte väliskihis, mis mõjutab keemilisi omadusi:
| Z | Element | Elektronide arv / elektronkiht |
|---|---|---|
| 2 | heelium | 2 |
| 10 | neoon | 2, 8 |
| 18 | argoon | 2, 8, 8 |
| 36 | krüptoon | 2, 8, 18, 8 |
| 54 | ksenoon | 2, 8, 18, 18, 8 |
| 86 | radoon | 2, 8, 18, 32, 18, 8 |
Väärisgaaside kõige välimine, valentselektronide kiht, mille elektronid osalevad keemiliste sidemete loomisel, on täitunud. Sellised aatomid on väga stabiilsed ning ei kipu seetõttu keemilisi sidemeid looma, elektrone liitma ega loovutama.[4]
Aatomorbitalide kirjeldamisel[muuda | muuda lähteteksti]
Kuna väärisgaaside elektronkatte väliskihis on täiskomplekt elektrone, siis saab neid kasutada teiste elementide elektronkatete kirjeldamiseks. Selleks asendatakse sisekihid lähima kirjeldatavast elemendist perioodilisustabelis eespool asuva väärisgaasiga ja kirjutatakse välja ainult väliskiht. Näiteks süsiniku elektronkate on 1s22s22p2 ja väärisgaasi esituses [He]2s22p2. Selline kirjaviis on lühem ja teeb elementide identifitseerimise lihtsamaks.[26]
Ühendid[muuda | muuda lähteteksti]
Kuna väärisgaaside reaktsioonivõime on ülimadal, on õnnestunud valmistada vaid mõnisada väärisgaasi ühendit. Neutraalseid ühendeid, kus heelium ja neoon oleks seotud keemiliste sidemetega, ei ole valmistatud, kuigi heeliumi ühendite võimalikkuse kohta on mõningaid teoreetilisi tõendeid. Ksenoon, krüptoon ja argoon on demonstreerinud vaid väikest reaktsioonivõimet.[27] Reaktsioonivõime alusel reastuvad elemendid järgmiselt: Ne < He < Ar < Kr < Xe < Rn.
Linus Pauling ennustas 1933. aastal, et väärisgaasid võivad moodustada ühendeid fluori ja hapnikuga. Ta ennustas, et eksisteerivad krüptoonheksafluoriid (KrF6) ja ksenoonheksafluoriid (XeF6). Pauling spekuleeris, et XeF8 võib eksisteerida ebastabiilse ühendina ja pakkus, et ksenoonhape võiks moodustada perksenoonsoolasid.[28][29] Need ennustused osutusid üldiselt täpseks, ainult XeF8 peetakse nüüd nii termodünaamiliselt kui ka kineetiliselt ebastabiilseks.[30]
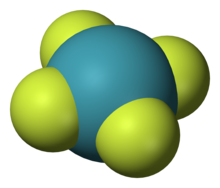
Kõige arvukamalt on valmistatud ksenooniühendeid.[31] Enamikus neist on ksenooniaatom oksüdatsiooniastmes +2, +4, +6 või +8 ning seotud väga elektronegatiivse aatomiga nagu fluor või hapnik, nagu näiteks ksenoondifluoriid (XeF2), ksenoontetrafluoriid (XeF4), ksenoonheksafluoriid (XeF6), ksenoontetraoksiid (XeO4) ja naatriumperksenaat (Na4XeO6). Mõningaid neist kasutatakse keemilise sünteesi juures oksüdeerijana. Näiteks XeF2 on tööstuses vabalt saadaval fluorimiseks.[32] Aastaks 2007 oli avastatud umbes 500 ühendit, kus ksenoon on keemiliselt seotud teiste elementidega, sealhulgas orgaanoksenoon ühendeid (kus ksenoon on seotud süsinikuga). Ksenooni ühendeid on moodustatud lämmastiku, kloori, kulla, elavhõbeda ja ksenooni endaga.[27][33] Ühendeid, kus ksenoon on seotud boori, vesiniku, broomi, joodi, berülliumi, väävli, titaani, vase ja hõbedaga on samuti täheldatud, kuid ainult väga madalatel temperatuuridel väärisgaasides koosnevas maatriksis või ülikiiretes väärisgaasijugades.[27]
Teoorias on radoon reageerimisvõimelisem, kui ksenoon ja peaks seega keemilisi sidemeid kergemini moodustama. Kuid radooni isotoopide suure radioaktiivsuse ja lühikese poolestusaja tõttu on praktikas valmistatud vaid mõned fluoriidid ja oksiidid.[34]
Krüptooni reaktsioonivõime on väiksem kui ksenoonil, kuid siiski on teateid mitmetest ühenditest, kus krüptooni oksüdatsiooniaste on +2.[27] Kõige tuntum on krüptoondifluoriid, kuid on kirjeldatud ka ühendeid, kus krüptoon moodustab ühe sideme lämmastiku või hapnikuga[35], kuid need on stabiilsed temperatuuridel −60 °C ja −90 °C.[27]
Krüptooni aatomid moodustavad sidemeid teiste mittemetallidega (vesinik, kloor, süsinik) ja mõningate siirdemetallidega (vask, hõbe, kuld), kuid seda ainult madalatel temperatuuridel väärisgaasidest koosnevates maatriksites või siis ülikiiretes väärisgaasijugades. Sarnastes tingimustes valmistati 2000. aastatel esimesed argooniühendid (argoonflorohüdriid HArF ja mõned sidemed siirdemetallidega vask, hõbe ja kuld. 2007. aasta seisuga pole teada ühtegi stabiilset neutroolset molekuli, mis sisaldaks heeliumi või neooni kovalentset sidet.[27]
Väärisgaasid, sealhulgas heelium, võivad moodustada stabiilseid molekulaarseid ioone. Kõige lihtsam neist on heeliumhüdriidi ioon, mis avastati 1925. aastal.[36] Kuna see koosneb kahest universumis kõige levinumast elemendist, siis arvatakse, et seda esineb looduslikult tähtedevahelises ruumis, kuigi seda pole veel avastatud.[37] Lisaks ioonidele on teada ka mitu neutraalset väärisgaasi eksimeeri. Need ühendid, näiteks ArF ja KrF, on stabiilsed ainult ergastatud olekus; mõned neist leiavad kasutust eksimeerlaserites.
Lisaks ühenditele, kus väärisgaas moodustab kovalentse sideme on ka mittekovalentseid ühendeid. Klatraadid, mida esmakordselt kirjeldati 1949. aastal,[38] koosnevad väärisgaasi aatomitest, mis on lõksustatud teatud orgaaniliste ja mitteorgaaniliste ainete kristallstruktuuri. Oluline eeltingimus nende moodustumisel on, et sisestatud (väärisgaasi) aatom peab olema sobiva suurusega, et kristallstruktuuris olevatesse tühimikesse mahtuda. Näiteks argoon, krüptoon ja ksenoon moodustavad klatraate hüdrokinooniga, kuid heelium ja neoon mitte, sest nad on liiga väikesed või ebapiisavalt polariseeritavad, et neid kinni hoida.[39] Neoon, argoon, krüptoon ja ksenoon moodustavad klatraate ka hüdraatidega, kui väärisgaas on jäässe lõksu jäänud.[40]
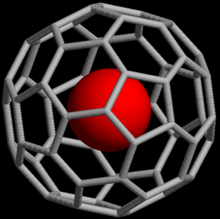
Väärisgaasid võivad moodustada ühendeid endoheedriliste fullereenidega, kus väärisgaasi aatom on lõksustatud fullereeni sisse. Aastal 1993. avastati, et kui C60, 60 süsiniku aatomist moodustunud sfääriline molekul panna kõrge rõhu all väärsigaasi keskkonda, siis tekivad kompleksühendid nagu He@C60 (@ tähendab, et He paikneb C60 sees, mitte ei ole sellega kovalentselt seotud).[41] 2008. aasta seisuga on saadud endoheedrilisi komplekse heeliumi, neooni, argooni, krüptooni ja ksenooniga.[42] Neid ühendeid on kasutatud fullereenide struktuuri ja reaktsioonivõime uurimiseks, kasutades väärisgaaside tuumamagnetresonantsi.[43]
Väärisgaasi ühendeid, nagu näiteks ksenoondifluoriid (XeF2), peetakse hüpervalentseteks, kuna nad rikuvad okteti reeglit. Sidemete moodustamist sellistes ühendites saab seletada Pimentel–Rundle kolme keskme mudeliga.[44][45] Esimest korda 1951. aastal välja pakutud mudeli järgi tekib side kolme kollineaarse aatomi vahel. Näiteks sidemeid XeF2 kirjeldatakse kolme molekulaarorbitalina, mis on moodustatud iga aatomi p-orbitalidest. Side tekib ksenooni täitunud p-orbitali kombineerumisega kummagi fluoriaatomi pooltühja p-orbitaliga. Selle tulemusel tekib täitunud siduv orbital, täitunud mittesiduv orbital ja tühi lõdvendav orbital. Kõrgeim täitunud molekulaarorbital paikneb kahel otsasidemel. See näitab laengu lokaliseerumist, mida soodustab fluori suur elektronegatiivsus.[46]
Levik ja tootmine[muuda | muuda lähteteksti]
| Leidumine | Heelium | Neoon | Argoon | Krüptoon | Ksenoon | Radoon |
|---|---|---|---|---|---|---|
| Päikesesüsteemis (iga räni aatomi kohta)[47] | 2343 | 2,148 | 0,1025 | 5,515 × 10−5 | 5,391 × 10−6 | – |
| Maa atmosfääris (osa mahust ppm)[48] | 5,20 | 18,20 | 9340,00 | 1,10 | 0,09 | (0,06–18) × 10−19[49] |
| Tardkivimites (osa massist ppm)[22] | 3 × 10−3 | 7 × 10−5 | 4 × 10−2 | – | – | 1,7 × 10−10 |
Mida suurem on väärisgaasi aatominumber, seda vähem see universumis levinud on. Heelium on vesiniku järel kõige levinum element universumis ja moodustades 24% selle massist. Enamus heeliumist tekkis Suure Paugu ajal tuumasünteesi käigus, kuid selle hulk kasvab pidevalt tänu tähtedes toimuvale tuumasünteesile ja väga vähesel määral ka raskemate elementide alfalagunemise tagajärjel.[50][51] Levimus Maal järgib veidi teist loogikat, heelium on leidumise järgi maa atmosfääris alles kolmandal kohal, põhjuseks ürgse heeliumi puudumine atmosfäärist. Kuna sellel on väike aatommass ei suuda maa gravitatsiooniväli seda kinni hoida.[52] Maal eksisteeriv heelium pärineb selliste maakoores leiduvate elementide nagu uraan ja toorium alfalagunemisest ja see akumuleerub tihti maagaasi reservuaarides.[52] Argooni hulk kasvab aga kaltsium-40 beetalagunemise käigus, mida leidub samuti maakoores. Nii tekib argoon-40, mis vaatamata suhtelisele haruldusele Päikesesüsteemis on kõige levinum isotoop Maal. See protsess on kaltsium-argooni dateerimismeetodi aluseks.[53] Ksenooni hulk atmosfääris on ootamatult väike ja seda olukorda on nimetatud "puuduva ksenooni probleemiks". Ühe teooria kohaselt võib puuduv ksenoon sisalduda maakoores leiduvates mineraalides.[54] Pärast ksenoon dioksiidi avastamist näitas üks uurimistöö, et ksenoon võib kvartsis räni asendada.[55] Radoon tekib litosfääris raadiumi alfalagunemise käigus. See võib läbi vundamendipragude hoonetesse imbuda ja akumuleeruda venilatsioonita ruumides. Suure radioaktiivsuse tõttu on see oluliseks terviseriskiks: ainuüksi Ameerika Ühendriikides põhjustab see kopsuvähi näol hinnanguliselt 21 000 surma aastas.[56]
| Gaas | Hind 2004. aastal (USD/m3)[57] |
|---|---|
| Heelium (tööstusliku puhtusega) | 4,20–4,90 |
| Heelium (labori puhtusega) | 22,30–44,90 |
| Argoon | 2,70–8,50 |
| Neoon | 60–120 |
| Krüptoon | 400–500 |
| Ksenoon | 4000–5000 |
Neooni, argooni, krüptooni ja ksenooni toodetakse õhust. Õhk vedeldatakse ja lahutatakse fraktsioneeriva destilleerimise abil komponentideks. Heeliumit eraldatakse tavaliselt maagaasist ja radooni raadiumi radioaktiivsete laguproduktide hulgast.[11] Väärisgaaside hinnad sõltuvad nende levikust: argoon on kõige odavam ja ksenoon kõige kallim.
Rakendused[muuda | muuda lähteteksti]

Väärisgaasidel on väga madalad keemis- ja sulamistemperatuurid, mis muudab nad kasutatavaks kürogeeniliste jahutusvedelikena.[58] Vedel heelium, mis keeb 4,2 K (−268,95 °C) juures, on levinud tuumamagnetresonantsspektroskoopias ja magnetresonantstomograafias kasutatavate ülijuhtivate magnetite jahutamisel.[59] Kuigi vedela neooniga ei saavutata nii madalaid temperatuure nagu heeliumiga, on selle külmutusvõimsus 40 suurem kui heeliumil ja kolm korda suurem kui vesinikul.[49]
Heeliumi kasutatakse hingamisgaasides lämmastiku asemel, sest see lahustub halvasti vedelikes, eriti lipiidides. Rõhu all, näiteks sukeldumisel, absorbeerivad veri ja koed gaase, mis põhjustab lämmastikunarkoosina tuntud anesteetilist efekti.[60] Kuna selle lahustuvus on väike, satub vaid väike kogus heeliumi rakumembraani.[61] Kui kasutada heeliumi hingamisgaasi, näiteks trimixi või helioxi osana, siis väheneb narkootiline efekt.[61] Heeliumi vähene lahustuvus tuleb kasuks ka kessoontõve puhul.[11][62] Väiksem lahustuvus tähendab väiksema hulga gaasimullide teket sügavusest pinnale tõusmisel. Argooni peetakse parimaks kuiva ülikonna täitegaasiks.[63] Heeliumit kasutatakse ka täitegaasina tuumareaktorite kütusevarrastes.[64]

Pärast Hindenburgi katastroofi 1937. aastal[65] on heelium asendanud vesiniku tõstegaasina aerostaatides ja õhupallides, kuna see on kerge ja mittesüttiv, kuigi 8,6%[66] väiksema üleslükkejõuga[11].
Paljude rakenduste puhul kasutatakse väärisgaase inertse keskkonna tekitamiseks. Õhu ja ka lämmastiku suhtes tundlike ainete sünteesimisel argooni. Tahket argooni kasutatakse väga ebastabiilsete ühendite, näiteks reaktsiooni vaheühendite uurimiseks, lõksustades viimaseid väga madalal temperatuuril inertsesse maatriksisse.[67] Heeliumi kasutatakse gaasikromatograafias kandegaasina, täitegaasina termomeetrites ja radioaktiivsust mõõtvates seadmetes, nagu geigeri loendur ja mullikamber.[57] Nii heelium kui ka argoon on levinud keevituskaare ja seda ümbritsevate oksüdeerivate metallide kaitsmiseks atmosfääri eest keevitamise või lõikamise ajal.[49] Mõlemat kasutatakse ka muudes metallurgiaprotsessides ja räni tootmiseks pooljuhtide tööstuses.[49]

Väärisgaase kasutatakse tänu nende vähesele reaktsioonivõimele valgustites. Lämmastikuga segatud argoon on kasutusel täitegaasina hõõglampides. Krüptooni kasutatakse kvaliteetsetes pirnides, millel on kõrge värvitemperatuur. Eriti halogeenlampides on kasutusel joodi- või bromiidiühenditega segatud krüptoon. Väärisgaasid helendavad iseloomulikult, kui neid kasutada gaaslahenduslampides, nn neoonvalgustites. Neid valgusteid nimetatakse neooni järgi, kuid need sisaldavad tihti muid gaase ja fosfaate, mis lisavad neooni oranž-punasele värvile varjundeid. Ksenooni kasutatakse peamiselt ksenoonlampides, mille valgus sarnaneb päevavalgusega ning mis on kasutusel videoprojektorites ja autolaternates.[49]
Mõningaid väärisgaase kasutatakse meditsiinis. Heeliumit kasutatakse mõnikord lihtsustamaks astmahaigel hingamist.[49] Ksenooni kasutatakse üldnarkoosis, kuna see lahustub hästi lipiidides ja on seetõttu efektiivsem kui lämmastikoksiid ja kuna see lahkub kergesti organismist, taastub patsient kiiremini.[68] Väga radioaktiivset radooni on saada vaid väikeses koguses ja seda kasutatakse kiiritusravis.[11]
Värvid[muuda | muuda lähteteksti]

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|
| Heelium | Neoon | Argoon (Argooni tähist kujutavates torudes on mõnevõrra elavhõbedat) |
Krüptoon | Ksenoon |
Gaaslahenduse värv sõltub mitmest asjaolust, sealhulgas:[69]
- Laengu parameetritest (voolu tihedus ja elektrivälja tugevus konkreetses punktis, temperatuur ja muud näitajad). Pane tähele värvi varieerumist gaaslahendustes ülemise rea piltidel.
- Gaasi puhtus. Teatud gaasid võivad värvi mõjutada ka väikeses koguses.
- Gaaslahenduse toru materjal. Eelviimases reas olevad elemendisümbolid on tehtud paksust majapidamisklaasist ning neelavad UV-valgust ja siniseid toone.
Viited[muuda | muuda lähteteksti]
- ↑ Clinton S. Nash Atomic and Molecular Properties of Elements 112, 114, and 118. J. Phys. Chem. 2005 vol. 109-15, lk 3493–3500. doi:10.1021/jp050736o, PMID 16833687
- ↑ 2,0 2,1 Facts About Oganesson (Element 118) www.livescience.com
- ↑ Edward Renouf, (1901). Noble gases. Science 13 (320): 268–270. doi:10.1126/science.13.320.268.
- ↑ 4,0 4,1 Ojima, Podosek 2002, lk 30–35
- ↑ Ojima, Podosek 2002, lk 4
- ↑ "argon(Ar)". Encyclopædia Britannica (Inglise keel). 2008. Vaadatud 8. märtsil 2013.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ Oxford English Dictionary (1989), helium Vaadatud 16. detsember 2006 veebiversioonist Oxford English Dictionary Online
- ↑ 8,0 8,1 8,2 Ojima, Podosek 2002, lk 1
- ↑ 9,0 9,1 Mendelejev 1903, lk 497
- ↑ J. R. Partington (1957). Discovery of Radon Nature 179 (4566): 912.doi:10.1038/179912a0
- ↑ 11,00 11,01 11,02 11,03 11,04 11,05 11,06 11,07 11,08 11,09 11,10 "noble gas". Encyclopædia Britannica (Inglise keel). 2008. Vaadatud 8. märtsil 2013.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ J.E. Cederblom (1904). "The Nobel Prize in Physics 1904 Presentation Speech" (Inglise keel). nobelprize.org/. Vaadatud 8. märtsil 2013.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ 13,0 13,1 J.E. Cederblom (1904). "The Nobel Prize in Chemistry 1904 Presentation Speech" (Inglise keel). nobelprize.org/. Vaadatud 8. märtsil 2013.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ R. J. Gillespie, E. A. Robinson (2007). Gilbert N. Lewis and the chemical bond: the electron pair and the octet rule from 1916 to the present day. J Comput Chem 28 (1): 87–97.doi:10.1002/jcc.20545
- ↑ 15,0 15,1 Neil Bartlett (1962). Xenon hexafluoroplatinate Xe+[PtF6]–. Proceedings of the Chemical Society (6): 218. doi:10.1039/PS9620000197
- ↑ Paul R. Fields, Lawrence Stein, Moshe H. Zirin (1962). Radon Fluoride. Journal of the American Chemical Society 84 (21): 4164–4165. doi:10.1021/ja00880a048
- ↑ A. V. Grosse, A. D. Kirschenbaum, A. G. Streng, L. V. Streng (1963). Krypton Tetrafluoride: Preparation and Some Properties. Science 139 (3559): 1047–1048.doi:10.1126/science.139.3559.1047
- ↑ Leonid Khriachtchev, Mika Pettersson, Nino Runeberg, Jan Lundell, Markku Räsänen (2000). A stable argon compound. Nature 406 (6798): 874–876. doi:10.1038/35022551
- ↑ Yu. Ts. Oganessian, V. Utyonkov, Yu. Lobanov, F. Abdullin, A. Polyakov, I. Shirokovsky, Yu. Tsyganov, G. Gulbekian, et al. (1999). Synthesis of Superheavy Nuclei in the 48Ca + 244Pu Reaction. Physical Review Letters (American Physical Society) 83 (16): 3154.doi:10.1103/PhysRevLett.83.3154.
- ↑ Michael Woods (9. märts 2003). "Chemical element No. 110 finally gets a name – darmstadtium". post-gazette.com (Inglise keel). Pittsburgh, PA. Originaali arhiivikoopia seisuga 20. oktoober 2012. Vaadatud 9. märtsil 2013.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ Gas Phase Chemistry of Superheavy Elements (loeng). Texas A&M University.
- ↑ 22,0 22,1 22,2 22,3 Greenwood 1997, lk 891
- ↑ Leland C. Allen, (1989). Electronegativity is the average one-electron energy of the valence-shell electrons in ground-state free atoms. Journal of the American Chemical Society 111: 9003. doi:10.1021/ja00207a003
- ↑ John C. Wheeler, (1997). Electron Affinities of the Alkaline Earth Metals and the Sign Convention for Electron Affinity. Journal of Chemical Education 74: 123–127.
- ↑ N. F. Mott, (1955). John Edward Lennard-Jones. 1894–1954. Biographical Memoirs of Fellows of the Royal Society 1: 175–184. doi:10.1098/rsbm.1955.0013.
- ↑ Bobrow Test Preparation Services (2007). CliffsAP Chemistry, lk 15. CliffsNotes. ISBN 0-470-13500-X
- ↑ 27,0 27,1 27,2 27,3 27,4 27,5 Wojciech Grochala (2007). 'Atypical compounds of gases, which have been called noble'. Chemical Society Reviews 36 (10): 1632–1655. doi:10.1039/b702109g.
- ↑ Linus Pauling (1933). The Formulas of Antimonic Acid and the Antimonates. Journal of the American Chemical Society 55 (5): 1895–1900. doi:10.1021/ja01332a016.
- ↑ Holloway 1968
- ↑ Konrad Seppelt (1979). Recent developments in the Chemistry of Some Electronegative Elements. Accounts of Chemical Research 12 (6): 211–216. doi:10.1021/ar50138a004.
- ↑ G. J. Moody (1974). A Decade of Xenon Chemistry. Journal of Chemical Education 51 (10): 628–630. doi:10.1021/ed051p628.
- ↑ Marko Zupan, Jernej Iskra, Stojan Stavber (1998). Fluorination with XeF2. 44. Effect of Geometry and Heteroatom on the Regioselectivity of Fluorine Introduction into an Aromatic Ring. J. Org. Chem 63 (3): 878–880. doi:10.1021/jo971496e.
- ↑ Harding 2002, lk 90–99
- ↑ V. V. Avrorin, R. N. Krasikova, V. D. Nefedov, M. A. Toropova (1982). The Chemistry of Radon. Russian Chemical Review 51 (1): 12–20. doi:10.1070/RC1982v051n01ABEH002787.
- ↑ J. Lehmann (2002). The chemistry of krypton. Coordination Chemistry Reviews 233–234: 1–39. doi:10.1016/S0010-8545(02)00202-3.
- ↑ T. R. Hogness, E. G. Lunn (1925). The Ionization of Hydrogen by Electron Impact as Interpreted by Positive Ray Analysis. Physical Review 26: 44–55. doi:10.1103/PhysRev.26.44.
- ↑ J. Fernandez, F. Martin (2007). Photoionization of the HeH2+ molecular ion. J. Phys. B: At. Mol. Opt. Phys 40 (12): 2471–2480. doi:10.1088/0953-4075/40/12/020.
- ↑ H. M. Powell, M. Guter (1949). An Inert Gas Compound. Nature 164 (4162): 240–241. doi:10.1038/164240b0.
- ↑ Greenwood 1997, lk 893
- ↑ Yuri A. Dyadin et al. (1999). Clathrate hydrates of hydrogen and neon. Mendeleev Communications 9 (5): 209–210. doi:10.1070/MC1999v009n05ABEH001104.
- ↑ M. Saunders, H. A. Jiménez-Vázquez, R. J. Cross, R. J. Poreda (1993). "Stable compounds of helium and neon. He@C60 and Ne@C60". Science 259 (5100): 1428–1430. doi:10.1126/science.259.5100.1428.
- ↑ Martin Saunders, Hugo A. Jimenez-Vazquez, R. James Cross, Stanley Mroczkowski, Michael L. Gross, Daryl E. Giblin, Robert J. Poreda (1994). Incorporation of helium, neon, argon, krypton, and xenon into fullerenes using high pressure. J. Am. Chem. Soc. 116 (5): 2193–2194. doi:10.1021/ja00084a089.
- ↑ Michael Frunzi, James R. Cross, Martin Saunders (2007). Effect of Xenon on Fullerene Reactions. Journal of the American Chemical Society 129 (43): 13343–6. doi:10.1021/ja075568n.
- ↑ Greenwood 1997, lk 897
- ↑ Weinhold 2005, lk 275–306
- ↑ G. C. Pimentel, (1951). The Bonding of Trihalide and Bifluoride Ions by the Molecular Orbital Method. The Journal of Chemical Physics 19 (4): 446–448. doi:10.1063/1.1748245[alaline kõdulink].
- ↑ Katharine Lodders (10. juuli 2003). "Solar System Abundances and Condensation Temperatures of the Elements" (PDF). The Astrophysical Journal 591 (2): 1220–1247 (inglise keel). The American Astronomical Society. Originaali (PDF) arhiivikoopia seisuga 7. november 2015. Vaadatud 10. märtsil 2013.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ "The Atmosphere" (inglise keel). National Weather Service. September 2010. Vaadatud 10. märtsil 2013.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ 49,0 49,1 49,2 49,3 49,4 49,5 Peter Häussinger, Reinhard Glatthaar, Wilhelm Rhode, Helmut Kick, Christian Benkmann, Josef Weber, Hans-Jörg Wunschel, Viktor Stenke, Edith Leicht, Hermann Stenger 2001. Noble Gases. Ullmann's Encyclopedia of Industrial Chemistry. doi:10.1002/14356007.a17_485.
- ↑ Achim Weiss (2006). "Elements of the past: Big Bang Nucleosynthesis and observation". Einstein Online Vol. 2 (Inglise keel).
{{netiviide}}: parameeter|vaadatud=nõuab parameetrit|url=(juhend); puuduv või tühi|url=(juhend)CS1 hooldus: tundmatu keel (link) - ↑ A. Coc et al. (2004). Updated Big Bang Nucleosynthesis confronted to WMAP observations and to the Abundance of Light Elements. Astrophysical Journal 600 (2): 544. doi:10.1086/380121.
- ↑ 52,0 52,1 P. Morrison, J. Pine (1955). Radiogenic Origin of the Helium Isotopes in Rock. Annals of the New York Academy of Sciences 62 (3): 71–92.
- ↑ Alexandra Scherer (16. jaanuar 2007). 40Ar/39Ar dating and errors (arhiveeritud). Technische Universität Bergakademie Freiberg. Kasutatud: 9. märts 2013
- ↑ Chrystèle Sanloup et al. (2005). Retention of Xenon in Quartz and Earth's Missing Xenon. Science 310 (5751): 1174–1177. doi:10.1126/science.1119070.
- ↑ Tyler Irving (mai 2011). "Xenon Dioxide May Solve One of Earth's Mysteries". L’Actualité chimique canadienne (Canadian Chemical News) (Inglise keel). Originaali arhiivikoopia seisuga 9. veebruar 2013. Vaadatud 9. märtsil 2012.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ "A Citizen's Guide to Radon" (inglise keel). U.S. Environmental Protection Agency. Mai 2012. Vaadatud 10. märtsil 2013.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ 57,0 57,1 Shuen-Chen Hwang, Robert D. Lein, Daniel A. Morgan (2005). Noble Gases. Kirk Othmer Encyclopedia of Chemical Technology. Wiley. lk 343–383. doi:10.1002/0471238961.0701190508230114.a01.
- ↑ Neon. Encarta. 2008.
- ↑ C. J. Zhang, X. T. Zhou, L. Yang, (1992). Demountable coaxial gas-cooled current leads for MRI superconducting magnets. Magnetics, IEEE Transactions on (IEEE) 28 (1): 957–959. doi:10.1109/20.120038.
- ↑ B Fowler, K. N. Ackles, G. Porlier (1985). "Effects of inert gas narcosis on behavior-a critical review". Undersea Biomed. Res. 12 (4): 369–402. (Inglise keel). Originaali (PDF) arhiivikoopia seisuga 27. juuli 2011. Vaadatud 10. märtsil 2013.
{{netiviide}}: CS1 hooldus: mitu nime: autorite loend (link) CS1 hooldus: tundmatu keel (link) - ↑ 61,0 61,1 Bennett 1998, lk 176
- ↑ R. D. Vann (toim.) (1989). ""The Physiological Basis of Decompression"". 38th Undersea and Hyperbaric Medical Society Workshop 75(Phys)6-1-89: 437. (Inglise keel). Originaali arhiivikoopia seisuga 5. jaanuar 2010. Vaadatud 9. märtsil 2013.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ Eric Maiken (1995). "Why Argon?" (Inglise keel). Vaadatud 9. märtsil 2013.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ G. Horhoianu (1999). Thermal behaviour of CANDU type fuel rods during steady state and transient operating conditions. Annals of Nuclear Energy 26 (16): 1437. doi:10.1016/S0306-4549(99)00022-5.
- ↑ Disaster Ascribed to Gas by Experts. The New York Times: lk 1. 7. mai 1937.
- ↑ Craig Freudenrich (26. veebruar 2001). "How Blimps Work". science.howstuffworks.com (Inglise keel). Vaadatud 9. märtsil 2013.
{{netiviide}}: CS1 hooldus: tundmatu keel (link) - ↑ I. R. Dunkin (1980). The matrix isolation technique and its application to organic chemistry. Chem. Soc. Rev. 9: 1–23. doi:10.1039/CS9800900001.
- ↑ Robert D. Sanders, Daqing Ma, Mervyn Maze (2005). Xenon: elemental anaesthesia in clinical practice. British Medical Bulletin 71 (1): 115–135. doi:10.1093/bmb/ldh034.
- ↑ Sidney 1999, lk 383–384.
Kirjandus[muuda | muuda lähteteksti]
- Peter B. Bennett, David H. Elliott (1998). The Physiology and Medicine of Diving. SPCK Publishing. ISBN 0-7020-2410-4.
- N. N. Greenwood, A. Earnshaw (1997). Chemistry of the Elements (2nd ed.). Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
- John H. Holloway (1968). Noble-Gas Chemistry. London: Methuen Publishing. ISBN 0-412-21100-9.
- Dmitri Mendelejev (1902–1903) (in Russian). Основы химии (The Principles of Chemistry, 7th ed.).
- Minoru Ojima, Frank A. Podosek (2002). Noble Gas Geochemistry. Cambridge University Press. ISBN 0-521-80366-7.
- Sidney F. Ray (1999). Scientific photography and applied imaging. Focal Press. ISBN 0-240-51323-1.
- F. Weinhold, C. Landis (2005). Valency and bonding. Cambridge University Press. ISBN 0-521-83128-8.
Välislingid[muuda | muuda lähteteksti]
| Pildid, videod ja helifailid Commonsis: Väärisgaasid |
