Orgaaniline keemia

Orgaaniline keemia on keemia haru, mis uurib orgaaniliste ühendite (st süsinikku sisaldavate ainete, välja arvatud mõned süsinikuühendid ja süsinik lihtainena) struktuuri, sünteesi ja reaktsioone.[1] See hõlmab õpetust orgaaniliste ühendite ehitusest, omadustest, muundumise seaduspärasustest, saamisest, kasutamisest ja palju muud.
Orgaaniliste ühendite rohkuse ja mitmekesisuse määrab süsiniku võime moodustada tohutult pikki ahelaid, mis saavad olla hargnenud, hargnemata või tsüklilised. Orgaanilist keemiat võib nimetada ka süsivesinike ja nende funktsionaalderivaatide keemiaks.[2]
Orgaanilise keemia põhieesmärk on inimkonnale vajalike orgaaniliste ühendite saamine (süntees või eraldamine looduslikust materjalist) ning nende ühendite omaduste ja kasutusvõimaluste kindlakstegemine. Seda põhieesmärki toetavad orgaaniliste ühendite struktuuri määramine, analüüsi ja puhastamismeetodite väljatöötamine, aga ka teoreetilise orgaanilise keemia arendamine.[3]
Orgaanilises analüütilises keemias eraldatakse ainete segust konkreetsed ained ning määratakse nende füüsikalised omadused (näiteks sulamistemperatuur, keemistemperatuur, murdumisnäitaja) ning seejärel määratakse nende elementaarkoostis (elementaaranalüüs) ja funktsionaalsed rühmad), kasutades regente, tuumamagnetresonantsspektroskoopiat, infrapunaspektroskoopiat ja UV/Vis-spektroskoopiat.
Peale selle uuritakse orgaanilises keemias anorgaaniliste ja orgaaniliste reagentide mõju orgaanilistele ainetele, et määrata seaduspärasused, kuidas need mõjuvad kindlatele funktsionaalsetele rühmadele ja ainerühmadele. Neid seaduspärasusi tundes saab kavandada looduslike orgaaniliste ainete (näiteks suhkrute, peptiidide, looduslike värvainete, alkaloidide, vitamiinide) sünteesi või sünteesida looduses mitteleiduvaid kasulikke orgaanilisi ühendeid (plaste, polüetüleenist kilekotte ja pakendeid, erinevaid polümeere, ioonivaheteid, ravimeid, taimekaitsevahendeid, kunstkiude).
Viimase 150 aasta jooksul on orgaanilise keemia saavutused märgatavalt mõjutanud inimeste tervist, toitumist ja riietust ning loonud palju uusi tarbekaupu.
Piiritlus
[muuda | muuda lähteteksti]Väheste eranditega hõlmab orgaaniline keemia kõik süsiniku ühendid süsinikuga ja teiste elementidega. Nende seas on ka kõik seni tuntud elu ehituskivid, kogu elusloodus on ülesehitatud süsinikuühenditest. Aastal 2012 oli teada umbes 40 miljonit orgaanilist ühendit. Ligemale 95% kõigist tänapäeval tuntud ja valmistatud ainetest on süsinikuühendid. Süsiniku ühendite arv ei ole kindel suurus, vaid erinevaid süsinikku sisaldavaid makromolekule sünteesitakse pidevalt juurde. Süsinikuühendite arv on põhimõtteliselt lõpmatu suur.[4]
Eranditeks on lihtained (grafiit, teemant) ja kõik anorgaanilise keemia alla kuuluvad süsiniku vesinikuvabad halkogeniidid (süsinikmonoksiid, süsinikdioksiid, väävelsüsinik, süsihape ja karbonaadid, karbiidid ja ioonilised tsüaniidid, tsüanaadid ja tiotsüanaadid (vaata süsinikuühendid).
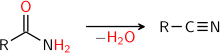
Sinihape kuulub anorgaanilise ja orgaanilise keemia vahelisele piirialale. Kuigi see kuuluks traditsiooniliselt anorgaanilise keemia alla, käsitatakse seda sipelghappe nitriilina (orgaaniline ainerühm). Tsüaniide käsitletakse anorgaanilises keemias, kus nende hulka arvatakse ainult sinihappe soolad, samanimelised estrid aga kuuluvad nitriilidena orgaanilise keemia alla. Ka tsüaanhapnikhapped, tiotsüaanhapped ja nende estrid on piirjuhtumid. Ka metallorgaaniline keemia (metallorganüülid) ei kuulu ühemõtteliselt orgaanilise ega anorgaanilise keemia alla.
Ka mõned täiesti ebalooduslikuna tunduvad ained, näiteks plastid ja nafta, kuuluvad orgaaniliste ainete hulka, sest need koosnevad süsinikeühenditest nagu organismide koostisained. Nafta, maagaas ja süsi, mis on paljude sünteetiliste saaduste lähteained, on orgaanilise päritoluga. Kuigi need miljonite aastate jooksul tekkinud maavarad on algselt elusorganismidest tekkinud ei tähenda see, et need ained ning neist saadud ja sünteesitud orgaanilised ühendid oleksid osa kaasaegses maailmas, biosfääris toimuvast elusaine ringkäigust, elusloodusest. Organismides leiduvad biomolekulid on evolutsiooni jooksul kujunenud väga spetsiifilisteks molekulideks. Ühendid, mis koosnevad küll samadest keemilistest elementidest aga on erineva struktuuriga on keskkonnale võõrad ja ei lagune nagu eluslooduses olevad looduslikud orgaanilised ühendid. Sellepärast on suur hulk orgaanilise keemia saadustest, üksnes nime poolest orgaanilised (Mõiste orgaaniline tuli keemiasse (elus)organismides sisalduvate molekulide iseloomustamiseks, seostudes elavaga. Selle vastandiks oli eluta aine – anorgaaniline). Keskkonda sattununa, mitte lagunedes rikuvad nad maakera biosfääri loomulikku tasakaalu aastasadadeks.
Kõik elusolendid sisaldavad orgaanilisi aineid, nende seas aminohappeid, valke, süsivesikuid ja nukleiinhappeid. Orgaanilise keemia haru, mis tegeleb nende ainetega ja ainevahetusprotsessidega, nimetatakse biokeemiaks (või ka molekulaarbioloogiaks).
Ajalugu
[muuda | muuda lähteteksti]XVIII sajandil ja XIX sajandi alguses koosnesid keemiaõpikud valdavalt ainete loeteludest ja nende kirjeldustest. Aineid avastati üha juurde ja nende hulk kasvas kiiresti. Orgaaniline keemia kui iseseisev keemiaharu tekkis XIX sajandi alguses. 1808. aastal nimetas kuulus rootsi keemik Jakob Berzelius orgaanilisi aineid käsitleva valdkonna orgaaniliseks keemiaks ning avaldas õpiku, milles orgaanilisele keemiale oli pühendatud omaette peatükk. Selles ta väljendas ja propageeris tol ajal valitsenud seisukohta, et anorgaanilisi aineid saab valmistada laboratoorselt, orgaanilisi aga ei saa. Berzelius väitis, et orgaanilised ained tekivad ainult elusorganismides erilise elujõu (vis vitalis) toimel. Viimasest terminist tuleneb ka vitalistliku teooria nimetus. Vitalistid väitsid, et ainult elusorganismides esineb salapärane elujõud, mille mõjul lihtsamatest anorgaanilistest ühenditest tekivad keerulised orgaanilised ühendid.[5][6]
Esimesena hakkas Berzeliuse teooriat kahtluse alla seadma tema hea sõber ja õpilane, saksa keemik Friedrich Wöhler. Wöhler soojendas ammooniumtsüanaadi (NH4OCN) lahust, mida tol ajal loeti tüüpiliseks anorgaaniliseks ühendiks, ja täheldas, et ammooniumtsüanaat muutus uureaks ehk karbamiidiks (CO(NH2)2). Uurea on elusorganismis tekkiv valkude ainevahetuse lõppsaadus, mis väljub organismist uriini koostises. Nii anti 1828. aastal esimene hoop vitalismile. Seepeale väitsid vitalistid, et uurea süntees on võimalik vaid seetõttu, et uurea ei kujuta endast organismile vajalikku ainet, vaid on heitprodukt. Kuid järgnevatel aastatel sünteesiti ka mitmeid muid orgaanilisi ühendeid. 1842. aastal sünteesis vene teadlane Nikolai Zinin aniliini. Varem saadi seda taimse päritoluga värvainest indigost. 1848. aastal sünteesisid saksa keemik Hermann Kolbe ja inglise keemik Edward Frankland äädikhappe. Edasi tulid juba tehisrasv (1854) ja sajandi lõpul suhkrulaadne aine. Nende orgaaniliste sünteesidega kummutati vitalism lõplikult ning XX sajandi alguseks ei kaheldud enam võimalikkuses sünteesida mistahes orgaanilisi ühendeid. Sellest ajast alates peetaksegi orgaaniliste ühendite eripäraks nende koosnemist peamiselt süsinikust.[5] Seega on nimetus orgaaniline keemia pisut eksitav, ajalooline rudiment. Sest algselt mõeldi ju orgaanilise keemia all üksnes elusorganismides olevate ainete uurimisega seonduvat. (Tänapäeval tegeleb kitsamalt selle valdkonnaga biokeemia) Nii ongi nimetus "orgaaniline keemia" nüüdisajal ainult osaliselt õige, sisaldades nii elusorganismide kui ka eluslooduses puuduvate süsinikuühendite uurimist. Keemiateaduse arenedes on mõiste, nimetuse sisu laienenud ja oma esialgse piiri ületanud, nimi ise on jäänud aga samaks.

Orgaanilise keemia struktuuriteooria üheks loojaks peetakse F. A. Kekuléd, kes 1866. aastal seda benseeni struktuuri mõistmiseks rakendas. Tema teooria lähtepunktideks olid kolm eeldust:
- benseeni valem on C6H6;
- kõik benseeni vesinikud on võrdsed;
- igal süsinikul on 4 sidet (vastavalt valentssidemete teooriale ja hübridisatsioonile).
Kekulé arvas, et benseeni molekuli süsinikud on tsükliks ühendatud ning neli sidet saaks iga süsinik anda siis, kui üksik- ja kaksiksidemed paikneksid tsüklis vaheldumisi. Kekulé teoorias leiti peagi viga, kuid sellest arenes siiski välja resonantsvormide teooria, konjugatsiooni ja molekulide stabiliseerituse mõistmine. Samuti on tänapäevani kasutusel Kekulé väljapakutud benseeni struktuuri üleskirjutusviis.[7]
Orgaanilise keemia üheks iseseisvaks ja järjest arenevaks alaliigiks on bioorgaaniline keemia. Ehkki bioorgaaniline keemia on aastatuhandeid organismide sees toiminud, tekkis nendest protsessidest fundamentaalsem arusaam alles XIX sajandi lõpus ning biokeemia termin võeti kasutusele XX sajandi alguses. Enne seda ei võtnud orgaaniline keemia arvesse bioloogilisi protsesse ning bioloogia tegeles vaid morfoloogia ja organismide käitumisega. Kui bioloogid ja keemikud hakkasid koostööd tegema, oli võimalik bioloogilisi nähtusi kirjeldada molekulide tasandil ning see aitas seletada väga paljusid protsesse, mis elusorganismides toimuvad. Kekulé õpilane Otto Wallach oli esimene, kes hakkas uurima looduslikku päritolu molekulide struktuuri. Wallachi terpeenide uurimine pani alguse ka teiste biomolekulide struktuuriuuringutele ning ka sünteesile. 1952. aastaks oli Ameerika teadlane R. B. Woodward sünteesinud selliseid tuntud isoprenoide nagu testosteroon, progesteroon ja kolesterool. Woodwardi saavutused julgustasid keemikuid sünteesima üha keerukama struktuuriga molekule.[8]
Struktuur
[muuda | muuda lähteteksti]
Selleks et mõista orgaaniliste ühendite omadusi ja käitumist, tuleb aru saada nende ehitusest ehk struktuurist. Aatomite elektronstruktuurist selgub, kuidas paiknevad elektronid ja mille abil moodustuvad keemilised sidemed. Tuleb mõista aatomorbitaalide olemust ja molekulaarorbitaalide teooriat, samuti keemiliste elementide perioodilisussüsteemi. Molekulide ühinemisel tuleb arvestada keemilise sideme tüüpide ja omadustega, kindlasti ka tekkivate isomeeride omapäradega. Keemiliste reaktsioonide mõistmisel aitavad kaasa aktivatsioonienergia ja reaktsiooni kineetika.[2]
Liigitamine
[muuda | muuda lähteteksti]Maailmas tuntakse üle 10 miljoni orgaanilise ühendi, kusjuures igaühel neist on ainulaadsed keemilised ja füüsikalised omadused. Orgaanilised ühendid jagunevad paarikümnesse aineklassi, millel on struktuurilised omapärad.[3]
Funktsionaalrühmad
[muuda | muuda lähteteksti]Ühendid jagatakse aineklassidesse nendes sisalduvate funktsionaalrühmade järgi. Funktsionaalrühm on osa suuremast molekulist, mis koosneb aatomist või aatomite grupist ning millel on kindlad keemilised omadused. Igal funktsionaalgrupil on iseloomulik reaktiivsus, mida saab varieerida, kui muuta molekulis funktsionaalgrupi asendit või kõrvalrühmi. Orgaanilises keemias on levinud funktsionaalrühmad hüdroksüülrühm, alküülrühm, karboksüülrühm, ester, eeter, amiin, amiid, nitrorühm, aminorühm.
Alifaatsed ja aromaatsed ühendid
[muuda | muuda lähteteksti]Orgaanilises keemias on väga levinud ka ühendite liigitamine nende omaduste järgi. Näiteks süsivesinikud jagunevad kahte suurde alaklassi:
- aromaatsed ühendid on molekulid, milles on konjugeeritud kaksiksidemed. Nii asetsevana on elektronid molekulis delokaliseeritud ning seega ühend väga stabiilne;
- alifaatsed ühendid on molekulid, kus elektronid pole delokaliseeritud. Alifaatsed ühendid võivad sisaldada ka kaksiksidemeid, kuid need pole omavahel konjugeeritud ja see vähendab ühendite stabiilsust.
Alifaatseid ja aromaatseid süsivesinikke saab vaadelda kõikide orgaaniliste ühendite lähtealusena.[2]
Polümeerid
[muuda | muuda lähteteksti] Pikemalt artiklis polümeerid
Pikemalt artiklis polümeerid Pikemalt artiklis polümerisatsioon
Pikemalt artiklis polümerisatsioon
Polümeerid on kõrgmolekulaarsed ained, mis koosnevad makromolekulidest. Enamasti koosneb makromolekul väikestest molekulidest ehk monomeeridest. Levinud on polümeeride liigitamine orgaanilisteks ja anorgaanilisteks polümeerideks. Orgaanilised polümeerid omakorda jagunevad kolmeks:
- looduslikud polümeerid on kõikjal meie ümber ning tekivad elusorganismides. Kõige sagedamini esinevad looduslike polümeeride klassid on nukleiinhapped, valgud, polüsahhariidid, polüpreenid ja alifaatsed polüestrid;
- tehispolümeerid on modifitseeritud looduslikud polümeerid. Neid valmistatakse looduslikest polümeeridest keemilise töötlemise teel. Levinuimad tehispolümeerid on tsellofaan, pargitud nahk ja kautšuk;
- sünteetilised polümeerid on inimeste sünteesitud polümeerid. Neid toodetakse keemiatööstustes naftast ja maagaasist. Levinuimad sünteetilised polümeerid on polüetüleen, polüvinüülkloriid ja polütetrafluoroetüleen.[9]
Biomolekulid
[muuda | muuda lähteteksti]Biomolekulid on orgaanilised ühendid, millest kõik elusorganismid koosnevad. Biomolekule saab kirjeldada samade omaduste abil nagu teisi orgaanilisi ühendeid, mida saadakse laboratoorselt ja mida eluslooduses pole. Eriti oluliseks muutub aga stereokeemia, sest see tagab bioloogiliste protsesside spetsiifilisuse. Biomolekulid jagunevad neljaks: valgud, sahhariidid, nukleiinhapped ja lipiidid. Biomolekulidega tegelevat orgaanilise keemia alaklassi nimetatakse bioorgaaniliseks keemiaks. Bioorgaaniline keemia tegeleb kõige elava keemilise koostise, struktuuride, muundumiste ja spetsiifiliste funktsioonidega.[10]
Esitus
[muuda | muuda lähteteksti]Orgaaniliste ühendite hõlpsamaks ja kõigile arusaadavamaks kirjapanekuks on loodud mitmeid lihtsustusi. Enim kasutatavad struktuuride kirjapanemise viisid on esitatud tabelis koos näidetega.
| Nimetus | Propaan |
|---|---|
| Summaarne valem (brutovalem) | C3H8 |
| Lihtsustatud struktuurivalem | CH3CH2CH3 |
| Tasapinnaline struktuurivalem | 
|
| Graafiline valem | 
|
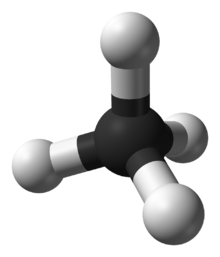
| 3D-kujutis | 
|
Nimetus
[muuda | muuda lähteteksti] Pikemalt artiklis orgaaniliste ühendite süstemaatiline nomenklatuur
Pikemalt artiklis orgaaniliste ühendite süstemaatiline nomenklatuur
Nomenklatuur on kommunikatsioonivahend, mis aitab struktuuri ja nimetust üks ühele vastavusse viia. Levinumad nimetusviisid on toodud tabelis koos näidetega.
| Nomenklatuur | Näide | Nimi |
|---|---|---|
| Süstemaatiline (IUPAC) |  |
karbonüüldiamiid |
| Poolsüstemaatiline |  |
karbamiid |
| Triviaalne |  |
uurea |
Reaktsioonid
[muuda | muuda lähteteksti] Pikemalt artiklis orgaaniline reaktsioon
Pikemalt artiklis orgaaniline reaktsioon
Orgaanilisi reaktsioone saab liigitada mitmeti, ent kõige üldisemalt saab nad jaotada 3 kategooriasse:[11]
- Asendusreaktsioonid on reaktsioonid, milles üks rühm asendab teise. Asendusreaktsioonid on iseloomulikud küllastunud ühendite puhul;
- Liitumisreaktsioonid on reaktsioonid, milles üks ühend või rühm liitub teise külge. Liitumisreaktsioonid on iseloomulikud küllastumata ühenditele;
- Elimineerimisreaktsioonid on reaktsioonid, milles eraldub uus rühm. Elimineerimisreaktsioonid on iseloomulikud küllastumata ühenditele.
Tasub teada, et paljud reaktsioonid, mida esmapilgul võib pidada asendusreaktsioonideks, toimivad esmalt liitumis- ja seejärel elimineerimismehhanismide järgi. Samuti võib pidada oksüdeerumis- ja redutseerumisreaktsioone vastavalt elimineerimis- või lisamisreaktsiooni mehhanismi osaks.
Kõik keemilised reaktsioonid toimivad olemasolevate sidemete lõhustamise ja uute sidemete tekkimise teel. Sideme katkemise järgi jagatakse reaktsioonid kaheks:
- homolüütilisel reaktsioonil jääb sideme katkemisel kummalegi aatomile üks elektron ja seega moodustuvad radikaalid. Radikaalid on väga reaktsioonivõimelised;
- heterolüütilisel reaktsioonil lähevad mõlemad sideme elektronid ühele aatomile ja seega moodustuvad ioonid. Reagente, mis heterolüütilisi reaktsioone läbi viivad, nimetatakse nukleofiilideks ja elektrofiilideks.[11]
Lisaks mainitud põhikategooriatele on suur hulk tööstustele olulisi polümerisatsioonireaktsioone.
Vaata ka
[muuda | muuda lähteteksti]- orgaanilised ühendid
- orgaaniline reaktsioon
- orgaaniline süntees
- orgaaniliste ühendite süstemaatiline nomenklatuur
- süsinik
- analüütiline keemia
- füüsikaline keemia
- kolloidkeemia
Viited
[muuda | muuda lähteteksti]- ↑ Breitmaier, Jung 2009:1
- ↑ 2,0 2,1 2,2 Atkins, P.; Jones, L. Keemia alused. Teekond teadmiste juurde; Tartu Ülikooli Kirjastus, 2012, lk 855.
- ↑ 3,0 3,1 McMurry, J. Fundamentals of organic chemistry; Brooks/Cole: Belmont, United States of America, 1994, pp 1–2, 32.
- ↑ "Keemia. Orgaaniline keemia gümnaasiumile" Mati Karelson, Aarne Tõldsepp. Kirjastus Koolibri, Tallinn, 2007 a. lk 10.
- ↑ 5,0 5,1 Tuulmets, A. Orgaaniline keemia XI klassile; Koolibri: Tallinn, 1998, lk 6.
- ↑ Greenwood, N. N.; Earnshaw, A. Chemistry of the elements; Elsevier Butterworth-Heinemann: Amsterdam, 2008.
- ↑ Carey, F. A.; Giuliano, R. M. Orgaaniline keemia; Tallinna Raamatutrükikoda, 2014, lk 430–432.
- ↑ Poulter C. D. Bioorganic Chemistry. A Natural Reunion of the Physical and Life Sciences. J. Org. Chem. 2009, 74, 2631–2645.
- ↑ Loog, O.; Timotheus, H., Järv, J. Orgaanilised polümeerid; Tartu Ülikooli Kirjastus, 2012, lk 1, 21, 121, 161–171.
- ↑ Lehninger, A. L.; Nelson, D. L.; Cox, M. M. Principles of Biochemistry; Worth Publishers: New York, 1993, p 1.
- ↑ 11,0 11,1 Hanson, J. R. Functional Group Chemistry; The Royal Society of Chemistry: Cambridge, 2001, pp 1, 15–16.
Kirjandus
[muuda | muuda lähteteksti]- Eberhard Breitmaier, Günther Jung. Organische Chemie: Grundlagen, Verbindungsklassen, Reaktionen, Konzepte, Molekülstruktur, Naturstoffe, 6., ümbertöötatud trükk, Thieme 2009.
Välislingid
[muuda | muuda lähteteksti]| Pildid, videod ja helifailid Commonsis: Orgaaniline keemia |