Benseen
Benseen on orgaaniline keemiline ühend molekulvalemiga C6H6. Selle molekul koosneb kuuest ringikujuliselt liitunud süsinikuaatomist, millest iga küljes on üks vesiniku aatom. Benseen on lihtsaim aromaatne süsivesinik[1]. Benseeni tähistatakse valemites Ph. Benseen esineb naturaalselt naftas.
Benseen on värvitu ja väga tuleohtlik magusa lõhnaga vedelik. Tema keemistemperatuur on +80,1 °C, sulamistemperatuur on +5,5 °C ja tihedus 879 kg/m³[1]. Benseeni lubatud piirkontsentratsioon tööruumide õhus on 20 mg/m³[1]. Plahvatusohtlik kontsentratsioon õhus on 1,5–8 mahuprotsenti.[1]
Benseeni kasutatakse enamasti lähteainena raskete kemikaalide tootmiseks, näiteks etüülbenseeni ja isopropüülbenseeni toodetakse miljardeid tonne aastas. Kuna benseenil on kõrge oktaaniarv, on see tähtis koostisosa bensiinis. Enamik mittetööstuslikust kasutusest on piiratud benseeni kantserogeensuse tõttu.
Ajalugu
[muuda | muuda lähteteksti]Sõna "benseen" tuleb ajalooliselt "bensoiinist", aromaatsest vaigust, mida teati Euroopas juba 15. sajandil Kagu-Aasia tootena. Bensoiinist saadi happeline materjal, mida kutsuti "bensoiini lilledeks" ja mis tõenäoliselt oli bensoehape.
Michael Faraday isoleeris ja identifitseeris esimesena benseeni 1825. aastal õlisest jäägist ning nimetas selle vesiniku bikaburetiks.[2]
Benseeni empiiriline valem oli ammu teada, kuid selle polüküllastamata struktuuri ühe vesinikuga iga süsiniku kohta oli raske määrata. 1865. aastal avaldas Saksa keemik Friedrich August Kekulé prantsuskeelse artikli, kus väitis, et struktuur koosnes kuuelülilisest süsinikuaatomite ringist vahelduvate üksik- ja kaksiksidemetega. Aasta hiljem andis ta samal teemal välja palju pikema saksakeelse artikli.[3][4] Kekulé kasutas varasematel aastatel kogutud eksperimenditulemusi, mis näitasid, et igal benseeni monoderivaadil oli ainult üks isomeer ja igal diderivaadil oli kolm derivaati, mida tänapäeval nimetatakse orto-, meta- ja paraasendiks.
Benseeni tsüklilisuse tõestas 1929. aastal kristallograaf Kathleen Lonsdale.[5][6]
19. sajandil ja 20. sajandi alguses kasutati benseeni meeldiva lõhna tõttu aftershave-vedelikuna. Enne 1920. aastat kasutati benseeni laialdaselt tööstusliku lahustina. Pärast selle toksilisuse ilmnemist asendati see teiste lahustitega, eriti tolueeniga (metüülbenseeniga), millel on sarnased füüsikalised omadused, aga mis pole nii kantserogeenne.

1903. aastal populariseeris Ludwig Roselius benseeni kasutamist kofeiinitustamiseks. Benseen oli tähtis koostisosa paljudes tarbekaupades, näiteks värvilahustites, kummiliimides ja muudes süsivesinikke sisaldavates ainetes. Enamik firmasid lõpetasid benseeni kasutamise 1950. aastatel, kuid mõned jätkasid kuni 1970. aastate lõpuni, kui ilmnesid seosed leukeemiasurmade ja Goodyeari Pliofilmi tootmise vahel. Selle ajani müüdi paljudes kauplustes benseeni väikestes purkides tavakasutuseks. Paljud õpilased said koolis ja ülikoolis benseeniga katseid tehes tervisekahjustusi. Tänapäevaks on see ohtlik praktika lõpetatud.
Struktuur
[muuda | muuda lähteteksti] Pikemalt artiklis Aromaatsus
Pikemalt artiklis Aromaatsus
Benseeni struktuur tekitab erilise probleemi, kuna sidemete pikkuse kvantitatiivseks selgitamiseks peab esinema kas elektronide delokalisatsioon (molekulaarorbitaalide teooria) või π-orbitaalide spinnpaardumine (valentssidemete teooria)[7].

Röntgendifraktsioon näitab, et kõik 6 süsinikuaatomite vahelist sidet benseenis on sama pikkusega, 140 pikomeetrit (pm). See on pikem kui kaksikside (135 pm) ja lühem kui üksikside (147 pm). See vahepealne pikkus on vastavuses elektronide delokalisatsiooniga: C-C siduvad elektronid on võrdselt jagatud kõigi kuue süsinikuaatomi vahel. Benseenil on 8 vesinikuaatomit vähem kui vastaval alkaanil heksaanil. Molekul on planaarne[8]. Molekulaarorbitaalide teooria järgi on benseeni molekulis 3 delokaliseeritud π-orbitaali kõigi kuue aatomi vahel, valentssidemete teooria järgi tulenevad aromaatsed omadused kõigi kuue π-orbitaali spinnpaardumisest[9][10][11][12] See stabiilsus on tõenäoliselt aromaatsete ühendite omapäraste omaduste põhjuseks. Näitamaks sidemete delokaliseeritud iseloomu, kujutatakse benseeni tihti ringiga kuusnurkse aatomiteahela sees.
Benseeni derivaadid
[muuda | muuda lähteteksti] Pikemalt artiklis Areenid
Pikemalt artiklis Areenid
Benseenist saab mitmeid tähtsaid keemilisi ühendeid, kui asendada üks või rohkem vesinikku mõne teise funktsionaalrühmaga. Näited lihtsatest benseeni derivaatidest on fenool, tolueen ja aniliin, mida esitatakse vastavalt PhOH (hüdroksübenseen), PhMe (metüülbenseen) ja PhNH2 (aminobenseen). Kaht benseenirõngast omavahel liites saadakse bifenüül. Rohkem vesinikke kaotades saadakse "kokkusulanud" aromaatsed süsivesinikud, näiteks naftaleen ja antratseen. Vesinikuvaba süsiniku allotroop grafiit koosneb paljudest "kokkusulanud" süsinikurõngastest.
Heterotsüklistes ühendites on süsiniku aatomid benseenituumas asendatud teiste elementide aatomitega. Kõige tähtsamad heterotsüklilised ühendid on lämmastikku sisaldavad tuumad. Asendades tuumas ühe süsiniku aatomi lämmastikuga, saadakse püridiin (C5H5N). Kuigi benseen ja püridiin on struktuuri poolest sarnased, ei ole benseenist võimalik püridiini sünteesida. Kaks süsiniku aatomit lämmastikuga asendades saadakse olenevalt teise lämmastiku asukohast kas püridasiin (1,2-diasiin), pürimidiin (1,3-diasiin) või pürasiin (1,4-diasiin).
Tootmine
[muuda | muuda lähteteksti]Benseeni tööstuslikuks tootmiseks kasutatakse nelja keemilist protsessi: katalüütiline reformatsioon, tolueeni hüdrodealküleerimine, tolueeni disproportsioneerumine ja aurukrakkimine. ATSDRi benseeni toksikoloogilise profiili kohaselt toodeti aastatel 1978–1981 USA-s umbes pool benseenist katalüütilise reformatsiooni teel.
Teise maailmasõjani toodeti enamik benseenist terasetööstuses koksi kõrvasaadusena. Alates 1950. aastatest suurenes nõudlus benseeni järele, eriti kasvava polümeeritööstuse tõttu. Benseeni hakati tootma naftast.
Katalüütilises reformatsioonis segatakse süsivesinike segu keemistemperatuuride vahemikus 60–200 °C vesinikuga ja juhitakse katalüsaatorile (plaatinakloriid või reeniumkloriid) 500–525 °C ja rõhu 8–50 atm juures. Sellistes tingimustes moodustavad alifaatsed ühendid rõngaid, sealhulgas aromaatseid süsivesinikke.
Tolueeni hüdrodealküleerimisel muundatakse tolueen benseeniks. Vesinikintensiivses protsessis segatakse tolueen vesinikuga ning juhitakse kroom, molübdeen või plaatinaoksiid katalüsaatori 500–600 °C ja 40–60 atm juures.
C6H5CH3 + H2 → C6H6 + CH4
Kasutusalad
[muuda | muuda lähteteksti]Benseeni kasutatakse enamasti vaheühendina teiste kemikaalide tootmisel. Umbes 80% benseenist kasutatakse kolme kemikaali tootmiseks: etüülbenseen, isopropüülbenseen ja tsükloheksaan. Kõige laialdasemalt toodetav on stüreeni lähteaine etüülbenseen. Stüreenist toodetakse mitmesuguseid polümeere ja plaste. Kumeen (isopropüülbenseen) muundatakse fenooliks vaikude ja liimide tootmiseks. Tsükloheksaani kasutatakse nailoni tootmiseks. Väiksemad kogused benseeni lähevad kummide, lubrikantide, värvide, detergentide, ravimite, lõhkeainete ja pestitsiidide tootmiseks.
Nii Euroopas kui USA-s kulub 50% benseenist etüülbenseeni, 20% kumeeni ja 15% tsükloheksaani tootmiseks. [viide?] Kesk-Aasias kasvab benseeni tootmine ja nõudlus kasvavad kõige jõudsamalt. Arvatakse, et 2018. aastaks tõusevad need vastavalt 3,7 ja 3,3 protsenti. Aasia ja Vaikse ookeani piirkond aga jätkab nõudluse domineerimist peaaegu poolega turust.[13]
Bensiinilisandina suurendab benseen oktaaniarvu ja vähendab mootoridefekte. 1950. aastatel asendati see tetraetüülpliiga.
Laboratoorsetes uuringutes kasutatakse benseeni asemel tänapäeval tolueeni, mille lahustamisomadused on sarnased, kuid mis pole nii mürgine.

Reaktsioonid
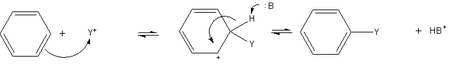
[muuda | muuda lähteteksti]Kõige tavalisemad benseeni reaktsioonid on seotud prootoni asendamisega teiste rühmadega.[14] Elektrofiilne aromaatne asendusreaktsioon on tavaline meetod benseeni derivatiseerimiseks. Benseen on piisavalt nukleofiilne, et toimuks asendusreaktsioon atsüülrühmrühmaga ja alküül karbokatiooniga.
Levinuim näide sellest reaktsioonist on benseeni etüleerimine.
1999. aastal toodeti umbes 25 miljonit tonni etüülbenseeni.[15]
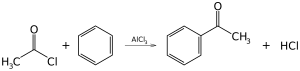
Elektrofiilse aromaatse asendusreaktsiooniga saab benseeni tuumale lisada mitmeid kasulikke funktsionaalrühmi. Benseeni sulfoneeritud derivaadid on kasulikud detergendid. Nitreerimise käigus saadakse nitrobenseen, mis on aniliini lähteaine. Kloorimine, mille käigus saadakse klorobenseen, toimub klooriga katalüsaatori, näiteks alumiinium(III)kloriidi, juuresolekul. Hüdrogeenimisel muundatakse benseen ja derivaadid tsükloheksaaniks ja selle derivaatideks. Benseen on hea ligand vähevalentsete organometallide keemias.
Mõju tervisele
[muuda | muuda lähteteksti]
Benseen suurendab vähi ja muude haiguste ohtu. Ta on kurikuulus luuüdihaiguste põhjustaja. Paljud epidemioloogilised, kliinilised ja laboratoorsed uuringud seovad benseeni aneemiaga, leukeemiaga ja luuüdi ebanormaalsustega.[16][17]
Ameerika Ühendriikide Tervishoiu- ja Teenindusministeerium klassifitseerib benseeni inimese kantserogeeniks. Pikaajaline kokkupuude suure benseenisisaldusega õhuga põhjustab leukeemiat.[18]
Vaata ka
[muuda | muuda lähteteksti]Viited
[muuda | muuda lähteteksti]- ↑ 1,0 1,1 1,2 1,3 Tehnikaleksikon, lk. 49
- ↑ Faraday, M. (1825). "On new compounds of carbon and hydrogen, and on certain other products obtained during the decomposition of oil by heat". Philosophical Transactions of the Royal Society of London. 115: 440–466. DOI:10.1098/rstl.1825.0022. ISSN 0261-0523. JSTOR 107752.
- ↑ Kekulé, F. A. (1865). "Sur la constitution des substances aromatiques". Bulletin de la Société Chimique de Paris. 3: 98–110.
- ↑ Kekulé, F. A. (1866). "Untersuchungen über aromatische Verbindungen] (Investigations of aromatic compounds)". Liebigs Annalen der Chemie und Pharmacie. 137 (2): 129–36. DOI:10.1002/jlac.18661370202.
- ↑ Lonsdale, K. (1929). "The Structure of the Benzene Ring in Hexamethylbenzene". Proceedings of the Royal Society. 123A: 494.
- ↑ Lonsdale, K. (1931). "An X-Ray Analysis of the Structure of Hexachlorobenzene, Using the Fourier Method". Proceedings of the Royal Society. 133A (822): 536–553. Bibcode:1931RSPSA.133..536L. DOI:10.1098/rspa.1931.0166.
- ↑ David Cooper (2002). Valence Bond Theory. Elsevier. Lk 125–131. ISBN 0-080-54349-9.
- ↑ Moran D, Simmonett AC, Leach FE, Allen WD, Schleyer PV, Schaefer HF (2006). "Popular Theoretical Methods Predict Benzene and Arenes To Be Nonplanar". Journal of the American Chemical Society. 128 (29): 9342–3. DOI:10.1021/ja0630285. PMID 16848464.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Cooper, David L.; Gerratt, Joseph; Raimondi, Mario (1986). "The electronic structure of the benzene molecule". Nature. 323 (6090): 699. Bibcode:1986Natur.323..699C. DOI:10.1038/323699a0.
- ↑ Pauling, Linus (1987). "Electronic structure of the benzene molecule". Nature. 325 (6103): 396. Bibcode:1987Natur.325..396P. DOI:10.1038/325396d0.
- ↑ Messmer, Richard P.; Schultz, Peter A. (1987). "The electronic structure of the benzene molecule". Nature. 329 (6139): 492. Bibcode:1987Natur.329..492M. DOI:10.1038/329492a0.
- ↑ Harcourt, Richard D. (1987). "The electronic structure of the benzene molecule". Nature. 329 (6139): 491. Bibcode:1987Natur.329..491H. DOI:10.1038/329491b0.
- ↑ Market Study on Benzene by Ceresana Research. Ceresana.
- ↑ Stranks, D. R.; M. L. Heffernan, K. C. Lee Dow, P. T. McTigue, G. R. A. Withers (1970). Chemistry: A structural view. Carlton, Victoria: Melbourne University Press. Lk 347. ISBN 0-522-83988-6.
{{cite book}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Welch, Vincent A.; Fallon, Kevin J. and Gelbke, Heinz-Peter (2005) “Ethylbenzene” in Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, DOI:10.1002/14356007.a10_035.pub2
- ↑ Kasper, Dennis L.et al. (2004) Harrison's Principles of Internal Medicine, 16th ed., McGraw-Hill Professional, p. 618, ISBN 0071402357.
- ↑ Merck Manual, Home Edition, "Overview of Leukemia".
- ↑ WHO. INTERNATIONAL AGENCY FOR RESEARCH ON CANCER, IARC Monographs on the Evaluation of Carcinogenic Risks to Humans, Overall Evaluations of Carcinogenicity: An Updating of IARC Monographs, Volumes 1 to 42, Supplement 7
Välislingid
[muuda | muuda lähteteksti]| Pildid, videod ja helifailid Commonsis: Benzene |
- Benzene (www.eco-usa.net)
- International Chemical Safety Card 0015
- USEPA Summary of Benzene Toxicity
- NIOSH Pocket Guide to Chemical Hazards
- Dept. of Health and Human Services: TR-289: Toxicology and Carcinogenesis Studies of Benzene
- Video Podcast Sir John Cadoganist pidamas loengut benseenist pärast Faradayd aastal 1991
- Substance profile
- NLM Hazardous Substances Databank – Benzene