Estrid
| See artikkel räägib orgaanilistest ühenditest; Piibli tegelase kohta vaata artiklit Ester. |
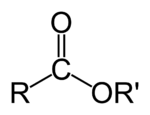
Estrid on orgaanilised ühendid, mis tekivad happe vesinikuaatomite asendumisel süsivesiniku radikaalidega. Karboksüülhapetest tekivad estrid karboksüülrühmade vesinikuaatomite asendumisel süsivesiniku radikaalidega.
Üldvalem[muuda | muuda lähteteksti]
Estrite üldvalem on R–COO–R', kus R ja R' on süsivesiniku radikaalid, kusjuures R ja R' võivad olla ühesugused radikaalid.
Nomenklatuur[muuda | muuda lähteteksti]
Estrite nimetused moodustatakse nagu karboksüülhappe sooladelgi (esimene osa nimest tuleb alkoholist ning teine vastavast karboksüülhappest):
- CH3CH2CH2COOCH2CH3: etüülbutanaat
- CH3CH2CH2COOCH2CH2CH3: propüülbutanaat
- CH3CH2COOCH3: metüülpropanaat
- CH3COOCH2CH2CH3: propüületanaat ehk propüülatsetaat
Estrid on ainult sellised ühendid, kus mõlemal pool on süsivesiniku radikaal. Järgnev ühend on küll sarnase ehitusega nagu ester, kuid ei ole ester, vaid tavaline karboksüülhappe sool.
- CH3CH2COOK: kaaliumpropanaat
Füüsikalised omadused[muuda | muuda lähteteksti]
Madalad estrid on vedelikud. Kõrgemad estrid on tahked ained. Nad lahustuvad orgaanilistes lahustes, vees aga vähe või peaaegu üldse mitte. Keemistemperatuur on madalam kui vastavatel alkoholidel ja karboksüülhapetel. Estrid on enamasti lenduvad. Pika süsiniku ahelaga hapete ja alkoholide estrid ei lendu ja on seetõttu lõhnatud.
Lõhn[muuda | muuda lähteteksti]
Mõnel vedelal estril on meeldiv lõhn.
| Valem | Nimetus | Lõhn |
|---|---|---|
| HCOOC2H5 | etüülmetanaat | rummi |
| CH3COOC4H9 | butüületanaat | banaani |
| CH3COOC5H11 | pentüületanaat | pirni |
| C3H7COOC2H5 | etüülbutanaat | ananassi |
| CH3COOC8H17 | oktüületanaat | apelsini |
| C3H7COOC5H11 | pentüülbutanaat | aprikoosi |
| C4H9COOC5H11 | isopentüülpentanaat | õuna |
Kasutusalad[muuda | muuda lähteteksti]
Estreid kasutatakse lille- ja puulõhnade tõttu puuviljaessentsidena, näiteks karastusjookides, kondiitritoodetes, seebi- ja parfümeeriatööstuses.
Estrid on lahustiteks värvidele ja lakkidele.
Neid kasutatakse ka ravimite valmistamisel.
Suurtes kogustes vajatakse estreid plastide ja kiudainete tootmiseks.
Keemilised omadused[muuda | muuda lähteteksti]
Estrite tähtsaim keemiline omadus on hüdrolüüs ehk klassikalises mõistes reaktsioon veega katalüsaatori juuresolekul ehk antud juhul neutraalne ja happeline hüdrolüüs. Happeline hüdrolüüs on pöörduv, neutraalne aga mitte.
Leidumine[muuda | muuda lähteteksti]
Estreid leidub eeterlike õlidena taimedes (näiteks apelsinikoores). Veel on nendeks rasvad ja vahad.
Saamine[muuda | muuda lähteteksti]
Vanim estrite saamise viis oli nende tootmine taimedest eeterlike jm. õlidena ja loomadest rasvana. Kui peenestatud taimemassi juhitakse veeauru, siis võtab see kaasa lenduvad eeterlikud õlid. Muid rasvu ja õlisid saab kudedest eraldada veega keetmise või lihtsalt pressimise teel.
Estrid tekivad karboksüülhapete ja alkoholide reageerimise tulemusena. Seda nimetatakse esterdamiseks ehk estrifikatsiooniks .
CH3COOH + CH3CH2OH = CH3COOCH2CH3 + H2O
Tekib etüületanaat ehk etüülatsetaat.
Mineraalhapete estrid[muuda | muuda lähteteksti]
Lämmastikhappe estrid põlevad kergesti. Paljud neist võivad lõhkeda, sealhulgas tugevalt nitreeritud nitrotselluloos ja nitroglütseriin.
Ohutus[muuda | muuda lähteteksti]
See alajaotus tuleb alles kirjutada.
