Pseudomonas aeruginosa
| Pseudomonas aeruginosa | |
|---|---|
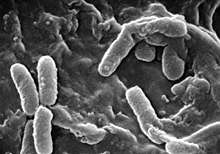 Pseudomonas aeruginosa elektronmikroskoobist vaadelduna | |
| Taksonoomia | |
| Riik |
Bacteria |
| Hõimkond |
Proteobacteria |
| Klass |
Gammaproteobacteria |
| Selts |
Pseudomonadales |
| Sugukond |
Pseudomonadaceae |
| Perekond |
Pseudomonas |
| Liik |
Pseudomonas aeruginosa |
| Binaarne nimetus | |
|
Pseudomonas aeruginosa Migula 1900 | |
Pseudomonas aeruginosa on gramnegatiivne aeroobne kepikujuline bakter. Ta on laialdase levikuga oportunistlik patogeen, kes on võimeline tekitama infektsioone nii loomadel (sh inimesel) kui ka taimedel. 1,5–3,0 µm pikkused kepikesekujulised rakud on püotsüaniini tõttu iseloomuliku roheka värvusega.
Vähenõudlikkus toitainete suhtes võimaldab P. aeruginosa'l asustada väga erinevaid keskkondi ja ta on üheks põhiliseks haiglainfektsioonide põhjustajaks. Esimesena kirjeldas teda 1900. aastal Walter Migula. Aastal 2000 sekveneeriti tüüptüve PAO1 6,3 Mbp suurune genoom.[1]
Süstemaatika
[muuda | muuda lähteteksti]Pseudomonas aeruginosa on gramnegatiivne ja oksüdaaspositiivne[2] Pseudomonadaceae sugukonda ja gammaproteobakterite klassi kuuluv bakter. 16S ribosomaalse RNA (rRNA) analüüsi põhjal kuulub sugukonda vaid perekond Pseudomonas, mis on omakorda jaotatud kaheksasse alagruppi. P. aeruginosa on pseudomonaadide perekonna tüüpliik.[3] Perekonda kuulub kokku 12 liiki.[4]
Levik
[muuda | muuda lähteteksti]P. aeruginosa on laialt levinud nii pinnases kui ka vees. Looduses esineb P. aeruginosa biokilena substraadil või planktoonilise ainurakse vormina. Vibur võimaldab tal vees kiiresti liikuda ja erinevatele pindadele kinnituda.
P. aeruginosa optimaalne kasvutemperatuur on 37 °C, kuid ta suudab kasvada ka 42 °C juures.
Ta on tavaline bakter pinnases, vees, naha mikroflooras ja enamikus tehiskeskkondades ning suudab ellu jääda ka anaeroobsetes tingimustes. Kasvades diisli- ja reaktiivkütustel, põhjustab ta bakteriaalset korrosiooni.
Morfoloogia
[muuda | muuda lähteteksti]

Tegu on gramnegatiivse kepikesekujulise bakteriga, kelle läbimõõt on 0,5–0,8 µm ja pikkus 1,5–3,0 µm.[5] Kepikese ühes otsas paiknev vibur võimaldab unipolaarset liikumist. Eritatavatest eksopolüsahhariididest moodustub raku ümber limakapsel, mis soodustab liikumist, kaitseb fagotsütoosi ja antikehade eest ning takistab väljutamist loomade hingamisteedest. P. aeruginosa sekreteerib mitmeid pigmente, mis sõltuvalt söötme koostisest annavad kolooniatele värvuse – püotsüaniin (sinakasroheline), püoverdiin (kollakasroheline ja fluorestseeruv) ja püorubiin (punakaspruun). E. O. King, M. K. Ward ja D. E. Raney töötasid välja Pseudomonas'e agari A (Kingi A-sööde) püotsüaniini ja püorubiini tuvastamiseks ning Pseudomonas 'e agari F (Kingi B-sööde) fluorestsiini määramiseks.[6]
Genoom
[muuda | muuda lähteteksti]Tüüptüve PAO1 genoom sekveneeriti täielikult 2000. aastal. Genoomi suurus on 6,3 Mbp ja see sisaldab 5570 geeni. G+C-rikas P. aeruginosa kromosoom koosneb konserveerunud ja varieeruvatest osadest. Konserveerunud lõigud on kollineaarsed, sisaldavad vähe kordusjärjestusi ja üksikuid suure sagedusega lookusi. Olulisemateks on püoverdiini lookus, viburivalkude sünteesi regulonid, pilA ja O-antigeeni sünteesi lookus. Varieeruvad segmendid paiknevad hajusalt üle genoomi, neist umbes 1/3 asuvad vahetult tRNA või tmRNA geenide läheduses. Genoomi mitmekesistumist põhjustab pKLC102/PAGI-2 perekonna genoomsete saarekeste lülitumine tRNALys või tRNAGly geenidesse (vastavalt lüsiini ja glütsiini transportimiseks vajalike tRNA molekulide sünteesi kodeerivad järjestused). Saarekeste mõju bakteri metaboolselt olulistele geenidele on varieeruv, kuid tehisgeenide abil on näidatud nende horisontaalset ülekannet kloonidesse ja teistesse liikidesse. Harvaesinevate haigustega patsiente nakatades suureneb tõenäosus deletsioonide, genoomi ümberkorralduste (nt translokatsioon) ja funktsioonita mutatsioonide kuhjumiseks. P. aeruginosa populatsiooni moodustavad paar domineerivamat laialdase levikuga tüve.
16S rRNA järjestuse alusel on eristatud mitmeid tüvesid:
ATCC 10145
CCUG 551
CFBP 2466
CIP 100720
DSM 50071
JCM 5962
LMG 1242
NBRC 12689
NCCB 76039
NCIMB 8295
NCTC 10332
NRRL B-771
Ainevahetus
[muuda | muuda lähteteksti]Metabolism on aeroobne ja mittefermenteeriv, kuid siiski on Pseudomonas aeruginosa võimeline kasvama ka anaeroobsetes tingimustes, kui keskkonnas leidub nitraatioone (NO3-), mida kasutada elektronide aktseptorina.[7] Sobilikuks on osutunud ka substraat, mis sisaldab arginiini, mille P. aeruginosa fosforüülib ornitiiniks.[8]
P. aeruginosa on toitainete osas vähenõudlik. Ta on võimeline kasvama ka peaaegu destilleeritud vees – väga väheste toitainetega tingimustes. Lihtsaim sööde P. aeruginosa laboratoorsetes tingimustes kasvatamiseks sisaldab süsinikuallikana atsetaati ja lämmastikuallikana ammooniumsulfaati. Sarnaselt teiste pseudomonaadidega on P. aeruginosa metaboolselt mitmekülgne. Orgaaniliste ühendite olemasolu keskkonnas ei ole talle vajalik, kuigi ta suudab substraadina kasutada rohkem kui 75 orgaanilist ühendit. Ta on vastupidav füüsikalistele teguritele, sh temperatuurile. Ta on vastupidav ka suurele soolakontsentratsioonile ja paljudele laialdasemalt kasutatavatele antibiootikumidele. Seedeensüümi SdsA abiga suudab ta lagundada ka naatriumlaurüülsulfaati (SDS). Seetõttu saab ta kasvada ka suure SDS-sisaldusega kasvukohtades (nt šampoonid), kus enamik teisi baktereid hukkub.[9]
Patogeensus
[muuda | muuda lähteteksti]
Pseudomonas aeruginosa on oportunistlik patogeen, nakatades nii loomi kui ka taimi. Levinumad on P. aeruginosa põhjustatud kopsu-, kuseteede-, põletushaavade ja vereinfektsioonid. Ta on sagedane põletushaavade ja sisekõrvainfektsioonide tekitaja. Väga vastupidava biokilena katab ta meditsiiniseadmeid ja -tarvikuid (nt kateetreid), olles oluliseks haiglainfektsioonide põhjustajaks. Püotsüaniin on üks bakteri virulentsusfaktor. Püotsüaniini tekitatud oksüdatiivne stress võib põhjustada organismi surma (nt C. elegans'i puhul). On leitud, et salitsüülhape inhibeerib püotsüaniini tootmist.[10] Riskirühmaks on tsüstilise fibroosiga patsiendid, kelle immuunsüsteem on nõrgenenud ja kes on seetõttu vastuvõtlikumad P. aeruginosa nakkusele. Lisaks võimaldab tsüstilise fibroosi korral hingamisteedes esinev suurem limakogus bakterite kiiret kasvu.[7][11][12] Halva kvaliteediga ja Pseudomonas aeruginosa rakke sisaldav vesi võib pikaajalise kasutamise korral põhjustada dermatiiti.
Toksiinid
[muuda | muuda lähteteksti]P. aeruginosa virulentsusfaktor eksotoksiin A ADP-ribosüleerib peremeesrakus eukarüootset elongatsioonifaktorit 2 (nukleotiidi või valgu sünteesimise initsiatsiooni ja terminatsiooni vaheline etapp). Elongatsioonifaktori 2 puudumisel on takistatud raku valgusüntees ja rakk hukkub. Rakusisu vabanemine tekitab organismis immuunvastuse. Lisaks kasutab P. aeruginosa ka eksoensüümi ExoU, mis lagundab plasmamembraani ja põhjustab peremeesrakkude lüüsumist.
Diagnoosimine
[muuda | muuda lähteteksti]Diagnoosimine sõltub infektsiooni tüübist. Kogutakse sobiv proov, mida analüüsitakse laboratoorselt. Esmalt viiakse läbi Grami järgi värvimine. P. aeruginosa esinemise korral on nähtavad gramnegatiivsed kepikesekujulised bakterid ja valged verelibled. P. aeruginosa kolooniad on iseloomuliku viinamarjalõhnaga. Segakultuuridest isoleeritakse MacConkey agaril puhtad kolooniad. Puhaste kolooniate eraldamiseks kasutatakse oksüdaasitesti. Kuna P. aeruginosa ei ole võimeline kääritama laktoosi, on ta oksüdaaspositiivne. Kontrolltestis määratakse veel võimet kasvada 42 °C juures ja iseloomuliku roheka värvuse (püotsüaniini) olemasolu.[13]
Ravi
[muuda | muuda lähteteksti]
Üksikud kolooniad ei põhjusta tervete kudede nakatumist. Oportunisliku patogeenina nakatab P. aeruginosa vaid nõrgenenud immuunsusega organisme, kehapiirkondi ja elundeid. Ta kuulub normaalsesse naha mikrofloorasse ja ravi ei ole alati vajalik. Juba väljakujunenud infektsioon vajab peaaegu alati ravi. P. aeruginosa on looduslikult resistentne paljudele antibiootikumidele ja võib ebaõnnestunud ravi korral muutuda veel resistentsemaks. Resistents kujuneb välja peamiselt poriinide modifitseerimise teel. Seetõttu on enne antibiootikumide manustamist vaja laboratoorselt kindlaks määrata infektsiooni tekitanud tüve tundlikkus erinevate antibiootikumide suhtes. Seni on kõige tõhusamaks ravimeetodiks osutunud faagiteraapia, mida võib ka antibiootikumidega kombineerida. Faagiteraapiale ei ole vastunäidustusi ja kõrvalnähte on minimaalselt. Faage toodetakse vedelikuna, mis sobib suukaudseks manustamiseks.[14] Esimesena kirjeldati faagiteraapia kasutamist P. aeruginosa põhjustatud kõrvapõletiku ravis 2009. aastal.[15]
Antibiootikumid, mida kasutatakse raviks, võivad sisaldada:
- aminoglükosiide (gentamütsiin, amikatsiin, tobramütsiin, kuid mitte kanamütsiin);
- kinoloone (tsiprofloksatsiin, levofloksatsiin, kuid mitte moksifloksatsiin);
- tsefalosporiine (tseftasidiim, tsefepiim, tsefoperasoon, tsefpiroom, tseftobiprool, kuid mitte tsefuroksiim, tseftriaksoon, tsefotaksiim);
- antipseudomonaalseid penitsilliine: karboksüpenitsilliinid (karbenitsilliin ja tikartsilliin) ja ureidopenitsilliinid (meslotsillin, aslotsillin ja piperatsilliin). P. aeruginosa on resistentne kõikidele teistele penitsilliinidele;
- karbapeneeme (meropeneem, imipeneem, doripeneem, kuid mitte ertapeneem);
- polümüksiine (polümüksiin B ja kolistiin);[16]
- monopaktamiide.
Antibiootikumi manustatakse otse vereringesse. Harvadel juhtudel, kui infektsioon on pinnapealne ja piiratud levikuga (nt kõrva- või küünepõletiku korral), kasutatakse ka välispidist gentamütsiini või kolistiini.
Antibiootikumiresistentsus ja biokile
[muuda | muuda lähteteksti]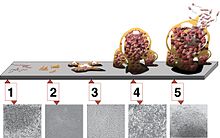
Ravi raskendab Pseudomonas aeruginosa'le iseloomulik vähene tundlikkus antibiootikumidele. Seda põhjustavad mitmed geenid (nt mexAB, mexXY jne) ja bakteri rakuümbrise väike läbilaskvus. Lisaks looduslikule resistentsusele on vastupanuvõime tingitud ka kromosomaalsete geenide mutatsioonidest ja horisontaalsest antibiootikumiresistentsust põhjustavate fragmentide ülekandest. Fenotüübiline resistentsus on tingitud biokile moodustumisest. Biokile on mikroorganismide agregeerumise vorm. Omavahel kokkukleepunud bakterid eritavad enda ümber eksopolüsahhariide ning on seetõttu kaitstud väliskeskkonna eest.
Patogeensus taimedes
[muuda | muuda lähteteksti]Kõrgematel taimedel, näiteks harilikul müürloogal ja spargelsalatil põhjustab P. aeruginosa pehmemädanikku.[17]
Viited
[muuda | muuda lähteteksti]- ↑ Stover, CK et al. (2000): Complete genome sequence of Pseudomonas aeruginosa PAO1, an opportunistic pathogen In: Nature Bd. 406(6799), S. 947-8 , PMID 10984043
- ↑ Ryan KJ, Ray CG (toimetajad) (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. ISBN 0-8385-8529-9.
- ↑ Özen, Asli I.; Ussery, David W. "Defining the Pseudomonas Genus: Where Do We Draw the Line with Azotobacter?". Microbial Ecology. 63 (2): 239–248.
- ↑ Todar's Online Textbook of Bacteriology. Textbookofbacteriology.net (2004-06-04). Retrieved on 2011-10-09.
- ↑ Todar, Kenneth. "Pseudomonas aeruginosa". Todar's Online Textbook of Bacteriology. Vaadatud 17.01.2022.
- ↑ King EO, Ward MK, Raney DE (1954). "Two simple media for the demonstration of pyocyanin and fluorescein". J Lab Clin Med. 44 (2): 301–7. PMID 13184240.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ 7,0 7,1 "Arhiivikoopia". Originaali arhiivikoopia seisuga 15. juuni 2015. Vaadatud 19. novembril 2012.
{{netiviide}}: CS1 hooldus: arhiivikoopia kasutusel pealkirjana (link) - ↑ Vander Wauven C, Piérard A, Kley-Raymann M, Haas D (1984). "Pseudomonas aeruginosa mutants affected in anaerobic growth on arginine: evidence for a four-gene cluster encoding the arginine deiminase pathway". J. Bacteriol. 160 (3): 928–34. PMC 215798. PMID 6438064.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Hagelueken, Gregor; Adams, Thorsten M.; Wiehlmann, Lutz; Widow, Ute; Kolmar, Harald; Tümmler, Burkhard; Heinz, Dirk W.; Schubert, Wolf-Dieter. "The crystal structure of SdsA1, an alkylsulfatase from Pseudomonas aeruginosa, defines a third class of sulfatases". Proceedings of the National Academy of Sciences of the United States of America. 103 (20): 7631–7636.
- ↑ Prithiviraj, B.; Bais, H. P.; Weir, T.; Suresh, B.; Najarro, E. H.; Dayakar, B. V.; Schweizer, H. P.; Vivanco, J. M. "Down regulation of virulence factors of Pseudomonas aeruginosa by salicylic acid attenuates its virulence on Arabidopsis thaliana and Caenorhabditis elegans". Infection and Immunity. 73 (9): 5319–5328. Originaali arhiivikoopia seisuga 18. jaanuar 2022. Vaadatud 17. jaanuaril 2022.
- ↑ Hassett DJ (1996). "Anaerobic production of alginate by Pseudomonas aeruginosa: alginate restricts diffusion of oxygen". J. Bacteriol. 178 (24): 7322–5. PMC 178651. PMID 8955420.
- ↑ Cooper, Megan; Tavankar, Gholam Reza; Williams, Huw D. "Regulation of expression of the cyanide-insensitive terminal oxidase in Pseudomonas aeruginosa". Microbiology (Reading). 149 (5): 1275–1284.
- ↑ Brett, M. M.; Ghoneim, A. T.; Littlewood, J. M. "Prediction and diagnosis of early Pseudomonas aeruginosa infection in cystic fibrosis: a follow-up study" (PDF). Journal of Clinical Microbiology. 26 (8): 1565–1570.
- ↑ Sulakvelidze, Alexander; Alavidze, Zemphira; Morris, Jr., J. Glenn. "Bacteriophage Therapy". Antimicrobial Agents and Chemotherapy. 45 (3): 649–659.
- ↑ Wright, A.; Hawkins, C. H.; Änggård, E. E.; Harper, D. R. "A controlled clinical trial of a therapeutic bacteriophage preparation in chronic otitis due to antibiotic-resistant Pseudomonas aeruginosa; a preliminary report of efficacy". Clinical Otolaryngology. 34 (4): 349–357.
- ↑ Hachem, Ray Y.; Chemaly, Roy F.; Ahmar, Corine A.; Jiang, Ying; Boktour, Maha R.; Rjaili, Georges Abou; Bodey, Gerald P.; Raad, Issam I. "Colistin is effective in treatment of infections caused by multidrug-resistant Pseudomonas aeruginosa in cancer patients". Antimicrobial Agents and Chemotherapy. 51 (6): 1905–1911.
- ↑ Walker, Travis S.; Bais, Harsh Pal; Déziel, Eric; Schweizer, Herbert P.; Rahme, Laurence G.; Fall, Ray; Vivanco, Jorge M. "Pseudomonas aeruginosa-Plant Root Interactions. Pathogenicity, Biofilm Formation, and Root Exudation". Plant Physiology. 134 (1): 320–331.
