Papilloomiviirused
See artikkel vajab toimetamist. |
See artikkel ootab keeletoimetamist. |
| Papilloomiviirused | |
|---|---|
 | |
| Taksonoomia | |
| Riik |
Viirused |
| Sugukond |
Papillomaviridae |
Papilloomiviirused (Papillomaviridae) on sugukond väikseid ümbriseta DNA-viirusi.
Klassifikatsioon[muuda | muuda lähteteksti]
- Baltimore'i klassifikatsioon: Klass 1.
Sugukonda Papillomaviridae liigitatakse järgmised viiruste perekonnad:
- Alphapapillomavirus
- Betapapillomavirus
- Gammapapillomavirus
- Deltapapillomavirus
- Epsilonpapillomavirus
- Etapapillomavirus
- Iotapapillomavirus
- Kappapapillomavirus
- Lambdapapillomavirus
- Mupapillomavirus
- Nupapillomavirus
- Omikronpapillomavirus
- Pipapillomavirus
- Thetapapillomavirus
- Xipapillomavirus
- Zetapapillomavirus.
Morfoloogia[muuda | muuda lähteteksti]
- Genoom: dsDNA tsirkulaarne, keskmiselt 8000 bp
- Kapsiid: ikosaeedriline
- Kest: puudub
- Replikatsioon: rakutuumas
Evolutsioon[muuda | muuda lähteteksti]
Võrreldes teiste viirustega on papilloomiviiruste evolutsioon olnud aeglane. Aeglane areng tuleneb sellest, et papilloomiviiruse genoomi, mis koosneb geneetiliselt stabiilsest kaheahelalisest DNA-st, sünteesitakse ainult peremeesraku DNA replikatsioonimehhanismi abil. Papilloomiviirused arenevad üldiselt koos oma peremeesorganismiga. HPV-16 arenes inimpopulatsioonide laienemisel üle maakera ning nüüd ta varieerub erinevates geograafilistes piirkondades.[1][2]
Teised HPV tüübid, nagu HPV-13, varieeruvad erinevates inimpopulatsioonides vähe. HPV-13 järjestus on sarnane bonobote papilloomiviiruste omaga.[3] Ei ole selge, kas sarnasuse põhjuseks on hiljutine liikidevaheline ülekandumine või asjaolu, et HPV-13 on alates inimese ja bonobote lahknemisest vähe muutunud.[2]
Struktuur[muuda | muuda lähteteksti]
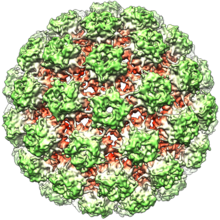
Papilloomiviirused on ümbriseta viirused, mis tähendab, et viiruse kapsiid ei ole kaetud lipiidse membraaniga. Peamine struktuurvalk on L1, mis on vajalik ja piisav 55–60 nm diameetriga kapsiidi moodustamiseks. Kapsiidi koostisse kuulub 72 tähekujulist kapsomeeri. Sarnaselt suurema osaga ümbriseta viirustest on papilloomiviiruse kapsiidi geomeetria korrapärane ja omab ikosaeedrilist sümmeetriat. In vitro L1 valgust kokku pandud viiruselaadsed partiklid on edukate profülaktiliste HPV vaktsiinide aluseks.
Papilloomiviiruse genoom on kaheahelaline tsirkulaarne DNA molekul. Pikkus on umbes 8000 aluspaari. DNA paikneb virionis koos rakuliste histoonidega, mis moodustab kromatiiniga sarnaneva kompleksi.
Papilloomiviiruse kapsiid sisaldab lisaks L1 valgule ka valku L2. Peale kapsiidi moodustamise täidab E2 ka selliseid funktsioone nagu genoomi pakkimise hõlbustamine virionidesse ja viiruse infektsioonilisele sisenemisele kaasaaitamine. L2 on HPV vaktsiinide üks võimalikke sihtmärke.
Koespetsiifilisus[muuda | muuda lähteteksti]
Papilloomiviirused replitseeruvad üksnes keratinotsüütides, mis paiknevad naha välimistes kihtides ja limaskestadel. Need epiteelkoed koosnevad lamestunud rakkude kihtidest. Kihid moodustuvad rakulise diferentseerumise tulemusena, milles keratinotsüüdid järk-järgult spetsialiseeruvad. Lõpuks moodustub tugev ja omavaheliste kontaktidega seostunud pind, mis takistab niiskuskadu ja on mehaaniliseks barjääriks patogeenidele. Vähediferentseerunud keratinotsüütide tüvirakud paiknevad basaalkihis ning nad täiendavad pidevalt pindmisi kihte. Kuna nad on ainsana epiteelirakkudest jagunemisvõimelised, siis on nad papilloomiviiruse infektsiooni sihtmärgiks. Edasised sammud viiruse elutsüklis on ranges sõltuvuses keratinotsüütide diferentseerumisest ning seetõttu saavad papilloomiviirused replitseeruda ainult keha pindmistes kudedes.
Genoomne organisatsioon[muuda | muuda lähteteksti]
Nende genoomi moodustab kaheahelaline tsirkulaarne DNA molekul, mille keskmine pikkus on 8000 aluspaari. Põhiliseks struktuurvalguks on L1, mille abil moodustatakse korrapärane ikosaeedrilise sümmeetriaga ja 55–60 nm diameetriga kapsiid.
Teatakse sadu papilloomiviiruste liike, millele viidatakse kui "tüüpidele". Need on väga peremehe- ja koespetsiifilised. Viirused nakatavad epiteelkoe rakke ning replitseeruvad rakutuumas. Seejuures võivad mõned viiruse tüübid vähki tekitada.
Siiani on koostatud rohkem kui saja inimese papilloomiviiruse tüübi genoomid ja PCR-andmete töötlemise tulemiks võib olla veel umbes 100 tüübi olemasolu tuvastamine.[4]
Tuntuim esindaja on inimese papilloomiviirus.
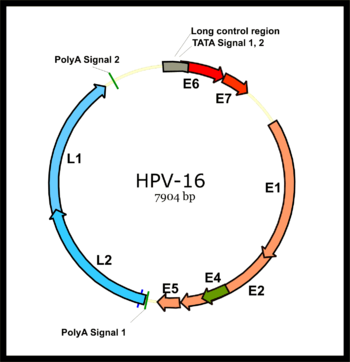
Papilloomiviiruse genoom on jagatud varajaseks regiooniks (early region, E) ja hiliseks regiooniks (late region, L). Varajase ja hilise kodeeriva ala vahele jääb mittekodeeriv regulatoorne ala (URR ehk upstream regulatory region, LCR ehk long control region). Varajane regioon kodeerib geene, mida ekspresseeritakse kohe pärast esmast raku infektsiooni ning hiline regioon kapsiidivalke L1 ja L2. Kõik geenid asuvad ühes DNA ahelas. See on suur erinevus papilloomiviiruste ja polüoomiviiruste vahel, kuna viimases ekspresseeritakse varajased ja hilised geenid bipolaarse transkriptsiooniga mõlemalt DNA ahelalt. See näitab, et papilloomiviirustel ja polüoomiviirustel pole olnud ühist eellast, kuigi nende struktuurides on märkimisväärsed sarnasused.
E1[muuda | muuda lähteteksti]
E1 on papilloomiviiruse peamine replikatsioonivalk. E1 avatud lugemisraam (open reading frame, ORF) kodeerib valku, mis seostub viraalsele replikatsioonioriginile ehk replikatsiooni alguspunktile LCR'is. E1 kasutab ATP energiat, et rakendada helikaasset aktiivsust DNA ahelate lahutamiseks. Nii valmistab ta viiruse genoomi ette DNA replikatsiooniks.
E2[muuda | muuda lähteteksti]
E2 valk täidab viraalsetes promootorites põhiliselt transkriptsioon regulaatori rolli. Valgul on transaktivatsiooni domeen ja DNA-d seondav domeen, mis on omavahel seotud hinge (hinge) domeeniga. Üksinda seondub E1 valk replikatsioonioriginile nõrgalt. E2 aitab kaasa E1 tugevamale seondumisele. E2 valk seondab viiruse genoomi ka raku mitootilistele kromosoomidele ja see on oluline viiruse genoomi segregatsioonil ehk jaotumisel tütarrakkude vahel.[5] Arvatakse, et onkogeenide E6 ja E7 ekspresseerumisel käitub E2 negatiivse regulaatorina. Geneetilised muutused, nagu viiruse DNA integratsioon peremeesraku kromosoomi, inaktiveerivad E2 ekspressiooni ja suureneb onkogeenide E6 ja E7 ekspressioon. Tulemuseks on rakusisesed muutused.
E3[muuda | muuda lähteteksti]
Väikest oletuslikku geeni E3 leidub ainult vähestes papilloomiviiruse tüüpides. Siiani ei ole õnnestunud tuvastada selle geeni ekspresseeritavat valku ja tal ei tundu olevat funktsioone.
E4[muuda | muuda lähteteksti]
E4 valke ekspresseeritakse varajases infektsioonifaasis madalal tasemel, kuigi ta kuulub varajaste geenite hulka. Hilises infektsioonifaasis võib ekspressioon järsult suureneda. HPV-1 tekitatud tüüka puhul moodustab E4 ligi 30% tüüka pinnavalgust.[6] Arvatakse, et mitmetes papilloomiviiruse tüüpides vahendab E4 virionide vabanemist keskkonda, selleks katkestab ta keratinotsüütide tsütoskeleti filamentide vahelised sidemed. E4 mutantidel ei toimub kõrgel tasemel DNA replikatsiooni, kuid ei ole selge, kuidas E4 replikatsioonis osaleb. Samuti on näidatud, et E4 osaleb rakutsükli peatamises G2 faasis.
E5[muuda | muuda lähteteksti]
E5 valgud on väga väikesed ja hüdrofoobsed, mis destabiliseerivad suurt hulka nakatunud raku membraanivalkude funktsioone.[7] Mõnedes papilloomiviiruse tüüpides (enamjaolt BPV-1) toimib E5 onkogeenina. Sellisel juhul ta aktiveerib rakkude kasvu soodustavaid signaale. Inimese papilloomiviirustes on E5 seotud vähitekkega. HPV-16 ja HPV-2 on näidatud, et E5 surub maha peamise koesobivuskompleksi (major histocompatibility complex, MHC), mis hoiab ära nakatunud rakkude elimineerimise tsütotoksiliste T-rakkude poolt.
E6[muuda | muuda lähteteksti]
Valgul E6 on rakus palju erinevaid rolle ja ta omab vastastikmõju paljude teiste valkudega. Peamiseks rolliks on tuumor-supressorvalgu p53 lagundamine. p53 peamine funktsioon on rakutsükli peatamine DNA kahjustuse korral ja raku suunamine apoptoosi, kui kahjustuse ulatus on parandamiseks liiga suur. p53 lagundamine vähendab raku suutlikkust vastata DNA kahjustustele.[8][9] E6 sihtmärgiks on mitmed rakulised valgud ning ta suudab muuta metabolismiradasid. Üheks selliseks valguks on NFX1-91, mis surub maha telomeraasi tootmist. Telomeraas lubab rakkudel jaguneda piiramata arv kordi. Kui NFX1-91 lagundatakse E6 poolt, siis telomeraasi hulk suureneb ja üks peamisi raku kasvu kontrollivaid mehhanisme inaktiveeritakse.[10]
HPV põhjustatud vähkides on E6 ekspressioon vajalik pahaloomulise fenotüübi säilitamiseks. Seetõttu on E6 ka inimese papilloomiviiruste vaktsiinide sihtmärk.
E7[muuda | muuda lähteteksti]
Enamikus papilloomiviirusetüüpides on E7 funktsiooniks tuumor-supressorvalgu pRb mahasurumine. Samuti indutseerib ta DNA sünteesi latentses faasis. Koos valguga E6 hoiab E7 ära raku surma e apoptoosi ning soodustab rakutsükli kulgemist. E7 osaleb telomeraasi aktiveerimises. E6 ja E7 on tähtsad uurimisobjektid ja usutakse, et neil on nakatunud rakkudes palju teisi olulisi efekte. E6 ja E7 on vajalikud vähirakuliinide elushoidmiseks (nt HeLa).[11]
E8[muuda | muuda lähteteksti]
Vähesed papilloomiviiruse tüübid kodeerivad E8 geenist lühikest valku. Näiteks mõnedel veise papilloomiviirustel on E8 geenid funktsionaalselt sarnased HPV E5 geenidega.[12]
L1[muuda | muuda lähteteksti]
L1 on peamine kapsiidivalk ja temast piisab viiruslaadsete partiklite moodustamiseks. L1 valgust in vitro kokku pandud kapsiidid on mitmete HPV-vastaste vaktsiinide aluseks.
L2[muuda | muuda lähteteksti]
L2 on samuti kapsiidivalk, mida leidub papilloomiviiruse virionis oksüdeeritud kujul. L2 osaleb koos valguga L1 viiruse DNA pakkimisel virioni, kuid L2 osaleb ka viiruse sisenemisel rakku.[13] Pärast sisenemist satub virion endosoomi, kus happelised tingimused viivad L2 valgu põhjustatud destabiliseerivate funktsioonideni. Vabanedes endosoomist, liigub viiruse genoom rakutuuma. Kuna L2 on oluline nakatumiseks, on ta huviobjektiks vaktsiinide väljatöötajatele.[14]
Elutsükkel[muuda | muuda lähteteksti]
Infektsiooniline sisenemine[muuda | muuda lähteteksti]
Papilloomiviiruse produktiivne infektsioon algab epiteelkoe basaalse rakukihi nakatamisest. Viirus pääseb keratinotsüütidele ligi väikeste haavade kaudu nahas või limaskestas. Esmast viiruse kinnitumist raku pinnale vahendavad kapsiidivalgu L1 ja sulfateeritud suhkrute interaktsioonid.[15][16] Viirus on seejärel võimeline sisenema rakku, spetsiifilisele retseptorile seondudes. Raku pinnal asuvaks retseptoriks on tõenäoliselt alfa-6 beeta-4 integriin.[17][18] Viiruse antiretseptoriks on kapsiidivalk L1. Seostunud viirus transporditakse endosoomidesse.[19][20] Kapsiidivalk L2 katkestab endosoomi membraani, mis lubab viiruse genoomil väljuda. Genoom transporditakse koos L2 valguga rakutuuma.[21][22]
Viiruse säilimine rakus[muuda | muuda lähteteksti]
Pärast edukat keratinotsüütide nakatumist hakkab viirus ekspresseerima valke E1 ja E2. Need valgud on vajalikud replitseerumiseks ja viiruse säilitamiseks tsirkulaarse episoomina. Viiruse genoomi koopiaarv on episoomina säilides väike. Viiruslikud onkogeenid E6 ja E7 inaktiveerivad tuumor-supressorgeenid p53 ja pRb, millega stimuleeritakse raku kasvu. Papilloomiviiruse genoomid võivad säilida keratinotsüütide tüvirakkudes episoomina aastakümneid.[23]
Uute virionide moodustamine[muuda | muuda lähteteksti]
Hiliste geenide L1 ja L2 ekspressioon toimub ainult naha või limaskesta välimise kihi keratinotsüütides. L1 ja L2 suurenenud ekspressioon on seotud viiruse genoomi koopianumbri hüppelise kasvuga. Kuna välimiste kihtide rakud on suhteliselt väikse immuunsüsteemirakkude järelevalve all, siis arvatakse, et hiliste geenide ekspressioon on seotud immuunsüsteemist kõrvalehoidmisega.
Uued nakatumisvõimelised viirused pannakse kokku rakutuumas. Papilloomiviirustel on arenenud mehhanism, kuidas vabastada virione keskkonda. Teised ümbriseta imetajate viirused kasutavad lüütilisi protsesse peremeesraku tapmiseks, mis võimaldavad viiruspartiklite vabanemist. Sageli kaasneb selle protsessiga põletik, mis omakorda võib päästa valla immuunsüsteemi rünnaku viiruse vastu. Papilloomiviirused kasutavad ära aga epiteeli pindmise kihi rakkude irdumist kui mittepõletikulist viiruspartiklite vabastamismehhanismi.
Patoloogia[muuda | muuda lähteteksti]
Papilloomiviirused tehti kindlaks 20. sajandil, kui leiti, et papilloomid või tüükad võivad kanduda ühelt indiviidilt teisele.
- 1935. aastal näitas Francis Peyton Rous, kes eelnevalt demonstreeris vähkipõhjustavate sarkoomiviiruste olemasolu, et papilloomiviirused võivad põhjustada nakatunud küülikutes nahavähki. See oli esimene näide, et imetajates võib viirus põhjustada vähki.[24]
- Richard Shope uuris samuti papilloomiviirust (cottontail rabbit papillomavirus, CRPV) ja avastas esimese DNA onkoviiruse.[25]
Papilloomiviirused nakatavad linde ja imetajaid,[26] aga ka väikest hulka roomajaid (kilpkonni).[27][28]
Enamiku papilloomiviiruste infektsioon on kas asümptomaatiline (näiteks tüüp 6, tüüp 11) või põhjustab väikseid healoomulisi kasvajaid, mis on tuntud kui papilloomid või tüükad (inglise warts).
Papilloomiviirused on peremehe- ja koespetsiifilised ning seega kanduvad liigilt liigile üle väga harva.[29] Papilloomiviirused replitseeruvad ainult keha epiteelkudede basaalkihis. Kõik tuntud papilloomiviirused nakatavad kindlat epiteeli,[26] tüüpiliselt nahaepiteeli või genitaalide, suu või hingamisteede limaskesta.[23] Limaskesta nakatavate inimese papilloomiviiruste (HPV) tüübid jagunevad kõrgesse ja madalasse riskirühma vastavalt sellele, kas nad on seotud vähitekkega või mitte. Kõrge riskiga on näiteks inimese papilloomiviiruse tüübid 16, 18, 31 ja 45 ning nende põhjustatud genitaalpiirkonna nakkused võivad edasi areneda pahaloomulisteks kasvajateks. Madala riski tüübid on näiteks HPV-6 ja −11, mis kahekesi vastutavad ligi 90% kõigi genitaalpiirkonna healoomuliste papilloomide tekke eest, kuid nende arenemist vähiks pole kirjeldatud.
Papilloomiviiruste tüübid on kõrgelt kohanenud replitseeruma ainult üksikutes loomaliikides. Sooküüliku papilloomiviirus (cottontail rabbit papillomavirus, CRPV) võib oma Põhja-Ameerika peremehes (sooküülikutel – perekond Sylvilagus) põhjustada kühmuna esileulatuvaid tüükaid.[25] Euroopa kodujänestele (perekond Oryctolagus) saab CRPV kanduda üle ainult laboratoorsetes tingimustes. Euroopa kodujänesed ei suuda toota nakatavaid viiruspartikleid, seega peetakse neid CRPV jaoks juhuslikeks või tupikperemeesteks.[30]
Liikidevahelist ülekandumist on näidatud ka veise papilloomiviiruse (BPV) tüübil 1.[31] Veistel põhjustab BPV-1 suuri kiulisi nahatüükaid. BPV nakatab ka hobuseid, kes on viirusele juhuslikud peremehed. Nakatumine võib viia healoomuliste kasvajate tekkeni.
Papilloomiviiruse juhte on olnud ka väiksematel närilistel, nagu Süüria hamster ja Euraasia põlluhiir.[32] Ometi ei ole leitud papilloomiviirust, mis suudaks nakatada laborihiiri ja seetõttu puudub laboratoorseteks uuringuteks hea uurimismudel.
Kuigi mõned papilloomiviiruse tüübid põhjustavad vähki, ei ole vähk infektsiooni tüüpiline tulemus. Tavaliselt toimub papilloomiviiruste indutseeritud vähkide areng mitme aasta jooksul.
Viited[muuda | muuda lähteteksti]
- ↑ Ho L, Chan SY, Burk RD; et al. (1993). "The genetic drift of human papillomavirus type 16 is a means of reconstructing prehistoric viral spread and the movement of ancient human populations". J. Virol. 67 (11): 6413–23. PMC 238076. PMID 8411343.
{{cite journal}}: et al.-i üleliigne kasutus kohas:|author=(juhend)CS1 hooldus: mitu nime: autorite loend (link) - ↑ 2,0 2,1 Calleja-Macias IE, Villa LL, Prado JC; et al. (2005). "Worldwide genomic diversity of the high-risk human papillomavirus types 31, 35, 52, and 58, four close relatives of human papillomavirus type 16". J. Virol. 79 (21): 13630–40. DOI:10.1128/JVI.79.21.13630-13640.2005. PMC 1262609. PMID 16227283.
{{cite journal}}: et al.-i üleliigne kasutus kohas:|author=(juhend)CS1 hooldus: mitu nime: autorite loend (link) - ↑ Van Ranst M, Fuse A, Fiten P; et al. (1992). "Human papillomavirus type 13 and pygmy chimpanzee papillomavirus type 1: comparison of the genome organizations". Virology. 190 (2): 587–96. DOI:10.1016/0042-6822(92)90896-W. PMID 1325697.
{{cite journal}}: et al.-i üleliigne kasutus kohas:|author=(juhend)CS1 hooldus: mitu nime: autorite loend (link) - ↑ Blossom Damania, James M. Pipas, "DNA Tumor Viruses", Springer Science Business Media, lk 127, 2009, Google'i raamatu veebiversioon (vaadatud 04.08.2013)(inglise keeles)
- ↑ McBride AA, McPhillips MG, Oliveira JG (2004). "Brd4: tethering, segregation and beyond". Trends Microbiol. 12 (12): 527–9. DOI:10.1016/j.tim.2004.10.002. PMID 15539109.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Doorbar J, Campbell D, Grand RJ, Gallimore PH (1986). "Identification of the human papilloma virus-1a E4 gene products". EMBO J. 5 (2): 355–62. PMC 1166739. PMID 3011404.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Bravo IG, Alonso A (2004). "Mucosal human papillomaviruses encode four different E5 proteins whose chemistry and phylogeny correlate with malignant or benign growth". J. Virol. 78 (24): 13613–26. DOI:10.1128/JVI.78.24.13613-13626.2004. PMC 533923. PMID 15564472.
- ↑ "iHOP information Hyperlinked over Proteins UBE3A". Originaali arhiivikoopia seisuga 27.09.2007. Vaadatud 1.05.2007.
- ↑ "Biochemistry, Nottingham University – 3.0 Enzymes of the Ubiquitin Pathway". Originaali arhiivikoopia seisuga 6.05.2007. Vaadatud 1.05.2007.
- ↑ Kelley ML, Keiger KE, Lee CJ, Huibregtse JM (2005). "The global transcriptional effects of the human papillomavirus E6 protein in cervical carcinoma cell lines are mediated by the E6AP ubiquitin ligase". J. Virol. 79 (6): 3737–47. DOI:10.1128/JVI.79.6.3737-3747.2005. PMC 1075713. PMID 15731267. Originaali arhiivikoopia seisuga 7. august 2011. Vaadatud 5. novembril 2011.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Nishimura A, Nakahara T, Ueno T; et al. (2006). "Requirement of E7 oncoprotein for viability of HeLa cells". Microbes Infect. 8 (4): 984–93. DOI:10.1016/j.micinf.2005.10.015. PMID 16500131.
{{cite journal}}: et al.-i üleliigne kasutus kohas:|author=(juhend)CS1 hooldus: mitu nime: autorite loend (link) - ↑ Jackson ME, Pennie WD, McCaffery RE, Smith KT, Grindlay GJ, Campo MS (1991). "The B subgroup bovine papillomaviruses lack an identifiable E6 open reading frame". Mol. Carcinog. 4 (5): 382–7. DOI:10.1002/mc.2940040510. PMID 1654923.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Richards RM, Lowy DR, Schiller JT, Day PM (2006). "Cleavage of the papillomavirus minor capsid protein, L2, at a furin consensus site is necessary for infection". Proc. Natl. Acad. Sci. U.S.A. 103 (5): 1522–7. DOI:10.1073/pnas.0508815103. PMC 1360554. PMID 16432208.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Pastrana DV, Gambhira R, Buck CB; et al. (2005). "Cross-neutralization of cutaneous and mucosal Papillomavirus types with anti-sera to the amino terminus of L2". Virology. 337 (2): 365–72. DOI:10.1016/j.virol.2005.04.011. PMID 15885736.
{{cite journal}}: et al.-i üleliigne kasutus kohas:|author=(juhend)CS1 hooldus: mitu nime: autorite loend (link) - ↑ Joyce JG, Tung JS, Przysiecki CT; et al. (1999). "The L1 major capsid protein of human papillomavirus type 11 recombinant virus-like particles interacts with heparin and cell-surface glycosaminoglycans on human keratinocytes". J. Biol. Chem. 274 (9): 5810–22. DOI:10.1074/jbc.274.9.5810. PMID 10026203.
{{cite journal}}: et al.-i üleliigne kasutus kohas:|author=(juhend)CS1 hooldus: mitu nime: autorite loend (link) - ↑ Giroglou T, Florin L, Schäfer F, Streeck RE, Sapp M (2001). "Human papillomavirus infection requires cell surface heparan sulfate". J. Virol. 75 (3): 1565–70. DOI:10.1128/JVI.75.3.1565-1570.2001. PMC 114064. PMID 11152531.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Evander M, Frazer IH, Payne E, Qi YM, Hengst K, McMillan NA (1997). "Identification of the alpha6 integrin as a candidate receptor for papillomaviruses". J. Virol. 71 (3): 2449–56. PMC 191355. PMID 9032382.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ McMillan NA, Payne E, Frazer IH, Evander M (1999). "Expression of the alpha6 integrin confers papillomavirus binding upon receptor-negative B-cells". Virology. 261 (2): 271–9. DOI:10.1006/viro.1999.9825. PMID 10497112.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Selinka HC, Giroglou T, Sapp M (2002). "Analysis of the infectious entry pathway of human papillomavirus type 33 pseudovirions". Virology. 299 (2): 279–287. DOI:10.1006/viro.2001.1493. PMID 12202231.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Day PM, Lowy DR, Schiller JT (2003). "Papillomaviruses infect cells via a clathrin-dependent pathway". Virology. 307 (1): 1–11. DOI:10.1016/S0042-6822(02)00143-5. PMID 12667809.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Kämper N, Day PM, Nowak T; et al. (2006). "A membrane-destabilizing peptide in capsid protein L2 is required for egress of papillomavirus genomes from endosomes". J. Virol. 80 (2): 759–68. DOI:10.1128/JVI.80.2.759-768.2006. PMC 1346844. PMID 16378978.
{{cite journal}}: et al.-i üleliigne kasutus kohas:|author=(juhend)CS1 hooldus: mitu nime: autorite loend (link) - ↑ Day PM, Baker CC, Lowy DR, Schiller JT (2004). "Establishment of papillomavirus infection is enhanced by promyelocytic leukemia protein (PML) expression". Proc. Natl. Acad. Sci. U.S.A. 101 (39): 14252–7. DOI:10.1073/pnas.0404229101. PMC 521143. PMID 15383670.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ 23,0 23,1 Doorbar J (2005). "The papillomavirus life cycle". J. Clin. Virol. 32 Suppl 1: S7–15. DOI:10.1016/j.jcv.2004.12.006. PMID 15753007.
- ↑ Campo MS. Animal models of papillomavirus pathogenesis.Virus Res. 2002 Nov;89(2):249-61. Osaline veebiversioon (vaadatud 04.08.2013)
- ↑ 25,0 25,1 [1][alaline kõdulink]
- ↑ 26,0 26,1 de Villiers EM, Fauquet C, Broker TR, Bernard HU, zur Hausen H. (2004). "Classification of papillomaviruses". Virology. 324 (1): 17–27. DOI:10.1016/j.virol.2004.03.033. PMID 15183049.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Herbst LH, Lenz J, Van Doorslaer K, Chen Z, Stacy BA, Wellehan JF Jr, Manire CA, Burk RD (2009). "Genomic characterization of two novel reptilian papillomaviruses, Chelonia mydas papillomavirus 1 and Caretta caretta papillomavirus 1". Virology. 383 (1): 131–5. DOI:10.1016/j.virol.2008.09.022. PMID 18973915.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Drury SE, Gough RE, McArthur S, Jessop M (1998). "Detection of herpesvirus-like and papillomavirus-like particles associated with diseases of tortoises". Vet Rec. 143 (23): 639. PMID 9881444.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Mistry N, Wibom C, Evander M (2008). "Cutaneous and mucosal human papillomaviruses differ in net surface charge, potential impact on tropism". Virol J. 5: 118. DOI:10.1186/1743-422X-5-118. PMC 2571092. PMID 18854037.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Christensen ND (2005). "Cottontail rabbit papillomavirus (CRPV) model system to test antiviral and immunotherapeutic strategies". Antivir. Chem. Chemother. 16 (6): 355–62. PMID 16331841.
- ↑ Coggins LW, Ma JQ, Slater AA, Campo MS (1985). "Sequence homologies between bovine papillomavirus genomes mapped by a novel low-stringency heteroduplex method". Virology. 143 (2): 603–11. DOI:10.1016/0042-6822(85)90398-8. PMID 2998027.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Van Ranst M, Tachezy R, Pruss J, Burk RD (1992). "Primary structure of the E6 protein of Micromys minutus papillomavirus and Mastomys natalensis papillomavirus". Nucleic Acids Res. 20 (11): 2889. DOI:10.1093/nar/20.11.2889. PMC 336941. PMID 1319576.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link)
Välislingid[muuda | muuda lähteteksti]
| Pildid, videod ja helifailid Commonsis: Papilloomiviirused |
- Viralzone: Papillomaviridae
- Los Alamos National Laboratory maintains a comprehensive (albeit somewhat dated) papillomavirus sequence database. This useful database provides detailed descriptions and references for various papillomavirus types.
- A short video which shows the effects of papillomavirus on the skin of an Indonesian man with epidermodysplasia verruciformis, the genetic inability to defend against some types of cutaneous HPV.
- [2] de Villiers, E.M., Bernard, H.U., Broker, T., Delius, H. and zur Hausen, H. Index of Viruses – Papillomaviridae (2006). In: ICTVdB – The Universal Virus Database, version 4. Büchen-Osmond, C (Ed), Columbia University, New York, USA.
- 00.099. Papillomaviridae description In: ICTVdB – The Universal Virus Database, version 4. Büchen-Osmond, C. (Ed), Columbia University, New York, USA
