Helikaasid
See artikkel ootab keeletoimetamist. (Juuni 2021) |
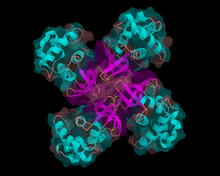
Helikaasid on kõigile elusorganismidele iseloomulikud elutähtsad ensüümid. Nad on motoorvalgud, mis liiguvad kindlasuunaliselt mööda nukleiinhappe suhkur-fosfaat selgroogu. Liikumise ajal eraldavad nad kokkupõimunud nukleiinhapete ahelaid. Sellisteks ahelateks võivad olla näiteks: DNA-DNA, RNA-RNA või DNA-RNA hübriid. Nimetatud protsessi läbiviimiseks saadakse energiat ATP hüdrolüüsist.
Funktsioon
[muuda | muuda lähteteksti]Nukleiinhapete ahelate eraldamist esineb mitmetes rakulistes protsessides (DNA replikatsioon, transkriptsioon, translatsioon, geneetiline rekombinatsioon, DNA reparatsioon, ribosoomide biogenees). Sageli kasutatakse helikaase DNA topeltheeliksi ehk biheeliksi või iseendaga seostunud RNA molekulide eraldamiseks. Selline lahutamisprotsess saab toimuda adenosiintrifosfaadi (ATP) hüdrolüüsil vabaneva energia kasutamise tulemusel. Ahelate eraldamine üksteisest toimub seetõttu, et lõhutakse vesinikside omavahel seostunud aluspaaride vahel. Helikaasid liiguvad astmeliselt, vastavalt konkreetsele ensüümile omase suuna ja kiirusega, piki üht biheeliksis olevat ahelat. Organismides esineb paljusid helikaase (näiteks on E. coli K12-s leitud 23 helikaasi[1]). Nad osalevad suures hulgas protsessides, kus eelduseks on ahelate üksteisest eraldamise katalüüsimine. Helikaasidel on mitmeid struktuure ja oligomerisatsiooni olekuid. Samas kui DnaB-sarnased helikaasid kerivad DNAd lahti sõõrikukujulisteks heksameerideks, on näidatud, et teised ensüümid on aktiivsed monomeeridena või valgudimeeridena. Uurimustega on kinnitatud, et helikaasid võivad käituda passiivselt ja oodata, kuni toimub katalüüsimata ahelate lahtikeerdumine, ning seejärel liiguvad nad lahutatud ahelate vahele.[2] Teise võimalusena on kirjeldatud aktiivset rolli, ahelate eraldamist katalüüsides. Selleks kasutatakse ATP hüdrolüüsist vabanevast energiat.[3] Viimasel juhul võib helikaasi võrrelda töötava mootoriga. Ta liigub ahelaid lahti keerutades mööda substraati. See on ATPaasi aktiivse töö otsene tulemus.[4] Helikaasid võivad töötada in vivo palju kiiremini kui in vitro. See on võimalik tänu abivalkude olemasolule, mis aitavad läbi viia kahvelliiduse destabilisatsiooni.[4] Defektid helikaase kodeerivates geenides võivad põhjustavad haigusi. Näiteks defekt WRN geenis põhjustab Werneri sündroomi – geneetilist haigust, mida iseloomustab enneaegne vananemine.[5]
Struktuurilised tunnusjooned
[muuda | muuda lähteteksti]Helikaaside üldine funktsioon on ennustatav lähtudes sellest, et neis on olemas kindlal hulgal aminohapete järjestuste homoloogiat. Kõigis helikaasides esineb ühine valgujärjestuse motiivi, mis paikneb nende primaarstruktuuri sisemuses. Arvatakse, et just need järjestused on spetsiifiliselt kaasatud ATP seondumisega, ATP hüdrolüüsi ning translokatsiooniga nukleiinhappe substraadil. Muutuv osa aminohapete järjestuses on seotud iga helikaasi spetsiifiliste tunnusjoontega. Lähtudes praeguseks kindlaks määratud helikaaside motiividest, on võimalik omistada oletatavat helikaasi aktiivsust erinevatele valkudele. Siiski ei kinnita sellise motiivi olemasolu, et see valk on helikaas. Konserveerunud motiivide leidumine toetab evolutsioonilise homoloogia olemasolu ensüümide vahel. Tulenevalt helikaaside juuresolekust ja nende motiivi vormist on helikaasid jagatud superperekondadeks. Mõned nende perekondade liikmed määratakse organismide põhjal, millest nad on eraldatud. Samuti lähtutakse helikaaside jaotamisel perekondadeks nende funktsioonist.
Superperekonnad
[muuda | muuda lähteteksti]Helikaasid jaotatakse konserveerunud motiivide alusel järgmistesse superperekondadesse (SF): SF1, SF2, SF3, DnaB-sarnane perekond ja Rho-sarnane perekond. Kõik need valgud seonduvad ATPga ning selle tulemusena kannavad nad klassikalist Walkeri motiivi: Walker A (fosfaadiga-seondumise ling ehk P-ling) ja Walker B (Mg2+-seonduv aspartaamhape) motiivi.
- Superperekond I :
Sellesse perekonda kuulub ka osa RNA helikaase. Arvatakse, et nad on seotud kahe ahela lahtikeerdumisega viiruse RNA replikatsiooni tsüklis. Kõnealuse superperekonna esindajaid on leitud üheahelaliste RNA-viiruste 1. superperekonna positiivsetelt ahelatelt. Mutatsioonide analüüsi tulemusel on jõutud järeldusele, et nendel helikaasidel on mitmeid varieeruvaid ülesandeid viiruse RNA replikatsioonitsükli erinevatel etappidel.[6] UvrD (E. coli, DNA reparatsioonis), Rep (E. coli, DNA replikatsioonis), PcrA (Staphylococcus aureus, rekombinatsioonis), Dda (bakteriofaag T4, replikatsiooni initsiatsioonis), RecD (E. coli, rekombinatsioonilisel reparatsioonis), TraI (F-plasmiid, bakteriaalses konjugatsioonis).
- Superperekond II :
RecQ helikaas (E. coli, DNA reparatsioonis), eIF4A (pagaripärmi, RNA translatsioonis), WRN geen inimese, DNA reparatsioonis), NS3[7] (C-hepatiit, viiruste replikatsioonis). TRCF (Mfd) (E. coli, transkriptsiooni-reparatsioonilisel paardumisel).
- Superperekond III :
Superperekond III koosneb helikaasidest, mida kodeerivad peamiselt väikesed DNA-viirused ning mõningate suured tuumatsütoplasma DNA-viirused.[8][9] Väikeste viiruste replikatsioon on suures sõltuvuses peremeesraku replikatsioonisüsteemist. Superperekonna III helikaasid on väikestes viirustes seotud origin'i seondumise domeeniga. Ori (DNA replikatsiooni alguspunkt) piirkonda ära tundva domeeni seondumisel helikaasiga saab viirus vahele jätta peremeesrakul põhineva regulatsiooni raja ning initsieerida oma enda replikatsiooni. Valk seondub viiruse Ori piirkonnaga, mille tulemusel toimub selle lahtikeerdumine. Rakusisesed replikatsioonvalgud koondatakse seejärel Ori piirkonda ning tänu sellele saab toimuda viiruse DNA replikatsioon. LTag (inimahvi viirus 40-e, replikatsioonis), E1 (inimese papilloomiviiruse replikatsioonis), Rep (adeno-seoseliste viiruste replikatsioonis, viiruste integratsioonis, virioni pakkimises).
- DnaB-sarnane perekond : dnaB helikaas (E. coli replikatsioonis), gp41 (bakteriofaag T4 DNA replikatsioonis), T7gp4 (bakteriofaag T7, DNA replikatsioonis).
- Rho-sarnane perekond : Rho (E. coli, transkriptsiooni terminatsioonis).
Siinkohal tuleb meeles pidada, et need superperekonnad ei hõlma kõiki võimalikke helikaase. Näiteks XPB ja ERCC2 on helikaasid, mis ei ole klassifitseeritud ühessegi ülalnimetatud perekonda.
RNA helikaasid
[muuda | muuda lähteteksti]RNA helikaasid ja DNA helikaasid esinevad koos peaaegu kõigis superperekondades.[10]
Siiski mitte kõikidel RNA helikaasidel ei esine helikaasset aktiivsust, selles mõttes, nagu seda tõlgendatakse ensümaatilisest funktsioonist lähtuvalt. Näiteks Swi/Snf perekonna valgud. Kuigi need valgud kannavad tüüpilist helikaasi motiivi, hüdrolüüsivad ATPd aminohappeseoseliselt ja on ehitatud ümber helikaasi kesta, olenemata sellest ei ole suudetud leida mingisugust ahelaid eraldavat aktiivsust.[11]
Need RNA helikaasid, mis siiski omavad ahelaid lahti keeravat funktsiooni, on iseloomustatud kahe järgmise mehhanismi alusel: tüüpiline biheeliksi lahti keeramine ning kindla asukohaga ehk (saitspetsiifiline) ahelate eraldamine. Üldtuntud biheeliksite lahtikeerdumine on astmeliselt toimuv kindlasuunaline kaksikahelate eraldamine, nagu juba eelnevalt ülal kirjeldatud. Seda kasutatakse näiteks DNA lahtikeerdumiseks. Kusjuures kohtspetsiifiline ahelate eraldamine esineb protsessis, mille käigus helikaasi ensüüm võib olla ühinenud biheeliksi suvalise kohaga. Helikaasi seondumisele aitavad kaasa üheahelalised RNA ahela regioonid ning kogu helikaasi seondumise protsess toimub koos ATP seondumisega.[12] Kui helikaas ja ATP on seondunud, ilmneb saitspetsiifiline ahelate lahknemine. See nõuab küll ATP seondumist, kuid ei vaja ATP hüdrolüüsi protsessi tegelikku toimumist.[13] Väiksema arvu aluspaaride korral dissotsieerub biheeliks ilma edasise ensüümi abita. Sellist lahtihargnemise meetodit kasutavad DEAD-box helikaasid.[14]
Veel helikaase
[muuda | muuda lähteteksti]- Kromodomiin helikaas DNA seonduv valk: CHD1, CHD1L, CHD2, CHD3, CHD4, CHD5, CHD6, CHD7, CHD8, CHD9
- DEAD box/DEAD/DEAH box helikaas: DDX3X, DDX5, DDX6, DDX10, DDX11, DDX12, DDX58, DHX8, DHX9, DHX37, DHX40, DHX58
- ASCC3, BLM, BRIP1, DNA2, FBXO18, FBXO30, HELB, HELLS, HELQ, HELZ, HFM1, HLTF, IFIH1, NAV2, PIF1, RECQL, RTEL1, SHPRH, SMARCA4, SMARCAL1, WRN, WRNIP1
Viited
[muuda | muuda lähteteksti]- ↑ Ensembl (november 2016). "EnsemblBacteria andmebaas". Originaali arhiivikoopia seisuga 17. november 2016.
- ↑ Lionnet T, Spiering MM, Benkovic SJ, Bensimon D, Croquette V (2007). "Real-time observation of bacteriophage T4 gp41 helicase reveals an unwinding mechanism". PNAS. 104 (50): 19790–19795. DOI:10.1073/pnas.0709793104. PMC 2148377. PMID 18077411.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Johnson DS, Bai L, Smith BY, Patel SS, Wang MD (2007). "Single-molecule studies reveal dynamics of DNA unwinding by the ring-shaped t7 helicase". Cell. 129 (7): 1299–309. DOI:10.1016/j.cell.2007.04.038. PMC 2699903. PMID 17604719.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ 4,0 4,1 "Researchers solve mystery of how DNA strands separate". 03.07.2007. Vaadatud 05.07.2007.
- ↑ Junko Oshima, MD, PhD, George M Martin, MD, and Fuki M Hisama, MD. (ilmus: 2. detsember 2012; viimati üle vaadatud: 9. veebruar 2012). "Werner Syndrome". GeneReviews™.
{{netiviide}}: kontrolli kuupäeva väärtust:|Aeg=(juhend)CS1 hooldus: mitu nime: autorite loend (link) - ↑ Garcia JA, Kaariainen L, Gomez de cedron M, Ehsani N, Mikkola ML (1999). "RNA helicase activity of Semliki Forest virus replicase protein NSP2". FEBS Lett. 448 (1): 19–22. DOI:10.1016/S0014-5793(99)00321-X. PMID 10217401.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Dumont S, Cheng W, Serebrov V, Beran RK, Tinoco Jr I, Pylr AM, Bustamante C, "RNA Translocation and Unwinding Mechanism of HCV NS3 Helicase and its Coordination by ATP", Nature. 2006 Jan 5; 439: 105–108.
- ↑ Koonin EV, Aravind L, Iyer LM (2001). "Common origin of four diverse families of large eukaryotic DNA viruses". J. Virol. 75 (23): 11720–34. DOI:10.1128/JVI.75.23.11720-11734.2001. PMC 114758. PMID 11689653.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Koonin EV, Aravind L, Leipe DD, Iyer LM (2004). "Evolutionary history and higher order classification of AAA+ ATPases". J. Struct. Biol. 146 (1–2): 11–31. DOI:10.1016/j.jsb.2003.10.010. PMID 15037234.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ "RNA helicases" Edited by Eckhard Jankowsky, RSC Publishing 2010
- ↑ Jankowsky, E (2011). "RNA helicases at work: Binding and rearranging". Trends in Biochemical Sciences. 36 (1): 19–29. DOI:10.1016/j.tibs.2010.07.008. PMC 3017212. PMID 20813532.
- ↑ Yang, Quansheng; Del Campo, Mark; Lambowitz, Alan M.; Jankowsky, Eckhard (2007). "DEAD-Box Proteins Unwind Duplexes by Local Strand Separation". Molecular Cell. 28 (2): 253–63. DOI:10.1016/j.molcel.2007.08.016. PMID 17964264.
- ↑ Liu, F.; Putnam, A.; Jankowsky, E. (2008). "ATP hydrolysis is required for DEAD-box protein recycling but not for duplex unwinding". Proceedings of the National Academy of Sciences. 105 (51): 20209. DOI:10.1073/pnas.0811115106.
- ↑ Jarmoskaite, Inga; Russell, Rick (2011). "DEAD-box proteins as RNA helicases and chaperones". Wiley Interdisciplinary Reviews: RNA. 2: 135. DOI:10.1002/wrna.50.
