Märgumine

Märgumine on pinnanähtus, mille korral vedelik jääb molekulaarjõudude tõttu tahkise pinnaga ühendusse ehk valgub laiali. See tuleneb molekulidevahelisest interaktsioonist, kui vedelik ja pind kokku saavad. Märgumise ulatus sõltub adhesiooni- ja kohesioonijõu vastastikuseist suhteist.
Kui märgumine toimub näiteks vee ja klaasi vahel, siis mittemärgumine esineb näiteks elavhõbedakuulikese liikumisel mööda põrandat. Sel juhul ületab elavhõbedakuuli kohesioonijõud põranda ja kuulikese vahelise adhesioonijõu.
Märgumine on tähtis omadus, mis iseloomustab kahe materjali kleepuvust või nendevahelist sidet. Märgumine ja pinnajõud põhjustavad lisaks märgumisele teisigi nähtusi, sealhulgas kapillaarnähtusi. Hoolimata märgumise ulatusest, on vedelikutilga kuju tahkel pinnal umbes kera segmendi kujuga.
Seletus
[muuda | muuda lähteteksti]Adhesioonijõud, mis esinevad vedeliku ja tahkise vahel, põhjustavad vedelikutilga levimist üle pinna. Kohesioonijõud vedeliku sees põhjustavad vedelikutilga kerakujuliseks muutumist ja pinnaga kontakti hoidmist.
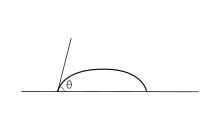
Märgumisnurk (nagu näha joonisel 1) on nurk, mille all vedeliku ja gaasi piirpind on kontaktis tahkise ja vedeliku piirpinnaga. Märgumisnurk on määratud adhesiooni ja kohesioonijõududega. Kui tilga kalduvus valguda laiali mööda tahket siledat pinda suureneb, väheneb märgumisnurk. Seega märgumisnurk on pöördvõrdeline märgavusega.[1]
Märgumisnurka, mis on väiksem kui 90°, nimetatakse väikeseks. See näitab tavaliselt, et pinna märgumine on soodustatud ja et vedelik voolab üle suure pinna laiali. Märgumisnurka, mis on suurem kui 90°, nimetatakse suureks. See näitab tavaliselt, et pinna märgumist ei toimu ja vedelik minimeerib kontakti pinnaga, moodustades kompaktseid vedelikutilgakesi.[2]
Käsitledes vett, võib märguvat pinda nimetada hüdrofiilseks ja mittemärguvat pinda hüdrofoobseks. Superhüdrofoobse pinna märgumisnurk on suurem kui 150°, mille tõttu on vedeliku ja pinna vahel peaaegu olematu kontakt. Seda nähtust kutsutakse lootose efektiks.[3] Vedelike jaoks, mis ei ole vesi, kasutatakse terminit lüofiilne väikese märgumisnurga jaoks ja lüofoobne suure märgumisnurga jaoks.

Pinnaenergia
[muuda | muuda lähteteksti]On kahte tüüpi pindasid, millega vedelikud saavad vastastikku toimida. Tahked pinnad on jaotatud kõrge ja madala energiaga pindadeks.
Tahkised, näiteks metallid, klaasid ja keraamika on tuntud kui "kõvad tahkised". Sidemetüübid, mis neid koos hoiavad (nt kovalentsed ja metallilised sidemed), on väga tugevad. Nende lõhkumiseks on vaja palju energiat, järelikult on nad kõrge energiaga. Enamik molekulaarseid vedelikke märgavad selliseid tahkiseid täielikult.
Teine tahkistetüüp on madala energiaga tahkised, mille molekulide vahel on nõrgad sidemed (nt Van der Waalsi jõud ja vesiniksidemed). Kuna need on väga nõrgad, kuluks nende lõhkumiseks väga vähe energiat, järelikult on nad madala energiaga tahkised. Olenevalt vedelikust võimaldavad madala energiaga pinnad kas täielikku või osalist märgamist.[4][5][6]
Laialivalgumistöö
[muuda | muuda lähteteksti]Laialivalgumistöö suurus määrab tilga kuju tahkise pinnal. Kui keha kattub vedelikukihiga, on laialivalgumistöö süsteemi energiamuut.
Kui vedelikutilk panna pinnale ja ta hakkab laiali valguma, siis tahkise- ja gaasifaasi vaheline pindala väheneb, tahkise- ja vedelikufaasi ning vedeliku- ja gaasifaasi vaheline pindala hakkab kasvama.
Kui vaadelda süsteemi tahkis-vedelik-gaas, siis vedelik valgub laiali, kui
- sTV + sVG – sTG < 0, kus
- sTV – tahkise ja vedeliku vaheline pindpinevus,
- sVG – vedeliku ja gaasi vaheline pindpinevus,
- sTG – tahkise ja gaasi vaheline pindpinevus.
- sTV + sVG – sTG < 0, kus
Antud võrrand kehtib ka vedeliku laialivalgumisel teisel vedelikul, juhul kui nad üksteises ei lahustu.[7]
Ideaalsed tahked pinnad
[muuda | muuda lähteteksti]Ideaalne tahke pind on lame, jäik, täielikult sile, keemiliselt homogeenne ega oma märgumisnurga hüstereesi. Lisaks võtab vedelikutilk pinnal oma esialgse kuju, kui teda häirida.[3][8] Järgnevad lähendused kehtivad vaid ideaalsete pindade korral.

Energia miinimumi printsiip, kolm faasi
[muuda | muuda lähteteksti]Vaatleme süsteemi, mis koosneb kolmest vedelikust. Joonis 3 kujutab joont, kus kolm faasi kokku puutuvad. Tasakaalulised olekus on kogujõud pikkusühiku kohta kolme faasi piirpinnal võrdne nulliga. Kogujõu komponendid igal piirpinnal on antud kui:
- γαθ + γθβ cos θ + γαβ cos α = 0
- γαθ cos θ + γθβ + γαβ cos β = 0
- γαθ cos α + γθβ cos β + γαβ = 0, kus
α, β ja θ on joonisel näidatud nurgad ja γij on pinnaenergia kahe faasi i ja j vahel. Neid suhteid saab kujutada ka kolmnurgana. See on tuntud kui Neumanni kolmnurk, mis on kujutatud joonisel 4. Neumanni kolmnurk allub kolmnurga omadusele α + β + θ = 2π ning siinuse ja koosinusega opereerimise reeglitele.[9]
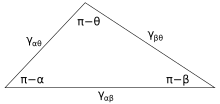
Kuna kolm pinnaenergiat moodustavad kolmnurga küljed, alluvad nad valemile γij < γjk + γik. See tähendab, et ükski pindpinevus ei tohi ületada teise kahe summat. Kui kolm vedelikku, mis ei allu nendele piirangutele, tuuakse kontakti, ei saa tekkida tasakaalu. Sel juhul tekib vedelikkude segunemine.
Youngi võrrand
[muuda | muuda lähteteksti]Kui faas nurgaga β vahetatakse sileda jäiga pinna vastu (näidatud joonisel 5), siis β = π ja teine jõud taandub Youngi võrrandiks[10]:
- γTG = γTV + γVG cos θ , kus
- γTG – pinnaenergia tahkise- ja gaasifaasi vahel,
- γTV – pinnaenergia tahkise- ja vedelikufaasi vahel,
- γVG – pinnaenergia vedeliku ja gaasifaasi vahel.[11]
- γTG = γTV + γVG cos θ , kus
See iseloomustab pindpinevust kolme faasi vahel: vedelik, tahkis ja gaas. See kehtib ka olukorras, kus gaasi asemel on teine vedelik, milles esimene, tilga kujul esinev vedelik, ei lahustu.

Reaalsed siledad pinnad ja Youngi märgumisnurk
[muuda | muuda lähteteksti]Youngi võrrand eeldab täielikult siledat ja jäika pinda. Paljudel juhtudel aga ei ole pinnad ligelähedaseltki ideaalsed. Probleemile saab läheneda kahel viisil: pind on kare (mitteideaalne kare jäik pind) või pind on sile, kuid siiski reaalne (lõplikult jäigad pinnad). Isegi täielikult siledal pinnal võib märgumisnurgal olla mitmesuguseid väärtusi alates maksimaalsest θA kuni minimaalse märgumisnurgani θR. Tasakaalulise märgumisnurga θC saab arvutada θA ja θR abil:
- ,
kus
Youngi-Dupré võrrand ja märgumiskoefitsient
[muuda | muuda lähteteksti]Youngi-Dupré võrrand ütleb, et ei γTG ega γTV või olla suuremad kui teise kahe pinnaenergia summa. Sellest võib järeldada, et täielik märgumine toimub, kui täidetud on tingimus γTG > γTV + γLG, ja märgumist ei toimu, kui täidetud on tingimus γTV > γTG + γVG. Kasulik parameeter märgumise uurimiseks on märgumisparameeter S, kus
- S = γTG – (γTV + γVG).
Kui S > 0, siis vedelik märgab pinna täielikult. Kui S < 0, siis toimub osaline märgamine. Kombineerides märgumisparameetri definitsiooni Youngi lähendusega, saab Youngi-Dupré võrrandi:
- S = γVG (cos θ – 1)
Selle järgi omab θ vaid siis füüsikalisi lahendeid, kui S < 0 .
Mitteideaalsed karedad pinnad
[muuda | muuda lähteteksti]Erinevalt ideaalsetest ei ole mitteideaalsed pinnad täiuslikult siledad, jäigad ega keemiliselt homogeensed. Sellised kõrvalekalded ideaalsusest tingivad nähtuse, mida kutsutakse märgumisnurga hüstereesiks. Märgumisnurga hüsterees on defineeritud maksimaalse ja minimaalse märgumisnurga vahena[13]:
- H = θA – θR.
Mitteideaalse pinna maksimaalne märgumisnurk on maksimaalne stabiilne märgumisnurk ja minimaalne märgumisnurk on minimaalne stabiilne märgumisnurk. Märgumisnurga hüsterees eksisteerib sellepärast, et on olemas mitu termodünaamiliselt stabiilset märgumisnurka. Need varieeruvad termodünaamiliselt stabiilsed märgumisnurgad on tuntud metastabiilsete olekutena.[8]
Levinud kõrvalekalduvus ideaalsusest on kare pind. Kare pind võib olla nii homogeene kui heterogeenne. Homogeense pinna korral täidab vedelik kareda pinna ebatasasused. Heterogeense pinna korral märgab vedelik mitut laadi karedusi. Sellistel pindadel on märgamisele mitmesugune mõju. Cassie-Baxteri ja Wenzeli mudel on kaks peamist mudelit, millega tekstuuriga pindade märgumist kirjeldatakse. Need kehtivad vaid siis, kui vedelikutilga suurus on palju suurem märjatava pinna kareduseastmest.[14]
Wenzeli mudel
[muuda | muuda lähteteksti]
Wenzeli mudel kirjeldab homogeenset märgamist ja seda on kujutatud joonisel 6. See mudel defineerib märgumisnurga karedal pinnal:[14]
- cos θ* = r cos θ,
kus θ* on nähtav märgumisnurk, mis on vastavuses stabiilse tasakaalulise olekuga, ehk süsteemi olek minimaalse vabaenergiaga. r on kareduse määr.[15]
θ on Youngi märgumisnurk, mis on defineeritud ideaalsel pinnal.
Cassie-Baxteri mudel
[muuda | muuda lähteteksti]
Heterogeense märgamise korral ei ole Wenzeli mudel enam piisav. Cassie-Baxteri võrrand on järgmine:[14]
- cos θ*= rf f cos θY + f – 1,
Kus r on karedus märgunud pinnal ja f on märjatud ala tahkel pinnal. On oluline tähele panna, et kui rf = r ja f = 1, muutub Cassie-Baxteri võrrand Wenzeli võrrandiks.
Pindaktiivsete ainete mõju pinna märgumisele
[muuda | muuda lähteteksti]Paljud tehnoloogilised protsessid nõuavad kontrolli vedeliku märgamise üle tahkel pinnal. Tilga asetamisel pinnale võib see pinna märjata täielikult, osaliselt või üldse mitte. Pindaktiivsete ainete abil saab vähendada pindpinevust ja muuta mittemärgava aine osaliselt või täielikult märgavaks.
Pindaktiivse aine segunedes vedelikuga tahkise- ja gaasifaasi piirpind suureneb ning tilga ääred muutuvad hüdrofiilseteks. Selle tulemusena tilk levib.[16]
Vaata ka
[muuda | muuda lähteteksti]Viited
[muuda | muuda lähteteksti]- ↑ Sharfrin, E.; Zisman, William A. (1960). "Constitutive relations in the wetting of low energy surfaces and the theory of the retraction method of preparing monolayers". The Journal of Physical Chemistry. 64 (5): 519–524. DOI:10.1021/j100834a002.
- ↑ U. Palm, V. Past (1974). Füüsikaline keemia. Tartu Riiklik Ülikool.
- ↑ 3,0 3,1 Eustathopoulos, N. (1999). Wettability at high temperatures. Oxford, UK: Pergamon. ISBN 0-08-042146-6.
{{cite book}}: eiran tundmatut parameetrit|coauthors=, kasuta parameetrit (|author=) (juhend) - ↑ Schrader, M.E (1992). Modern Approaches to Wettability. Theory and Applications. New York: Plenum Press. ISBN 0-306-43985-9.
{{cite book}}: eiran tundmatut parameetrit|coauthors=, kasuta parameetrit (|author=) (juhend) - ↑ de Gennes, P.G. (1985). "Wetting: statics and dynamics". Reviews of Modern Physics. 57 (3): 827–863. DOI:10.1103/RevModPhys.57.827.
- ↑ V. Loodmaa, Aksel Koorits (1971). Füüsikalise keemia ja kolloidkeemia alused. Tartu Riiklik Ülikool.
- ↑ Toomas Tenno, Aksel Koorits (1989). Pindnähtused ja adsorptsioon. Tartu Riiklik Ülikool.
- ↑ 8,0 8,1 Rulon E. Johnson, (1993) in Wettability Ed. Berg, John. C. New York, NY: Marcel Dekker, Inc. ISBN 0-8247-9046-4
- ↑ Rowlinson, J.S. (1982). Molecular Theory of Capillarity. Oxford, UK: Clarendon Press. ISBN 0-19-855642-X.
{{cite book}}: eiran tundmatut parameetrit|coauthors=, kasuta parameetrit (|author=) (juhend) - ↑ Young, T. (1805). "An Essay on the Cohesion of Fluids". Phil. Trans. R. Soc. Lond. 95: 65–87. DOI:10.1098/rstl.1805.0005.
- ↑ T. S. Chow (1998). "Wetting of rough surfaces". Journal of Physics: Condensed Matter. 10 (27): L445. DOI:10.1088/0953-8984/10/27/001.
- ↑ Tadmor, Rafael (2004). "Line energy and the relation between advancing, receding and Young contact angles". Langmuir. 20 (18): 7659. DOI:10.1021/la049410h. PMID 15323516.
{{cite journal}}:|pages=ja|page=dubleerivad üksteist (juhend) - ↑ Robert J. Good (1992). "Contact angle, wetting, and adhesion: a critical review". J. Adhesion Sci. Technol. 6 (12): 1269–1302. DOI:10.1163/156856192X00629.
- ↑ 14,0 14,1 14,2 Abraham Marmur (2003). "Wetting of Hydrophobic Rough Surfaces: To be heterogeneous or not to be". Langmuir. 19 (20): 8343–8348. DOI:10.1021/la0344682.
- ↑ Marmur, Abraham (1992) in Modern Approach to Wettability: Theory and Applications Schrader, Malcom E. and Loeb, Geroge New York: Plenum Press
- ↑ K.S. Lee; Ivanova, N; Starov, VM; Hilal, N; Dutschk, V (2008). "Kinetics of wetting and spreading by aqueous surfactant solutions". Advances in colloid and interface science. 144 (1–2): 54–65. DOI:10.1016/j.cis.2008.08.005. PMID 18834966.


