Immunohistokeemia
See artikkel vajab toimetamist. (August 2012) |
See artikkel ootab keeletoimetamist. |
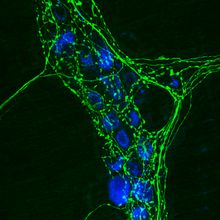
Immunohistokeemia (lühendina IHK) on antigeenide (nt valgud) tuvastamise protsess koelõikude rakkudes, kasutades antikehade spetsiifilist seondumist antigeenidele bioloogilises koes.[1]
Immunohistokeemia on nimetuse saanud tüvest "immuno", mis viitab protseduuris kasutatud antikehadele ja tüvest " histo", mis tähendab kude (võrreldes immunotsütokeemiaga).
Immunohistokeemilist värvimist on laialdaselt kasutatud vähkkasvajates leiduvate ebanormaalsete rakkude diagnoosiks. Spetsiifilised molekulaarsed markerid on iseloomulikud kindlatele rakus toimuvatele sündmustele nagu näiteks vohamine või raku tahtlik surm (apoptoos). IHK on laialdaselt kasutusel ka teadusuuringutes, aidates aru saada biomarkerite levikust ja lokalisatsioonist ning erinevalt ekspresseerunud valkudest bioloogiliste kudede eri osades. Antikeha – antigeeni vastastikku seondumise visualiseerimist võib saavutada mitmel viisil. Enamikul juhtudel on antikeha konjugeeritud ehk seondunud ensüümi nagu peroksüdaas külge, mis võib katalüüsida värvi tootvat reaktsiooni. Antikeha võib samuti seonduda fluorofooride (näiteks fluorestseiin, rodamiin) külge.
Proovi ettevalmistamine[muuda | muuda lähteteksti]
Visualiseerimisel on oluline sobivate antikehade kasutamine õigete antigeenide tuvastamiseks ja signaali võimendamiseks. Kriitilise tähtsusega on ka täielik proovi ettevalmistus koe morfoloogia säilitamiseks, koe ehituse ja sihtmärk epitoopide antigeensuse jaoks. See nõuab korralikke koekogumikke, fikseerimist ja sektsioneerimist. Tavaliselt kasutatakse fikseerimiseks paraformaldehüüdi. Sõltuvalt katse eesmärgist ja eksperimendiks vajaliku proovi paksusest lõigatakse huvipakkuvast koest viilud (4–40 µm). Võimalik on kasutada ka tervet kude, kuid vaid siis, kui kude ise pole väga paks ja on piisavalt aineid läbilaskev. Lõikamiseks kasutatakse tavaliselt mikrotoomi ja lõigud on kinnitatud alusklaasidele. Ujuvlõikude IHK kasutab lõike, mis ei ole kinnitatud. Need lõigud on tavaliselt vibreeriva mikrotoomiga valmistatud.
Fikseerimise ja koesäilitusmeetodi tõttu tuleks läbi viia täiendavaid etappe, mis teevad epitoobid antikeha sidumiseks kättesaadavaks. Nendeks on näiteks deparafiineerimine ja antigeeni tuvastamine (mikrolaine meetod, ensüümi meetod, inkubeerimise meetod). Need etapid on tihti erinevuseks värvumise (spetsiifilise seondumise) ja mittevärvumise (kõikjale seondumise) vahel. Sõltuvalt koe tüübist ja antigeeni tuvastamise meetodist, tuleb endogeensed biotiinid või ensüümid mõnikord enne antikeha värvimist vastavalt kas blokeerida või kustutada. Erinevalt immunotsütokeemiast ei ole vaja kude enam läbistada, sest see on saavutatud viilutamisel mikrotoomiga proovi ettevalmistamisel. Proovi ühtlasemaks katmiseks kasutatakse pindpinevuse vähendamist puhastusainete (nagu Triton X-100) abil. Antikehad näitavad enamasti soodustatud sidumist spetsiifilise epitoobiga. Ometi võiva nad osaliselt või nõrgalt seonduda mittespetsiifiliste valkudega alale (nimetatakse ka reaktiivisaitideks), mis sarnanevad spetsiifilise seostumispaiga märklaud-antigeeniga. Mittespetsiifilised seondumised põhjustavad kõrget taustvärvimist, mis võivad maskeerida sihtmärk-antigeeni tuvastamist. Taustvärvimise vähendamiseks IHK, ITK ja muude immunospetsiifiliste värvimiste puhul inkubeeritakse proovid puhvris. Puhver blokeerib reageerivad alad, kuhu primaarne või sekundaarne antikeha võib muidu seonduda. Blokeerimispuhvrid sisaldavad enamasti normaalset seerumit, BSA-d (veise (vere)seerumi albumiin) või želatiini. Suurema tõhususe saavutamiseks on saadaval patenteeritud koostisega kaubanduslikud blokeerimispuhvrid.
Proovi märgistamine[muuda | muuda lähteteksti]
Antikeha tüüp[muuda | muuda lähteteksti]
Spetsiifiliseks tuvastamiseks kasutatavad antikehad võivad olla kas polüklonaalsed või monoklonaalsed. Polüklonaalsed antikehad saadakse, kui süstitakse looma peptiidi antigeeniga ning seejärel, kui sekundaarne immuunvastus on stimuleeritud, isoleeritakse antikehad tervest seerumist. Seega on polüklonaalsed antikehad heterogeenne segu antikehadest, mis tunnevad ära mitmeid epitoope. Monoklonaalsed antikehad on spetsiifilised üksiku epitoobi suhtes, mistõttu peetakse neid märklaud-antigeeni suhtes enam spetsiifilisemaks kui polüklonaalseid antikehi. IHK tuvastamise strateegiate jaoks on antikehad klassifitseeritud primaarsete ja sekundaarsete reagentidena. Primaarsed antikehad on disainitud huvipakkuva antigeeni jaoks ning on tavaliselt mittemärgistatud, samas kui sekundaarsed antikehad on modelleeritud primaarse antikeha immunoglobuliinide vastu. Sekundaarne antikeha on tavaliselt konjugeeritud ühendusmolekuliga (näiteks biotiin) või on seotud otseselt reportermolekuli külge.
IHK reporterid[muuda | muuda lähteteksti]
Reportermolekulid liigitatakse nende tuvastamismeetodi põhjal. Kõige populaarsemad tuvastamismeetodid on ensüüm- ja fluorofoorvahendusega kromogeenne ja fluorestsentstuvastamine. Kromogeensete reporterite korral reageerib ensüümmärgis substraadiga, mis annab intensiivse värvusega produkti, mida on võimalik analüüsida valgusmikroskoobiga. Kuigi ensüümsubstraatide nimekiri on ulatuslik, on kaks ensüümi, alkaalne fosfataas (AP) ja mädarõika peroksüdaas (HRP), mida kasutatakse enim valkude tuvastamiseks. Saadaval on palju kromogeenseid, flouorogeenseid ja kemoluminestsents-substraate mõlema ensüümiga kasutamiseks, sisaldades näiteks DAB-d või BCIP/NBT-d, mis tekitavad vastavalt kas pruuni või lilla värvuse, olenemata sellest, kuhu ensüümid on parasjagu seotud. Reaktsiooni DAB-ga saab võimandada, kasutades niklit, mis annab tumepunase või musta värvuse. Fluorestseeruvad reporterid on väikesed orgaanilised molekulid, mida kasutatakse IHK tuvastamiseks ning mis sisaldavad üldjuhul FITC-d, TRITC-d ja AMCA-d. Kaubanduslikud derivaadid, nagu Alexa Fluor ja Dylight Fluor, annavad sarnaseid tulemusi, kuid varieeruvad hinnas. Densitomeetriline signaali analüüs võimaldab kromogeensete ja fluorestseerivate meetodite jaoks saada vastavalt poolikuid või täielikke kvantitatiivseid andmeid, et korreleerida reportersignaali taset valgu ekspressiooni või lokalisatsiooni tasemele.
Sihtmärk-antigeeni tuvastamise meetodid[muuda | muuda lähteteksti]
Otsene meetod on üheetapiline värvimismeetod, mis hõlmab märgistatud antikeha (nt FITC-ga konjugeeritud antiseerumi) otsest reageerimist koeproovis oleva antigeeniga. See meetod kasutab ainult ühte antikeha, olles seetõttu lihtne ja kiire, kuid tema tundlikkus on vähese signaali võimenduse tõttu madalam. Seetõttu on otsene meetod vähem levinud kui kaudsed meetodid.
Kaudne meetod hõlmab märgistamata primaarse antikeha seondumist koes sihtmärk-antigeeniga ning sekundaarse antikeha reaktsiooni primaarse antikehaga. Nagu eelnevalt mainitud, peab sekundaarne antikeha olema valmistatud vastava loomaliigi IgG vastu, kus primaarne antikeha on toodetud. See meetod on tundlikum kui otsesed tuvastamise moodused. Põhjuseks on signaali võimendumine, sest ühe primaarse antikeha külge seostub mitmeid sekundaarseid antikehasid, mis võivad olla konjugeeritud fluorestsents- või ensüümreporterile.
Edasist võimendust on võimalik saavutada, kui sekundaarne antikeha on konjugeeritud mitmete biotiini molekulidega, mis saavad moodustada komplekse avidiini, streptavidiini või NeutrAvidiini proteiinseostunud ensüümidega. Nimetatud kolme biotiini siduva valgu erinevuseks on nende individuaalne seondumisafiinsus endogeensetele koe sihtmärkidele. Nende valkude järjestus mittespetsiifilise seondumisafiinsuse põhjal alustades kõrgemast: 1) avidiin, 2) streptavidiin ja 3) Neutravidiinin.
Kaudse meetodi eelis lisaks suurele tundlikkusele on veel see, et standardselt konjugeeritud sekundaarseid antikehasid on vaja suhteliselt vähe luua. Näiteks märgistatud sekundaarne antikeha, mis on tehtud jänese IgG vastu ning mida saab osta kommertsiaalselt, on kasutatav mistahes primaarse antikehaga, mis on loodud jäneses. Otsese meetodiga oleks aga vajalik sildistada iga primaarne antikeha iga huvipakkuva antigeeni jaoks.
Kontrastvärvilahused[muuda | muuda lähteteksti]
Pärast sihtmärk-antigeeni immunohistokeemilist värvimist kasutatakse sageli veel teist värvi, et tõsta kontrasti, mis aitaks primaarsel värvil paremini välja paista. Paljud neist värvidest näitavad spetsiifilisust antigeenidele või diskreetsetele rakulistele komponentidele. Mõned neist värvivad aga terve raku. Nii kromogeensed kui ka fluorestsentsed värvid on IHK-s saadaval. See tagab laia reaktiivide valiku ning aitab sobituda iga eksperimentaalse katsega. Sageli kasutatakse näiteks hematoksüliini, Hoechsti värvi ja DAPI-t.
IHK veaotsing[muuda | muuda lähteteksti]
Immunohistokeemilistes tehnikates on enne koe antigeeni viimast värvimist mitmeid problemaatilisi etappe, mis võivad mõjutada kogu katse õnnestumist. Põhilised probleemid IHK värvimises on tugev tausta värvumine, nõrk antigeeni värvimine ja autofluorestsents. Endogeensete biotiinide, reporterensüümide või primaarsete/sekundaarsete antikehade ristreageerimine on tugeva taustavärvumise üks levinumaid põhjused. Nõrk värvumine võib olla põhjustatud ka kehvast ensüümaktiivusest või primaarse antikeha võimsusest. Autofluorestsents võib aga olla tingitud koe fikseerimise meetodist või iseloomust. Probleemide väljaselgitamiseks ja kõrvaldamiseks tuleb neile IHK koe ettevalmistamise aspektidele ning antikehaga värvimisele süstemaatiliselt tähelepanu pöörata.
Diagnoosi IHK markerid[muuda | muuda lähteteksti]

IHK on suurepärane detekteerimise meetod ja selle tohutuks eeliseks on võime näidata täpselt, kuhu antud valk meie uuritavas koes on lokaliseerunud. Samuti on see efektiivne viis koe uurimiseks. See on teinud selle meetodi neuroteadustes laialdaselt kasutatavaks, võimaldades teadlastel uurida valkude ekspressiooni konkreetsetes ajustruktuurides. Meetodi suureks puuduseks on aga see, et pole võimalik näidata, kas värvumisele vastab meid huvitav valk. Seetõttu peavad primaarsed antikehad olema hästi valideeritud Western Blotiga või mõne muu sellise protseduuri abil. Meetod on leidnud laialdaselt kasutust kasvajatüübi diagnostilises patoloogias (nt e-kadheriini immunovärvimine, et vahet teha DCIS-il (rinna duktaalne kartsinooma in situ: positiivne värvumine) ja LCIS-il (lobulaarne kartsinooma in situ: ei värvu positiivselt)).[2]
- Kartsinoembrüonaalne antigeen (CEA) – kasutatakse adenokartsinoomide tuvastamiseks. Ei ole asukohaspetsiifiline.
- Tsütokeratiinid – kasutatakse kartsinoomide tuvastamiseks, kuid võib ekspresseeruda ka mõnedes sarkoomides.[3]
- CD15 ja CD30 – kasutatakse Hodgkini tõve jaoks.
- Alpha fetoproteiin – rebukoti kasvaja ja hepatotsellulaarse kartsinooma jaoks.
- CD117 (KIT) – seedetrakti strooma kasvajad (GIST)
- CD10 (CALLA) – neerurakkude kartsinooma ja äge lümfoplastiline leukeemia
- Eesnäärme spetsiifiline antigeen (PSA) – eesnäärme vähi jaoks.
- Östrogeenide ja progesteroonide värvumine vähkkasvaja tuvastamiseks.
- B-rakkude tuvastamine lümfoomidest kasutades CD20.
- T-rakkude tuvastamine lümfoomidest kasutades CD3.
[muuda | muuda lähteteksti]
Vähi tõttu muutub suur osa molekulaarsetest radadest. Vähiteraapias saab mõningaid muutusi jälgida. Immunohistokeemiat kasutatakse selleks, et hinnata, millised kasvajad kõige suurema tõenäosusega alluvad ravile. Selleks tuvastatakse molekulaarse sihtmärgi olemasolu või selle kõrgendatud taset.
Keemilised inhibeerijad[muuda | muuda lähteteksti]
Kasvajate bioloogia võimaldab paljusid potentsiaalseid rakusiseseid sihtmärke. Suur osa kasvajatest on hormoonsõltuvad. Hormoonretseptorite juuresolekul määratakse, kas vähk on potentsiaalselt tundlik antihormonaalsele teraapiale. Üks esimesi ravisid oli antiöstrogeen, tamoxifen, rinnavähi raviks. Tamoxifen blokeerib östrogeense hormooni seostumise rinnavähi rakkudega. Selliseid hormoonretseptoreid saab immunohistokeemia abil tuvastada.[4]
Imatinib, mis on intertsellulaarne türosiinkinaasi inhibiitor, töötati välja ravimaks kroonilist müeloidset leukeemiat. Leukeemia on haigus, mida iseloomustab konkreetse ebanormaalse türosiinkinaasi moodustumine. Imitanib on osutunud efektiivseks kasvajate puhul, mis ekspresseerivad teisi türosiinkinaase.[5]
See artikkel on täielikult või osaliselt tõlgitud artikli(te)st Immunohistochemistry.
Viited[muuda | muuda lähteteksti]
- ↑ Ramos-Vara, JA (2005). "Technical Aspects of Immunohistochemistry". Vet Pathol. 42 (4): 405–426. DOI:10.1354/vp.42-4-405. PMID 16006601. Originaali arhiivikoopia seisuga 25. mai 2009. Vaadatud 5. novembril 2011.
- ↑ O'Malley F and Pinder S, Breast Pathology, 1st. Ed. Elsevier 2006. ISBN 978-0-443-06680-1
- ↑ Leader M, Patel J, Makin C, Henry K (detsember 1986). "An analysis of the sensitivity and specificity of the cytokeratin marker CAM 5.2 for epithelial tumours. Results of a study of 203 sarcomas, 50 carcinomas and 28 malignant melanomas". Histopathology. 10 (12): 1315–24. DOI:10.1111/j.1365-2559.1986.tb02574.x. PMID 2434403.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Jørgensen, Jan Trøst; Kirsten Vang Nielsen, Bent Ejlertsen (aprill 2007). "Pharmacodiagnostics and targeted therapies – a rational approach for individualizing medical anticancer therapy in breast cancer". The Oncologist. United States: AlphaMed Press. 12 (4): 397–405. DOI:10.1634/theoncologist.12-4-397. ISSN 1083-7159. PMID 17470682. Vaadatud 14.03.2008.
- ↑ Gold JS, Dematteo RP (august 2006). "Combined Surgical and Molecular Therapy: The Gastrointestinal Stromal Tumor Model". Ann. Surg. 244 (2): 176–84. DOI:10.1097/01.sla.0000218080.94145.cf. PMC 1602162. PMID 16858179.
