In situ hübridisatsioon
See artikkel ootab keeletoimetamist. |

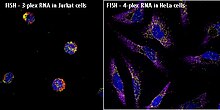
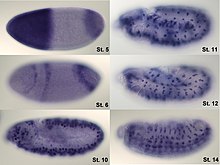
In situ hübridisatsiooni (ISH) põhimõte on fikseeritud koetükis märgistatud nukleiinhappe (DNA või RNA) ahela kinnitamine komplementaarse DNA või RNA ahela külge. Seda tehakse kuumutamisega, millele järgnevalt tuvastatakse vaatlusega uuritava sondi ehk märgistatud ahela asukoht. Seda meetodit saab kasutada selleks, et lokaliseerida DNA järjestusi kromosoomides, tuvastada RNA-d või viiruslikku DNA-d.[1]
In situ tähendab ladina keeles 'koha peal'.
In situ hübridisatsioon on hea tehnika mRNA (messenger RNA) kindlakstegemiseks koes individuaalsete rakkude sees. Sellega saab ülevaate füsioloogilistest protsessidest ja haiguste patogeneesist. Rakkudes mRNA säilitamiseks on tihti vaja kasutada ristisiduvat (crosslinking) fikseerijat (näiteks formalaldehüüd). Selle meetodiga suudame tuvastada umbes 10–20 mRNA koopiat raku kohta.
Üks probleem selle metoodikaga on see, et järjestused võivad peituda seotud proteiini tõttu või on raku struktuuri sees kaitstud. Järelikult, et uurida huvipakkuvaid rakke või kudesid, peab suurendama raku membraani läbilaskvust ja nukleotiidide sondide nähtavust ilma raku struktuuri terviklikkust lõhkumata.
In situ hübridisatsiooni kasutatakse, et leida kindlad nukleiinhapete järjestuste asukohad koes või kromosoomis. See on hädavajalik samm geenide organisatsiooni, regulatsiooni ja funktsiooni mõistmises. DNA ISH-d võib kasutada kromosoomide struktuuri kindlakstegemisel. Fluorestseeruvat DNA in situ hübridisatsiooni (FISH) saab kasutada haiguste diagnostikas kromosoomide terviklikkuse kindlakstegemisel. RNA ISH-d kasutatakse erinevate RNA-de (mRNA-d, lncRNA-d ja miRNA-d) mõõtmiseks ja lokaliseerimiseks kudede sektsioonides, rakkudes ja ringlevates kasvajarakkudes. On tehtud suuri uuringuid paljude järjestustega ja tulemused on tavaliselt Internetis saadaval (vt välislingid). In situ hübridisatsiooni leiutas Joseph G. Gall. [2][3][4]
Materjali ettevalmistamine
[muuda | muuda lähteteksti]Tavaliselt kasutatakse in situ hübridisatsiooni puhul kolme koelõiget.
a) Külmutatud lõigud. Värske kude külmutatakse väga kiiresti (pannakse −80-kraadisesse jääkappi). Seejärel asetatakse jäätunud lõigud spetsiaalsesse meediumi, mis on mõeldud õhukestele jäätunud koekihtidele. Lõigud fikseeritakse 4%-lisse paraformalaldehüüdi just enne hübridisatsiooni esilekutsumist.
b) Parafiini sisse pandud lõigud. Lõigud on fikseeritud formaliini (nagu on fikseeritud tavalised histoloogia preparaadid), mis pannakse omakorda vaha sisse (parafiinilõigud).

c) Rakud suspensioonis. Rakud pannakse kindla tehnikaga (cytospin) klaasilõikudele ja fikseeritakse metanooliga. [5]
Erinevad satelliidid
[muuda | muuda lähteteksti]On olemas nelja erinevat tüüpi sonde, mida kasutatakse in situ hübridisatsioonil.
Oligonukleotiidsed satelliidid.
[muuda | muuda lähteteksti]Neid produtseeritakse automaatse keemilise sünteesiga. See meetod kasutab desoksünukleotiide. See on ökonoomiline aga eeldab, et kasutaja juba teab spetsiifilist nukleotiidide järjestust, mida soovitakse ette valmistada. Nendel satelliitidel on eelisteks on väike suurus (tavaliselt umber 40–50 aluspaari) ja resistentsus RNaasile. See sobib ISH jaoks hästi, kuna need on väikesed ja suudavad läbida huvipakkuvad rakud või koed. Oligonukleotiidsed satelliidid on ühe ahelalised ja seetõttu ei saa toimuda renaturatsiooni (DNA ei saa võtta oma tavalist kaksikahela kuju).
Üksikahelalised DNA satelliidid.
[muuda | muuda lähteteksti]Need satelliidid on umbes 200–500 aluspaari pikad. Neid sonde toodetakse RNA pöördtranskriptsiooniga.
Kaheahelalised DNA satelliidid
[muuda | muuda lähteteksti]Neid sonde toodetakse nii, et bakteritesse viiakse sisse meid huvitav järjestus, baktereid paljundatakse, lüüsitakse, eraldatakse, DNA puhastatakse ja huvipakkuv järjestus väljub koos piiravate ensüümidega. Bakteriaalse meetodi eeliseks on, et korraga on võimalik saada suur kogus uuritavat satelliitjärjestust. Kuna see satelliit on kaheahelaline siis denaturatsioon peab toimuma enne hübridisatsiooni, et oleks võimalik ahela hübridisatsioon huvialuse mRNA-ga. Seda meetodit ei kasutata tänapäeval palju, kuna üksikud DNA ahelad kipuvad üksteisega rehübridiseeruma ja see vähendab sondide tundlikkust.
RNA satelliidid (cRNA satelliidid või ribosoomi satelliidid)
[muuda | muuda lähteteksti]RNA satelliitide eeliseks on, et RNA-RNA hübriidid ei ole tundlikud temperatuuri suhtes ja RNaasid ei mõju neile. See lubab pärast hübridisatsiooni RNaasiga lagundada mittehübridiseerunud RNA ja sellega ka võimaluse taustasodiks.[6]
Sondide märgistamine
[muuda | muuda lähteteksti]Sondide märgistamisel on kaks võimalust – radioaktiivne (tuvastatakse autoradiograafiaga) ja mitteradioaktiivne (tuvastatakse immunohistokeemia meetoditega).
1. Radioaktiivsed märgistused:
- 3H märgistus – 3H märgistus võimaldab nii suurt resolutsiooni, et on võimalik näha raku sisse, aga see vajab pikka paljastust radioaktiivsele ainele. 3H-l on pikk poolestusaeg (12 aastat) ja sonde saab hoiustada aastaid.
- 35S märgistus – 35S märgistus võimaldab näha üks raku diameetriseid elemente. See annab kiiremaid tulemusi, kuna paljastusaeg on umbes nädal. Selle märgistuse juures on oluline lisada redutseerijat sondi sisaldavale lahusele, et hoida ära väävli oksüdeerumist. Selle isotoobi poolestusaeg on 87 päeva ja sond tuleks kuu ajaga ära kasutada.
- 32P märgistuse – 32P annab halvema resolutsiooni, kui üks raku diameeter. Selle poolestusaeg on 14 päeva ja sondid peab 1 nädalaga ära kasutamata.
2. Mitteradioaktiivsed märgistused:
Mitteradioaktiivsed märgistused on ohutumad, stabiilsemad, annavad kiiremini tulemusi ja võimaldavad näha ühe raku diameetri suurusi objekte. Tundlikumad meetodid võtavad nukleotiidi derivaadi ja liidavad selle ühte mitteradioaktiivse märgisega, millele on olemas kindel antikeha või seostuv valk. Sellele järgneb hübridiseerimine ja pesemine (pestakse välja ülejääv materjal), kude inkubeeritakse (hoitakse soojas) koos märgisega siduva proteiiniga, mis on paari pandud ensüümiga. See produtseerib signaali, kasutades substraati ensüümi jaoks toodab lahustamatu ja värvitud produkti.
Mitteradioaktiivseid märgiseid on mitmeid, aga kõiki ei saa kasutada, kuna ei ole saadaval vajalikke antikehi või siduvaid valke.[7]
Protsess
[muuda | muuda lähteteksti]In situ hübridisatsiooniks kogutakse kõigepealt kudede või rakkude proovid. Seejärel töödeldakse neid nii, et huvipakkuv järjestus oleks fikseeritud kohas, kus nukleotiidhappe ahel oleks kõige paremini kättesaadav. See satelliitjärjestus on kas märgistatud komplementaarne DNA ahel või tihedamini RNA komplementaarne ahel. Konkreetne sond hübridiseerib kõrgel temperatuuril sihtmärkjärjestusega ja seejärel peseb minema üleliigse materjali, mis ei moodustanud sidet (pärast varasemat hüdrolüüsi, kasutades RNaasi, et lagundada üleliigne RNA ahel). Lahuse parameetreid, nagu temperatuuri, soola ja/või lahusti kontsentratsiooni, saab muuta, et eemaldada terve ahel, mis ei hübridiseerunud. See jätab alles ainult komplementaarsete järjestustega ahelad. Seejärel sildistatud ahel, mis oli märgistatud kasutades radio-, fluorestsents- või antigeenmärgistamise baasi, lokaliseeritakse ja mõõdetakse selle kogused koes. Neid mõõdetakse vastavalt kas autoradiograafiaga, fluorestsentsmikroskoopiaga või immunohistokeemia meetoditega. ISH-d võib kasutada ka kahe või enama transkripti tuvastamiseks, kui need on märgistatud radioaktiivse satelliidi või teiste mitteradioaktiivsete satelliitidega.
On olemas alternatiivne tehnoloogia RNA (mRNA, IncRNA ja miRNA) in situ hübridiseerimiseks ühe molekuli täpsusega – hargnenud DNA meetod (ingl branched DNA assay). See lähenemine (nt WiewRNA meetod) võimaldab visualiseerida kuni neli sihtmärki läbiviimise jooksul ning see kasutab patenteeritud sondimudelit ja bDNA amplifikatsiooni, et tekitada tundlikke ja spetsiifilisi signaale.
Proovid (rakud, koed ja ringlevad kasvajarakud) fikseeritakse ja töödeldakse, et saada ligi RNA sihtpunktidele (ingl RNA un-masking). Sihtmärgile spetsiifilised sondid (üksikud oligonukleotiidid, mis seostuvad kõrvuti RNA sihtkohtadel). Tüüpiline sond sisaldab 40 oligonukleotiidi, mis teeb kokku 20 paari, mis seostuvad kõrvuti sihtkohal, et tuvastada mRNA-d ja IncRNA-d, ning üks paar, mis seostub miRNA-ga.
Signaali võimendamine saadakse järjestikuste hübridisatsioonireaktsioonidega. Kõigepealt seostub eelvõimendaja molekul (ingl pre-amplifier molecule) iga oligonukleotiidipaariga sihtmärgi-spetsiifilisel RNA-l, seejärel seostub mitu võimendajamolekuli iga eelvõimendajamolekuliga. Järgnevalt seostuvad mitu märgisega sond-oligonukleotiidi (konjugeeritud aluseliseks fosfataasiga või otse fluorofooriga) võimendajatega.
Täielikult seostunud signaali võimendamise mehhanismil (ingl „tree“ – 'puu') on 400 seostumiskohta märgisega sondimolekulile. Kui kõik sihtmärgispetsiifilised sondid seostuvad sihtmärk-mRNA-ga, toimub 8000-kordne signaali võimendamine ühe transkriptsiooni jooksul. Erinevad kokkusobivad signaalivõimendamised lubavad teha mitu protseduuri (assay'd). Signaali saab teha nähtavaks fluorestsents- või valgusmikroskoobi abil.
ISH kasutusalad
[muuda | muuda lähteteksti]- Mikrobioloogia – mikroorganismide populatsioon ja morfoloogia.
- Patoloogia – ebanormaalsete geenide ekspressioon, patogeenide profiil.
- Arengubioloogia – embrüonaalsetes kudedes geeniekspressioonide profiilid.
- Karüotüüpide ja fülogeneesi analüüs – unikaalsed FISH mustrid individuaalsetes kromosoomides, kromosomaalsed aberratsioonid.
- Füüsiline kaardistamine – kromosoomides kloonide kaardistamine ja kaardistatud kloonide otsene määramine kromosomaalsetesse piirkondadesse heterokromatiini ja eukromatiiniga.
Viited
[muuda | muuda lähteteksti]- ↑ D.G. Wilkinson, 1992: "In situ Hybridization: A practical approach". Oxford University Press, Great Britain. lk 1
- ↑ O'Connor, Clare. "Fluorescence In Situ Hybridization (FISH)". Nature Education.
- ↑ Gall, JG; Pardue, ML (juuni 1969). "Formation and detection of RNA-DNA hybrid molecules in cytological preparations". Proceedings of the National Academy of Sciences of the United States of America. 63 (2): 378–83. DOI:10.1073/pnas.63.2.378. PMID 4895535.
- ↑ Gall, Joe. "Albert Lasker Award for Special Achievement in Medical Science". Lasker Foundation.
- ↑ "In situ hybrization protocol".
- ↑ D.G. Wilkinson, 1992: "In situ Hybridization: A practical approach". Oxford University Press, Great Britain. lk 3
- ↑ D.G. Wilkinson, 1992: "In situ Hybridization: A practical approach". Oxford University Press, Great Britain. lk 5
Välislingid
[muuda | muuda lähteteksti]- In Situ Hybridization of RNA and miRNA Probes to cells, CTCs and tissues.
- Whole-Mount In Situ Hybridization of RNA Probes to Plant Tissues.
- Preparation of Complex DNA Probe Sets for 3D FISH with up to Six Different Fluorochromes.
- Transcript In Situ Hybridization of Whole-Mount Embryos for Phenotype Analysis of RNAi-Treated Drosophila.
- Section on Neural Gene Expression (SNGE)
- RNA sequencing of pancreatic circulating tumour cells implicates WNT signalling in metastasis
- The Local Transcriptome in the Synaptic Neuropil Revealed by Deep Sequencing and High-Resolution Imaging
- In Situ Hybridization (ISH)
- In Situ Hybridization (ISH)
- ISH: in situ hybridization protocol
- [In Situ Hybridization
- in situ andmebaasid:
