Tseesium
| 55 |
1 8 18 18 8 2 |
| Cs 132,905 |
|
| Tseesium |
Tseesium on keemiline element sümboliga Cs ja aatomnumbriga 55. Tseesium asub perioodilisustabeli esimeses rühmas ja kuulub leelismetallide hulka. Tseesium on raskeim stabiilne leelismetall.
Tseesiumi avastasid 1861. aastal Robert Wilhelm Bunsen ja Gustav Robert Kirchhoff Dürkheimi mineraalvees. Kahe sinise spektrijoone järgi, mille abil element avastati, nimetati see caesium'iks (ladina keeles caesius – 'taevasinine'). Puhta elemendina esitas tseesiumi 1881. aastal Carl Setterberg.
Tseesium on väga reaktsioonivõimeline, väga pehme, kuldse värviga, väga puhtas vormis hõbedaselt läikiv metall. Kuna tseesium reageerib õhuga kohe ja väga aktiivselt, hoitakse seda suletult klaasampullis. Tseesiumi bioloogilist tähtsust ei teata, kuna see ei esine tavaliselt inimkehas, kuid ei ole ka toksiline.
Tseesiumi radioaktiivne isotoop 137Cs (poolestusajaga 30,1671 aastat), tuumalõhestumise produkt, köitis erilist avalikkuse tähelepanu, kui see Tšornobõli katastroofi tulemusena 26. aprillil 1986 suures koguses keskkonda sattus.
Ajalugu[muuda | muuda lähteteksti]
Tseesiumi avastasid Gustav Robert Kirchhoff ja Robert Wilhelm Bunsen 1861. aastal. Nad uurisid Dürkheimi mineraalvett ning avastasid pärast kaltsiumi, strontsiumi, magneesiumi ja liitiumi eraldamist sinises spektrialas kaks seni tundmatut joont. Nad järeldasid oma tähelepanekust, et uuritud mineraalvees peab olema järgmine, seni tundmatu element, millele nad panid siniste spektrijoonte järgi nimeks caesium – ladina sõnast caesius, mis tähendab 'taevasinine'.[1]
Bunsen püüdis tseesiumi teistest leelismetallidest eraldada, et elemendi omadusi uurida. Puhta tseesiumi proovi saamiseks aurustati 44 000 liitrit mineraalvett, milles uue elemendi olemasolu spektrijoonte jälgimisega tuvastati. Pärast aurustamist saadi mineraalveest 240 kg kontsentreeritud soolalahust, mis sisaldas erinevaid leelis- ja leelismuldmetalle. Leelismuldmetallid, nagu baarium, magneesium, kaltsium jne, sadestati lahusest sulfaatide või oksalaatidena (C2O42-). Pärast lahusesse jäänud ioonide nitraatideks muundamist ja etanooliga ekstraheerimist saadi naatriumioonidest vaba lahus. Sellele lahusele ammooniumkloriidi lisamise tulemusena sadenesid sealt liitiumioonid. Kaalium-, tseesium- ja rubiidiumioonid, mis olid veel lahusesse jäänud, moodustavad kõik kloroplatinaathappega reageerides vähelahustuvad soolad, mille lahustuvus kuumas vees on iga iooni korral pisut erinevad ja kaaliumsoola lahustuvus sealjuures kõige suurem. Seetõttu oli võimalik kaaliumkloroplatinaadist vähem lahustuvad tseesium- ja rubiidiumheksakloroplatinaadid sadestada, jättes kaaliumisoola veel lahusesse. Puhaste kloriidide saamiseks redutseeriti plaatinaioonid vesinikuga (neutraalseks) elemendiks, et lahuses tekiksid vees lahustuvad tseesium- ja rubiidiumkloriidid, mida järgmisena sadestada. Tseesium- ja rubiidiumkloriidide segu lahustati absoluutses etanoolis ning lisati karbonaati, et sadestada rubiidiumioonid rubiidiumkarbonaadina, mis on absoluutses alkoholis mittelahustuv sool, ja jääksid lahusesse tseesiumioonid. Rubiidiumkarbonaadi sade lahustati vees ja muundati rubidiumkloriidiks, tseesiumilahusest eraldati karbonaatioonid ja tseesiumkloriid ekstraheeriti tagasi vesikeskkonda. Mõlemad soolad sadestati kloriididena, mis on nende aktiivsete elementide üks stabiilsetest ühenditest. 44 000 liitrist mineraalveest saadi pärast selle töötlemist 9,2 grammi rubiidiumkloriidi ja 7,3 grammi tseesiumkloriidi. Puhastatud tseesiumkloriidi saamine võimaldas tseesiumi spetsiifilisi omadusi edasi uurida. Puhast tseesiumkloriidi kasutasid Bunsen ja Kirchoff ka uue elemendi molaarmassi esimeseks määramiseks, mille väärtuseks nad said 123,35 g/mol.[1]
Kumbki teadlane ei suutnud puhast tseesiumi saada, kuna sulatatud tseesiumkloriidi elektrolüüsil tekkis puhta metalli asemel sinine ühend, mida nad nimetasid subkloriidiks. Ilmselt oli see kolloidne segu tseesiumist ja tseesiumkloriidist.[2] Vesilahuse elektrolüüsil elavhõbeanoodiga moodustus kergesti lagundatav tseesiumamalgaam.[1]
Puhta tseesiumi saamiseni jõudis lõpuks 1881. aastal Carl Setterberg, kes vältis probleemi kloriididega, kasutades sulatatud soola elektrolüüsil tseesiumtsüaniidi. Esialgu oli see raskendatud tseesiumkloriidi kõrge sulamistemperatuuri tõttu, mida ta vähendas, lisades baariumtsüaniidi.[3]
Esinemine[muuda | muuda lähteteksti]

Tseesium on Maal väga haruldane element, seda esineb maakoores vaid kolm osakest miljoni kohta.[4] See on ebastabiilse frantsiumi järel kõige vähem levinud leelismetall. Suure reaktsioonivõime tõttu ei esine tseesium kunagi puhta elemendina, vaid alati ühendina. Enamasti on tseesium harva esinev lisand kaaliumi- või teistes leelismetallide soolades nagu lepidoliit, kuid tuntud on siiski ka mõned tseesiummineraalid. Kõige levinum tseesiumi sisaldav mineraal on pollutsiit (Cs,Na)2Al2Si4O12 · H2O, mille esinemine on kõige suurem Tanco kaevanduses Bernici järve ääres Lac du Bonnet' lähedal Kanadas Manitoba provintsis. Teised suured maardlad on Bikita kaevanduses Zimbabwes ja Karibibi kõrbes Namiibias. Tanco kaevandus Lac du Bonnet lähedal on ainus, kus tseesiumi kaevandatakse.[5] Haruldasemad tseesiummineraalid on näiteks tsesstibtantiit (Cs,Na)SbTa4O12 ja pautoviit CsFe2S3.
Enamiku tseesiumiühendite vees lahustuvuse tõttu on tseesium merevees lahustunud. Üks liiter merevett sisaldab 0,3 milligrammi tseesiumi. Võrdväärsetes kogustes leiame seal ka levinumaid, kuid halvemini lahustuvaid elemente, nagu nikkel, kroom ja vask.[4]
Omadused[muuda | muuda lähteteksti]
Füüsikalised omadused[muuda | muuda lähteteksti]
Tseesium on oma kõige puhtamas vormis hõbevalge värvusega pehme metall, mille tihedus on 1,873 g/cm3. Kuid juba vähese ebapuhtuse korral tundub tseesium kuldkollasena. Paljude omaduste poolest asub see rubiidiumi ja praeguste andmete järgi ebastabiilse frantsiumi omaduste vahel. Tseesiumi sulamistemperatuur 28,7 °C on leelismetallide seas madalaim (v.a ebastabiilne frantsium, mille sulamistemperatuur on tõenäoliselt madalam). Sarnaselt elavhõbedaga ja võrreldavalt galliumiga on tseesium üks kõige madalama sulamistemperatuuriga metalle üldse. Tseesium on ka väga pehme (Mohsi kõvadus 0,2) ja plastiline.
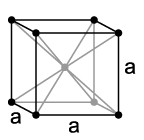
Nagu ka teised leelismetallid, kristalliseerub tseesium standardtingimustel struktuurina, mille ühikrakuks on kuubiline ruumtsentreeritud elementaarrakk võreparameetriga a=614 pm, samuti kaks valemiühikut iga elementaarraku kohta. Rõhul 41 kbar toimub faasissiire kuubiliseks tahktsentreeritud kristallstruktuuriks, võreparameetriga a= 598 pm.[6]
Tseesium seguneb teiste leelismetallidega, välja arvatud liitiumiga. Vahekorras 41% tseesiumi, 12% naatriumi ja 47% kaaliumi moodustub seni teadaolevalt kõige madalama sulamistemperatuuriga (−78 °C) sulam.[7]
Tseesium ja tema ioon Cs+ on väga suure raadiusega, nad on vastavalt kõige suuremad (väljaarvatud frantsium) aatom ja ioon. See on tingitud eriti madalast efektiivsest tuumalaengust, mistõttu välimised s- elektronid on tuumaga vähesel määral seotud. See põhjustab lisaks suurele aatomiraadiusele ka tseesiumi madalat ionisatsioonienergiat ja see omakorda ka tema suurt reaktsioonivõimet.[8]
Gaasilisel tseesiumil on ebaharilik murdumisnäitaja, väiksem kui üks. See tähendab, et elektromagnetlaine faasikiirus, antud juhul valgus, on tseesiumiaurudes suurem kui vaakumis.[9]
Keemilised omadused[muuda | muuda lähteteksti]
Frantsiumi järel on tseesium madalaima ionisatsioonienergiaga element. Väliskihi elektronide vastasmõju tõttu on tseesiumil kõige madalam elektronegatiivsus. Tseesium annab need kontaktis teiste elementidega väga kergesti ära ning moodustab monovalentseid tseesiumsoolasid. Kuna elektroni välja lüües saavutab tseesium väärisgaasi elektronkonfiguratsiooni, ei moodusta see mitmelaengulisi ioone.
Reaktsioonid tseesiumiga toimuvad reeglina väga aktiivselt, nii süttib see kohe kokkupuutel hapnikuga ning moodustab, nagu ka kaalium ja rubiidium, hüperoksiidi.
Tseesium reageerib ka veega väga aktiivselt, moodustades tseesiumhüdroksiidi. See reaktsioon toimub isegi jääga −116 °C juures.[10]
Kasutamine[muuda | muuda lähteteksti]
Tseesiumi keerulise ettevalmistamise ning tema kõrge reaktsioonivõime tõttu kasutatakse seda ainult vähesel määral. Tseesiumi rakendatakse eelkõige teadusuuringutes. Kuna tseesiumil on madal elektronide väljalöömistöö, saab seda kasutada katoodina vabade elektronide saamiseks. Samuti uuritakse tseesiumi kui võimalikku plasmamaterjali magnethüdrodünaamiliste generaatorite jaoks.[11] Kosmoselennus kasutatakse tseesiumi elavhõbeda ja ksenooni kõrval kui juhtivainet ioonijuhtivuses tema kõrge aatommassi tõttu, mis annab suurema tagasilöögi kui kergemad elemendid.[12]
Tseesiumi järgi on aastast 1967 defineeritud ajaühik sekund, mis on ajavahemik, mis võrdub 133Cs aatomi põhioleku kahe ülipeenstruktuurinivoo vahelisele siirdele vastava kiirguse 9 192 631 770 võnkeperioodiga.[13] Seepärast kasutatakse tseesiumi aatomkellades, mis loob aluse koordineeritud maailmaajale.[14] Tseesium valiti selliseks rakenduseks, kuna tema üleminek kahe põhioleku vahel 9,1 GHz-ga on veel elektrooniliste vahenditega saavutav. Selle ülemineku laius ja sellega kaasnev mõõtemääramatus ei ole tingitud aatomi omadustest. Tänu madalale aurustumistemperatuurile saab tekitada vähese vaevaga aatomkiiri madala kiiruse määramatusega.
Tseesiumi aatomite pilve saab hoida magnetoptilistes lõksudes tasakaalus ning laseri abiga μK-ni absoluutse nullpunkti lähedale külmutada. Sellisel meetodil õnnestus sagedusstabiilsust ning sellega tseesium-aatomkella täpsust oluliselt parandada.[15]
Määramine[muuda | muuda lähteteksti]
Tseesiumi määramiseks võib kasutada spektrijooni 455 ja 459 nm sinises alas.[7] Kvantitatiivselt kasutatakse neid leekfotomeetrias tseesiumi puhtuse määramiseks.
Polarograafias on tseesiumil pöörduv katoodiline aste −2,09 V (kalomelelektroodi suhtes). Seetõttu tuleb taustelektrolüüdina kasutada kvarternaarseid ammooniumühendeid (näiteks tetrametüülammooniumhüdroksiidi), kuna leelis- või leelismuldmetallidel on väga sarnased põhioleku potentsiaalid.[16]
Gravimeetriliselt saab tseesiumi, nagu ka kaaliumi, määrata mitmesuguste rasklahustuvate soolade kaudu. Näiteks sobivad selleks tseesiumi perkloraat CsClO4 ja heksakloroplatinaat Cs2[PtCl6].[17]
Bioloogiline tähtsus[muuda | muuda lähteteksti]
Tseesium inimkehas tavaliselt ei esine. Peamiselt toiduga omandatud tseesium, oma sarnasuse tõttu kaaliumiga, imendub seedetraktis ning analoogiliselt kaaliumiga ladestub peamiselt lihasmassis. Bioloogiline poolväärtusaeg, mille jooksul tseesium inimkehast väljub, sõltub vanusest ja soost ning on keskmiselt 110 päeva.[18]
Tseesium on keemiliselt ainult väga vähesel määral mürgine. Tüüpiline LD50-väärtus tseesiumsooladele on 1000 mg/kg.[11] Tähendusliku toksilise toimega on siiski radioaktiivse tseesiumisotoobi ioniseeriv kiirgus, mis põhjustab, sõltuvalt doosist, kiiritushaigust. Tseesiumsoolade hea lahustuvuse tõttu vees imenduvad need seedetraktis täielikult ning ladestuvad lihasmassis.[19] Pärast Tšornoboli katastroofi 1986. aastal põhjustas radioaktiivse tseesiumisotoobi 137Cs ladestumine kehas esimesel kolmel kuul keskmise efektiivse doosi 0,6 μSv ühe täiskasvanud inimese kohta (Saksamaal).[18]
Ohutusnõuded[muuda | muuda lähteteksti]
Tseesium süttib õhu käes spontaanselt, seepärast tuleb seda säilitada kinnises klaasampullis puhtas argoonis või vaakumis. Tugeva reaktsioonivõime tõttu reageerib tseesium veega plahvatuslikult. Plahvatusohtu võib teravdada ka reaktsioonil tekkinud vesinik. Põlevat tseesiumi tuleb kustutada metalltulekustutiga või kuiva liivaga. Tseesiumi kõrvaldamine käib nagu ka teiste leelismetallide korral: tilgutades ettevaatlikult mõnda sellist alkoholi nagu 2-pentanool, tert-butanool või oktanool ning seejärel neutraliseerides.
Ühendid[muuda | muuda lähteteksti]
Nagu tüüpiline leelismetall, esineb tseesium eranditult ioonsetes ühendites oksüdatsiooniastmega +1. Enamik tseesiumiühendeid lahustub vees.
Halogeniidid[muuda | muuda lähteteksti]
Tseesium moodustab kõigi halogeenidega vees lahustuvaid halogeniite valemiga CsX (X- halogeen). Tseesiumkloriidil on iseloomulik kristallstruktuur, mis on üks olulisemaid kristallstruktuure. Nii kristalliseeruvad, välja arvatud tseesiumfluoriid, ka teised tseesiumhalogeniidid. Tseesiumkloriid on puhta tseesiumi saamiseks lähteaineks. Kuna see moodustab piisavalt pikaajalisel tsentrifuugimisel tihedusgradiendi, kasutatakse tseesiumkloriidi DNA eraldamiseks ja puhastamiseks ultratsentrifuugimises.[11]
Hapnikuga ühendid[muuda | muuda lähteteksti]
Tseesium moodustab ebatavaliselt suurel hulgal hapnikuühendeid. On teada mitmeid suboksiide, näiteks Cs11O3 ja Cs3O, mille puhul on tegemist tseesiumi liiaga ja on näha elektrijuhtivust. Lisaks on teada suurenenud hapnikusisaldusega oksiid Cs2O, peroksiid Cs2O2, hüperoksiid CsO2 ja osoniid CsO3. Kõik need ühendid on erinevalt teistest tseesiumiühenditest värvilised, suboksiidid on violetsed või sinakasrohelised ja teised kollased, oranžid või punased. Tseesiumhüdroksiid on tugevalt hügroskoopne valge tahke aine, mis lahustub ainult vees. Tseesiumhüdroksiidi peetakse tugevaimaks aluseks vesikeskkonnas.
Teised tseesiumiühendid[muuda | muuda lähteteksti]
Tseesiumkarbonaat on valge tahke aine ja lahustub paljudes orgaanilistes lahustites. Seda kasutatakse paljudes orgaanilistes sünteesides alusena, näiteks ümberesterdamisel või eriliste kaitserühmade kõrvaldamiseks.[20]
Tseesiumnitraat leiab suuremat kasutust sõjalises pürotehnikas,[21] NIR-rakettides[22] ja infrapunasuitsukamuflaažides.[23].
Tseesiumkromaati võib koos tsirkooniumiga kasutada vee- ja hapnikujälgede ärahoidmiseks vaakumtorus puhta tseesiumi saamisel.[24]
Viited[muuda | muuda lähteteksti]
- ↑ 1,0 1,1 1,2 G. Kirchhoff, R. Bunsen: Chemische Analyse durch Spectralbeobachtungen. In: Annalen der Physik und Chemie. 1861, 189, 7, S. 337–381 (DOI:10.1002/andp.18611890702).
- ↑ Richard Zsigmondy: Colloids and the Ultramicroscope. Read books, 2007, ISBN 978-1-4067-5938-9, S. 69 (Mall:Google Buch).
- ↑ Carl Setterberg: Ueber die Darstellung von Rubidium- und Cäsiumverbindungen und über die Gewinnung der Metalle selbst. In: Justus Liebigs Annalen der Chemie. 1881, 221, 1, S. 100–116 (DOI:10.1002/jlac.18822110105).
- ↑ 4,0 4,1 David R. Lide (ed.): CRC Handbook of Chemistry and Physics, 90. Auflage, CRC Press, Boca Raton, Florida, 2005, ISBN 978-1-4200-9084-0. Section 14, Geophysics, Astronomy, and Acoustics; Abundance of Elements in the Earth's Crust and in the Sea.
- ↑ U.S. Geological Survey: Caesium. In: Mineral Commodity Summaries, Januar 2009.
- ↑ K. Schubert: Ein Modell für die Kristallstrukturen der chemischen Elemente. In: Acta Crystallographica. 1974, B30, S. 193–204, DOI:10.1107/S0567740874002469.
- ↑ 7,0 7,1 Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie, 102. Auflage, de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1274.
- ↑ Michael Binnewies, Michael Jäckel, Helge Willner: Allgemeine und Anorganische Chemie. Spektrum Akademischer Verlag, Berlin 2003, ISBN 978-3-8274-0208-0, S. 49–53.
- ↑ L. J. Wang, A. Kuzmich, A. Dogariu: Gain-assisted superluminal light propagation. In: Nature. 2000, 406, S. 277–279 (DOI:10.1038/35018520).
- ↑ Caesium bei webelements.com, eingesehen am 5. September 2009.
- ↑ 11,0 11,1 11,2 Manfred Bick, Horst Prinz: Cesium and Cesium Compounds. In: Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim 2005 (DOI:153 10.1002/14356007.a06 153).
- ↑ Europäische Weltraumorganisation: Ionentriebwerke: Der Ritt auf geladenen Teilchen. Stand September 2003, abgerufen am 26. September 2009.
- ↑ Resolution 1 of the 13th meeting of the CGPM (1967/68)
- ↑ Andreas Bauch: Lieferanten der Zeit. In: Physik in unserer Zeit. 1994, 25, 4, S. 188–198 (DOI:10.1002/piuz.19940250412).
- ↑ Andreas Bauch: Zeitmessung mit Fontänen: Atomuhren. In: Physik in unserer Zeit. 2001, 32, 6, S. 268–273 (DOI:<268::AID-PIUZ268>3.0.CO;2-N 10.1002/1521-3943(200111)32:6<268::AID-PIUZ268>3.0.CO;2-N).
- ↑ J. Heyrovský, J. Kůta: Grundlagen der Polarographie, Akademie-Verlag, Berlin 1965, S. 509.
- ↑ Caesium. In: Lexikon der Chemie. Spektrum Verlag, Heidelberg 2000.
- ↑ 18,0 18,1 Jenny Hartmann-Schreier: Caesium 137, Caesium 134. In: Römpp Chemie-Lexikon, Thieme-Verlag, Stand März 2006.
- ↑ Römpp Lexikon Lebensmittelchemie, 2. Auflage, Georg Thieme Verlag, Stuttgart 2006, ISBN 978-3-13-143462-3, S. 166.
- ↑ Timo Flessner, Sven Doye: Cesium carbonate: A powerful inorganic base in organic synthesis. In: Journal für praktische Chemie. 1999, 341, 2, S. 186–190 (DOI:<186::AID-PRAC186>3.0.CO;2–6 10.1002/(SICI)1521-3897(199902)341:2<186::AID-PRAC186>3.0.CO;2–6).
- ↑ E.-C. Koch: Special Materials in Pyrotechnics, Part II: Application of Caesium and Rubidium Compounds in Pyrotechnics. In: J. Pyrotech., 2002, 15, S. 9–24 (Abstract).
- ↑ C. W. Lohkamp: USP 3 733 223, The United States as represented by the Secretary of the Navy, USA, (1973).
- ↑ M. Weber DE 32 38 444, Pyrotechnische Fabrik F. Feistel GmbH & Co. KG, Göllheim, Germany, (1982)
- ↑ Helmut Sitzmann: Caesium-Verbindungen. In: Römpp Chemie-Lexikon, Thieme Verlag, Stand Mai 2005.
| Vikisõnastiku artikkel: tseesium |



