Liitumisreaktsioon: erinevus redaktsioonide vahel
P r2.7.2) (Robot: muudetud nl:Additiereactie |
LaaknorBot (arutelu | kaastöö) P r2.7.3rc2) (Robot: lisatud tr:Katılma Tepkimeleri |
||
| 55. rida: | 55. rida: | ||
[[sv:Additionsreaktion]] |
[[sv:Additionsreaktion]] |
||
[[vi:Phản ứng cộng]] |
[[vi:Phản ứng cộng]] |
||
[[tr:Katılma Tepkimeleri]] |
|||
[[zh:加成反应]] |
[[zh:加成反应]] |
||
Redaktsioon: 4. detsember 2012, kell 21:35
Liitumisreaktsioon on orgaaniline reaktsioon, milles kaks või enam molekuli ühinevad üheks suuremaks molekuliks.
Liitumisreaktsioonidesse astuvad kaksik- või kolmiksidet sisaldavad molekulid: alkeenid (C=C), alküünid (C≡C), karbonüülrühma (C=O), imiinrühma (C=N) jt sisaldavad ühendid. Näiteks etüleeni broomimine:
- H2C=CH2 + Br2 → BrH2C-CH2Br
Mehhanismid
Olenevalt reaktsioonis osalevate ühendite keemilisest olemusest eristatakse nelja põhilist liitumisreaktsiooni mehhanismi:
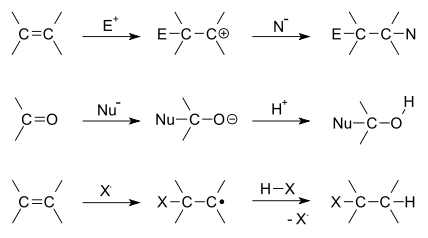
- elektrofiilne liitumine (tähistatakse AdE; karbokatioonne intermediaat)
- nukleofiilne liitumine (tähistatakse AdN; anioonne intermediaat)
- radikaalne liitumisreaktsioon (tähistatakse AdR; vaba radikaalne intermediaat)
- sünkroonliitumine (enamasti tsükloliitumine, näiteks Diels-Alderi reaktsion))
Siia kuulub ka liitumispolümerisatsioon (ahelpolümerisatsioon), mille puhul aktiivse intermediaadi genereerimine (initsieerimine) toimub analoogselt eeltoodud mehhanismidega. Need on katioonne polümerisatsioon, anioonne polümerisatsioon, radikaalpolümerisatsioon ja koordinatsioonipolümerisatsioon.


Sün- ja anti-liitumine
Orgaaniliste liitumisreaktsioonide korral tähendab sün-liitumine mõlema liituva rühma ühinemist kaksik- või kolmiksidemega ühelt ja samalt poolelt. Anti-liitumise korral ühinevad rühmad molekuliga selle vastaspooltelt.
Vaata ka
| Pildid, videod ja helifailid Commonsis: Liitumisreaktsioonid |
- Ühinemisreaktsioon
- Ahelpolümerisatsioon
- Liitumis-elimineerimisreaktsioon (näiteks nukleofiilne atsüülasendusreaktsioon)
