Vesinikelektrood
Vesinikelektroodiks nimetatakse elektroodi, millel kasutatakse vesinikgaasi H2 (või sellel tekib vesinikgaasi). Vesinikelektroode kasutatakse füüsikalises keemias referents- ehk võrdluselektroodina mitmesuguste elektrokeemiliste mõõtmiste korral, eelkõige metallide elektroodipotentsiaali kindlaksmääramisel.
Vesinikelektroodi elektrilist potentsiaali kirjeldab reaktsioon
Kasutatakse standardvesinikelektroode SHE (lühend inglise keele sõnadest Standard Hydrogen Electrode) ja normaalvesinikelektroode NHE (Normal Hydrogen Electrode), mille puhul ei järgita kõiki standardtingimusi.
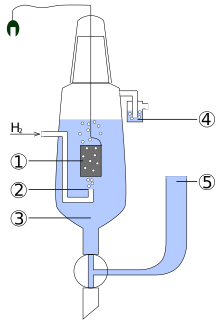
1 – pulbrilise plaatinakattega plaatinaelektrood
2 – vesiniku juurdevool
3 – happe lahus (H+ = 1 mol/l)
4 – vesilukk, mis tõkestab õhuhapniku juurdepääsu
5 – ühendus moodustatava galvaanielemendi teise elektroodiga, mille potentsiaali mõõdetakse
Standardne vesinikelektrood
[muuda | muuda lähteteksti]Klaaskestas on vesinikelektrood protoonses (vesinikuioonide) vesilahuses. Harilikult on selleks vesinikkloriid (HCl), mille kontsentratsioon H+ = 1 mol/l (mool liitri kohta) ehk ioonide aktiivsus on 1.
Kuna vesinikku ei saa vahetult elektroodiks vormida ja pealegi ei juhi vesinik elektrit, kasutatakse neutraalsest väärismetallist – plaatinast – abielektroodi. See ümbritsetakse vesinikgaasiga (rõhul 1013 hPa), millest vesinikuaatomid adsorbeeruvad plaatina pinnale, kattes selle õhukese vesinikukihiga. Nii kujuneb tasakaal happe vesinikuaatomitega ja elektrokeemiline potentsiaal.
Standardse vesinikelektroodi potentsiaal
[muuda | muuda lähteteksti]Standardse vesinikelektroodi potentsiaal ehk standardelektroodipotentsiaal E0 protoonse lahusti vesilahuses loetakse elementide potentsiaaliskaalal nullpunktiks. SHE absoluutne elektroodipotentsiaal E0(H+/H2)H2O (abs) on IUPACi määratluse kohaselt 4,44±0,02 V temperatuuril 298,15 К.[1]

