Mitteinvasiivne sünnieelne diagnostika
Mitteinvasiivne sünnieelne diagnostika on üks diagnostika võimalusi, mille eesmärk on võimalikult vähese sekkumisega ja võimalikult täpselt ning usaldusväärselt hinnata loote kromosoomhaigusi ja arenguhäireid.[1]
Sünnieelne diagnostika on loote kaasasündinud arenguhäirete uurimine. Keskendutakse nii geeni- kui ka kromosoomihäiretele, aga ka väärarendite ning kaasasündinud haiguste tuvastamisele. Mitteinvasiivse diagnostika puhul määratakse kaudseid markereid, mitte otseselt loote materjali ning hinnatakse kromosomaalse haiguse esinemise riski. Kuna mitteinvasiivse diagnostika puhul määratakse kaudseid markereid, siis see ei võimalda panna lõplikku diagnoosi ning kõrge riskiga tulemuse peab kinnitama invasiivse protseduuriga, mille käigus võetakse loote materjali (koorionibiopsia puhul platsenta tükk või amniotsenteesi käigus lootevedelikku). Invasiivseid meetodeid iseloomustab kõrge sekkumise tase ning küllalt suur oht raseduse katkemiseks pärast protseduuri.[1] Seega on vaja hoida mainitud meetodite kasutamine võimalikult minimaalsena, et välistada liigne oht rasedusele. Selleks on võetud kasutusele mitteinvasiivsed diagnostikameetodid.[2]
Levinud meetodid kliinilises praktikas[muuda | muuda lähteteksti]
Tänapäeva kliinilises praktikas võib mitteinvasiivne diagnostika tugineda ultraheliuuringule ja ema veres leiduvate valguliste markerite määramisele (kombineeritud sõeluuring, OSCAR-test) või/ja ema veres leiduva loote rakuvaba DNA analüüsimisele (NIPT).
Kombineeritud sõeluuring (OSCAR)[muuda | muuda lähteteksti]
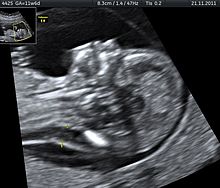
OSCAR test on kombineeritud riskihinnangu testi, mis koosneb ultraheliuuringust ning veres leiduvate valguliste markerite analüüsist. Uuringut teostatakse raseduse 1. trimestril (11-14 nädalal) ning on nii emale kui kui ka lootele ohutu. Veres leiduvad põhimarkerid on vaba-beeta HCG ja PAPP-A (plasmaproteiin A) [3]. Ultrahelis mõõdetakse loote kuklavoldi paksust ja kontrollitakse ninaluu olemasolu. Kuklavoldi paksuse seos trisoomiatega avastati 20. sajandi lõpus [4]. Loote kuklavolt on tavaliselt väga õhuke, kuid mõnede kromosomaalsete ja strukturaalsete probleemide korral võib see pakseneda, 2. trimestril on üldiselt loote kuklavolt normaliseerunud, mistõttu on oluline teha uuring enne seda. Haiguste riskide määramisel võetakse arvesse nii ultraheli kui ka vereanalüüsi tulemusi. Hinnatakse kui kõrge on risk kolmele kromosomaalsele haigusele: trisoomia 21 (Downi sündroom), trisoomia 18 (Edwardsi sündroom) ja trisoomia 13 (Patau sündroom). OSCAR-testi puhul jäävad paljud kromosomaalsed muutused leidmata. Juhul, kui OSCAR-iga tuvastamata jäänud kromosomaalsed haigused ei põhjusta väärarendeid, siis haigus jääb tuvastamata ka hilisemas raseduse faasis tehtud ultraheliuuringus. Teine OSCAR-i testi nõrk koht on valepositiivsete tulemuste suur osakaal[5].
NIPT[muuda | muuda lähteteksti]

Mitteinvasiivne sünnieelne testimine ehk NIPT (Non-invasive Prenatal Testing) on kromosoomhaiguste uuring, mis põhineb ema veres leiduva loote rakuvaba DNA (cffDNA) analüüsil. cffDNA satub ema verre kui trofoblasti rakud, mis moodustavad platsenta, surevad apoptoosi teel. See moodustab kogu ema veres ringlevast DNA-st ligikaudu kümnendiku. CffDNA on heaks loote geneetilise materjali allikaks lisaks mitteinvasiivsele kogumisvõimalusele veel kahel põhjusel – see on ema veres tuvastatav juba raseduse esimesel kolmandikul ning see kaob ema verest küllalt kiiresti pärast sünnitust. [1] Loote DNA olemasolu ema veres avastati 1997 aastal, see leid avas uued võimalused mitteinvasiivseks loote geneetiliseks testimiseks[6]. cffDNA eraldatatakse ema verest ning sekveneeritakse ehk analüüsitakse geneetilist järjestust. Geneetilisest järjestusest on võimalik hinnata kromosoomide anomaaliaid ning sellest teha riskihinnang kromosomaalsete kõrvalekallete esinemiseks suunatud (targeted) analüüsi tehes keskendutakse ainult spetsiifilistele genoomi piirkondadele [7]. Juhul, kui sekveneeritakse kogu genoom (whole genome), siis võimaldab NIPT hinnata kõikide kromosoomide kõrvalekaldeid[7]. Selliseid leide kromosoomaalsetest kõrvalekalletest, mis ei ole seotud kindla sündroomiga (nagu 21.kromosoomi trisoomia Downi sündroomiga), nimetatakse juhuleidudeks. Juhuleiu esinemine tõstab rasedustüsistuste tekke riski ning seetõttu peaks juhuleiu esinemise korral raseduse kulgu hoolikamalt jälgima, kuid see ei anna konkreetset teavet profülaktiliseks sekkumiseks[8]. NIPT testi puhul on 10 korda vähem valepositiivseid tulemusi kui OSCAR testi puhul[5].
Mõjutavad faktorid[muuda | muuda lähteteksti]
NIPT analüüsi tulemusi võivad mõjutada mitmed tegurid, sealhulgas:
"Loote fraktsioon" mis näitab, milline protsent ema veres leiduvast ringlevast vabast loote DNA-st (cfDNA) on pärit lootest. Mida suurem on loote fraktsioon, seda kindlam võib testi tulemustes olla, sest see võimaldab selgemalt eristada loote DNA-d ema DNA-st. Madal loote fraktsioon võib olla tingitud suuremast kehakaalust [9], varajasest rasedusest, loote anomaaliatest. Madala loote fraktsiooni korral oleks vajalik anda uus vereproov, et tagada usaldusväärne tulemus.
Pahaloomulise kasvaja olemasolu tekitab NIPT analüüsil vastuolulisi tulemusi, mis ei ole usaldusväärsed. NIPT analüüsi mustrid võivad osutada pahaloomulisele kasvajale, mis võib olla kasulik täiendavatele kliinilistele uuringutele kasvaja tuvastamiseks [10]. Sellegipoolest ei pruugi see tähendada, et lootel esineb anomaaliaid, vaid tulemused võivad olla tingitud ema kasvajast.
Veel üks tulemuste mõjutaja on loote mosaiiksus, mis tekib rakkude pooldumisel arengu eri etappides. Mosaiiksusel on erinevaid variatsioone: esineb ainult lootel või platsental; esineb mõlemal või kannavad osad looterakud normaalset kromosoomide komplekti ja teised rakud kromosomaalseid anomaaliaid [11]. Juhul kui anomaalia on platsentas, aga mitte lootel, siis võib NIPT test näidata kõrgemat riski, kuigi lootel anomaaliat ei esine. Samas võib NIPT test jätta detekteerimata anomaalia, mis esineb ainult lootel ja mitte platsental. Mosaiiksust ei esine igal lootel, selle esinemissagedus on 1-3% rasedustest [12]. Mosaiiksuse kahtluse puhul on vajalikud täiendavad diagnostilised testid, amniotsentees või koorionibiopsia.
Muud metoodid[muuda | muuda lähteteksti]
Mitteinvasiivsete sünnieelse diagnostika meetodite väljatöötamisel on probleemile võimalik läheneda erinevaid teid pidi. Testi väljatöötamisel lähtutakse ema veres ringlevast loote geneetilisest materjalist, mis võib olla nii DNA kui ka RNA kujul. [1]
Epigeneetiliste mustrite analüüs[muuda | muuda lähteteksti]
Teine võimalus loote DNA-d ema omast eraldada on uurida loote DNA epigeneetilisi markereid, mis erinevad ema DNA-st. Tegemist on muutustega geenide avaldumise regulatsioonis, mitte konkreetsetes DNA järjestustes, ning enamasti kantakse need edasi teatud DNA järjestuste metülatsiooni abil. Kui mõnda geeni on vaja ekspresseerida, siis on tema promootorala reeglina üsna madala metülatsioonitasemega ehk hüpometüleeritud ja sisaldab vähe lisametüülrühmadega tsütosiine. Samas kui geeni ekspressioon on vaja alla suruda, on vastav ala hüpermetüleeritud ehk sisaldab keskmisest rohkem metüleeritud tsütosiini molekule. [13] Erinevate uuringutega on näidatud, et ema veres ringlev loote DNA on pärit platsentast. Platsentas ning loote arengu käigus avalduvad hoopis erinevad geenid nendest, mis parajasti ema organismis kõrgelt ekspresseeritud on ning seetõttu esinevad ka erinevused DNA metülatsioonimustris. Siin võib eristada kahte suunda – juhud, kus loote DNA piirkond on hüpometüleeritud ning emal hüpermetüleeritud, või vastupidi – lootel hüpermetüleeritud ja emal hüpometüleeritud.[1]
Kui võtta uurimisel aluseks DNA epigeneetilised mustrid, on võimalik tuvastada tavalisemates kromosoomiarvu häireid põhjustavates kromosoomides DNA piirkondi, mille puhul metülatsioonimuster erineb emal ja lootel. Sel juhul saab eraldada konkreetse metülatsioonitaseme järgi loote vastava DNA lõigu, seda mitmekordistada polümeraasi ahelreaktsiooni (PCR) abil ning võrrelda selle taset normaalse kromosoomistiku puhul esinevaga. [2]
Loote DNA hüpometülatsioon[muuda | muuda lähteteksti]
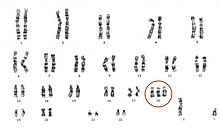
Olukorras, kus loote DNA uuritav lõik on hüpometüleeritud ja sisaldab võrdlemisi vähe metüülrühmi, peaks ema DNA olema hüpermetüleeritud. Üheks näiteks on SERPINB5 geeni promootorala. See geen asub 18. kromosoomis ning on seega heaks markeriks selle kromosoomi trisoomia testimisel. Teadlastel õnnestus metülatsioonspetsiifilise polümeraasi ahelreaktsiooni abil see loote geen eraldada ema rakuvabast DNA-st ema veres ning tõestada ka selle seos rasedusega. SERPINB5 on esimene tuvastatud universaalne cffDNA marker, mida saab kasutada sõltumata loote soost ja genotüübist. Kasutatud metoodikal on siiski üks oluline viga – selline metülatsioonispetsiifiline PCR põhineb DNA töötlemisel vesiniksulfitiga, mis muudab metüleerimata tsütosiini uratsiiliks ning lagundab seetõttu ligikaudu 95% analüüsitavast DNA-st. [1][2]
Loote DNA hüpermetülatsioon[muuda | muuda lähteteksti]
Olukord, kus on hüpermetüleeritud loote DNA ning ema vastava geeni promootorala on hüpometüleeritud, pakub tunduvalt perspektiivikamaid võimalusi sobilike DNA markerite leidmiseks. Sel juhul pole probleemiks ka metülatsioonspetsiifilise PCR käigus kasutatav vesiniksulfitiga töötlemine, sest see ei kahjusta hüpermetüleeritud DNA-d. Geene, mille promootorala on lootes hüpermetüleeritud ning ema DNA-s hüpometüleeritud, on tuvastatud nii 13., 18. kui ka 21. kromosoomis.[2]
RNA-põhised meetodid[muuda | muuda lähteteksti]
Nagu mainitud, on platsenta hea allikas loote geneetilise materjali saamiseks. Sarnaselt cffDNA-ga eritab platsenta ka loote rakuvaba RNA-d (cffRNA), kuid tunduvalt suuremas koguses kui cffDNA-d. Samas on RNA isoleerimine tehniliselt palju keerulisem ning RNA-de koostises ja avaldumise tasemes esineb populatsioonis väga palju variatsioone. Test, millega saaks määrata kõigi populatsioonis esinevate raseduste korral geneetiliste häirete esinemist, peaks sisaldama enam kui ühe markeri samaaegset määramist ühe kromosoomi jaoks, et välistada polümorfismidest tingitud valenegatiivsed tulemused. Praeguseks on tuvastatud mitmed markeriks sobilikud mRNA molekulid, mis on transkribeeritud 13., 18. või 21. kromosoomilt.[2]
Kromosoomide arvu hindamine[muuda | muuda lähteteksti]
Kui ema verest on tuvastatud sobilik DNA või RNA marker, tuleb selle hulk kvantiteerida ning määrata kindlaks, kas tegemist on euploidse või aneuploidse lootega. Praeguste teadmiste juures on üks töökindlamaid viise seda teha alleelide suhte hindamine. Alleelide suhte hindamisel kasutatakse üksiknukleotiidsete polümorfismide (SNP) määramist.[2] Kuna loode pärib ühe alleeli ühelt vanemalt ning teise teiselt, peaks heterosügootse euploidse loote korral ema veres nende omavaheline suhe olema ligikaudu 1:1. Kui aga tegemist on aneuploidse lootega, erineb see suhe märkimisväärselt. Erinevaid alleele saab eraldada siiski vaid heterosügootse loote puhul, kes on vanematelt pärinud erinevad alleelid. Kui aga loode on homosügootne antud DNA piirkonna suhtes, tuleb kasutada mõnda teist markerit. Selleks, et kogu populatsiooni saaks ühe testiga hinnata, tuleks kombineerida mitme eri markeri määramine ühe kromosoomi arvu kõrvalekalde kohta. [1] See meetod on küll loote soost sõltumatu, kuid polümorfismide esinemisest sõltuv. Seetõttu esinevad selle kasutamisel küllalt suured piirangud.[2]
Teine võimalus määrata kromosoomi ploidsust on epigeneetiline-geneetiline lähenemine. Selle meetodiga määratakse võimaliku aneuploidse kromosoomi puhul loote epigeneetilise markeri (näiteks metülatsioonimustri) tase ning võrreldakse seda mõne teise teadaolevalt euploidse kromosoomi geneetilise markeri (DNA järjestuse) tasemega. Kui need erinevad teineteisest oluliselt, võib eeldada, et lootel on tuvastatud uuritava kromosoomi aneuploidsus.[1]
Perspektiivikad uurimissuunad[muuda | muuda lähteteksti]
Eelmainitud metoodikad on jõudnud juba laiemasse kasutusse, kuid lisaks on veel mitmeid lähenemisi, mis võivad lähiaastatel tuua loodetud läbimurde erinevate geneetiliste haiguste mitteinvasiivsesse testimisse. Nendeks on
- platsenta mikroRNA-de kui uute võimalike markerite uurimine;
- platsenta makroRNA-de kui uute võimalike markerite uurimine.
Ülaltoodud meetodid on siiski veel erinevas uurimisjärgus, kuid lisanduvad tõenäoliselt järgmise 10 aasta jooksul ka kliinilisse praktikasse.[2]
Sünnieelne diagnostika Eestis[muuda | muuda lähteteksti]
Eestis on kasutusel esimese testina I trimestri kombineeritud skriining ning selle skriiningu keskmise riski tulemuse korral tehakse teise rea testina NIPT alates aastast 2020[14]. Kui tuvastatakse kõrgenenud risk mõnele häirele, viiakse ema nõusolekul läbi invasiivne uuring, millega täpsustatakse konkreetse kromosoomhaiguse esinemine.[15]
Teine ultraheliuuring viiakse läbi raseduse 19.–21. nädalal. Selle uuringu käigus hinnatakse loote kasvu, lootevee hulka, platsenta asetust ning tehakse põhjalik loote elundkondade ülevaatus, et tuvastada võimalikke väärarendeid või muid terviseprobleeme.[15]
Edasise raseduse käigus hinnatakse pidevalt raseduse kulgu, kuid ilma mõjuva põhjuseta enam korduvaid looteuuringuid arenguhäirete hindamise eesmärgil läbi ei viida.[15] Mitmel pool saab lisaks riigi garanteeritud ja rahastatud uuringutele rasedatele lisatasu eest teha lisaks ultraheliuuringuid või NIPT teste.
Sünnieelne diagnostika väljaspool Eestit[muuda | muuda lähteteksti]
Enamikes Euroopa riikides on esimese astme sünnieelne sõeluuring OSCAR, aga Belgia on esimene riik, mis pakub alates 2017.aastast NIPT-i esimese astme sõeluuringuna ja see on riiklikult rahastatud. Hollandis on pakutud 2014.aastast NIPTi rasedatele, kellele OSCAR andis kõrgema riski, kuid alates 2023. aasta aprillist on võimalik teha testi kõikidel rasedatel esmase loote kromosoomhaiguste sõeluuringuna [16][17].
Aasias, eriti Hiinas, Jaapanis ja Indias, on NIPT-i vastuvõtmine olnud aeglane, kuid tõusuteel. 2016. aastal avaldas Hiina riiklik tervishoiukomisjon ravijuhised NIPT kasutamiseks 12–22 rasedusnädalal. Sellegipoolest ei ole Hiinas veel NIPT täielikult riigi poolt rahastatud. Jaapanis on NIPT kättesaadav alates 2013. aastast, kuid see on tasuline ja seda soovitatakse peamiselt kõrge riskiga rasedatele . Põhja-Ameerikas ja Lõuna-Ameerikas on NIPT-i kasutamine levinud, kuid sõeluuringu kättesaadavus ja rahastamine varieerub riigiti. USA-s on NIPT rutiinne T21 sõeluuringuna alates 2011. aastast, Kanadas on NIPT rahastatud teise astme sõeluuringuna OSCARi järel. Brasiilias, Mehhikos ja teistes Ladina-Ameerika riikides on NIPT laialt levinud eratervishoiu sektori kaudu ning enamik teste ei ole riiklikult rahastatud. Lähis-Idas, nagu Liibanonis ja Iisraelis, pakutakse NIPT-i peamiselt erasektoris ja ei ole kaasatud riiklikku sünnieelsesse sõeluuringusse [17].
Kommertsiaalsed NIPT testid[muuda | muuda lähteteksti]
Allolevas tabelis on esitatud Eesti turul kättesaadavad NIPT testid.
| Ettevõte | SYNLAB | GenePlanet test | Tervisetehnoloogiate Arenduskeskus | Natera |
| Testi nimi | NeoBona (Advanced) | NIFTY (plus) | NIPTIFY | Panorama Prenatal Test |
| Mida testitakse? | 13., 18. ja 21. kromosoomi trisoomiad, sugukromosoomide arvu häired, loote sugu | 13., 18. ja 21. kui ka 9., 6. ja 12. kromosoomi trisoomiad, sugukromosoomide arvu kõrvalekalded, mikrodeletsioonid/duplikatsioonid, loote sugu | Ülegenoomne uuring (kõikide kromosoomide trisoomiad ja monosoomiad), sugukromosoomide arvu kõrvalekalded, mikrodeletsioonid/duplikatsioonid, loote sugu | 13., 18. ja 21. kromosoomi trisoomiad, sugukromosoomide arvu häired, 5 mikrodeletsiooni, triploidia, loote sugu |
| Testi tundlikkus | 99,1% tuvastusmäär trisoomiate avastamiseks, valepositiivsuse määr: < 1/1500 analüüsist | Üle 99% avastamismäär 13.,18. ning 21. kromosoomi trisoomiate tuvastamisel, alla 0,14% valepositiivseid vastuseid | Üle 99,9% avastamismäär 13.,18. ning 21. kromosoomi trisoomiate, X kromosoomi monosoomia ja 22q11 mikrodeletsiooni tuvastamisel | 96,4-99% tuvastusmäär trisoomiatele, 92,9% Turneri sündroomi (45,X) korral ja 83,6-99% mikrodeletsioonide korral ja 99% triploidia korral. |
Osad NIPT testid võimaldavad hinnata ka ühe geeni mutatsioonist põhjustatud haigusi[23][24].Loote soo täpne määramine võimaldab välistada isaliini pidi päranduvate Y-kromosoomil esinevate haiguste edasikandumise.[1] Lisaks testitakse reesusnegatiivsete emade loodet ka reesusfaktori suhtes, et ennetada võimalikku reesuskonflikti arenemist lootel. Nagu ka AB0 veregrupisüsteemi puhul on reesussüsteemi korral suur oht, et kui reesusnegatiivse ema veri puutub kokku vastava antigeeniga, tekivad ema veres selle vastu antikehad ning need võivad järgmise raseduse korral põhjustada lootel eluohtlikke probleeme. Kui testiga tuvastatakse reesusnegatiivsel emal reesuspositiivne loode, saab anti-D immunoglobuliini süstimise abil hoida ära ema organismi tundlikuks muutumise ehk antikehade tekke reesusantigeeni suhtes. Kui ema organism on juba varem reesusantigeeniga kokku puutunud ja tundlik selle suhtes jälgitakse raseduse kulgu enam ning vajadusel tehakse lootele emakasisene vereülekanne. [25]
Eetilised probleemid[muuda | muuda lähteteksti]
Selliste testide väljatöötamise ja patsientidele kättesaadavaks tegemisega tekib mitmeid eetilisi küsitavusi, mille võib jagada kolmeks suuremaks valdkonnaks.
- Mida peaks üldse testima ning millisest piirist muutub haiguste vältimine juba eugeenikaks? Kui paljude erinevate markerite määramist võiks üks test sisaldada ning kas need markerid peaksid tuvastama vaid juba teadaolevate põhjustega häireid või tuleks tuvastada kõik võimalikud kõrvalekalded loote genoomis?
- Kui palju infot tuleks patsiendile anda, et tema nõusolek testis osalemiseks oleks tõeliselt informeeritud? Kui patsiendil viiakse läbi invasiivne uuring, eelneb sellele alati geneetiku konsultatsioon ja põhjalik nõustamine. Vereproovide analüüsile tavaliselt seda ei eelne. Seetõttu tuleks kindlasti selliste testide pakkumisel ka testide olemust piisavalt selgitada.
- Kuidas nõustada patsienti testi tulemuste osas? Kui testis analüüsitakse ka SNP esinemist lootel, võib sageli juhtuda, et konkreetsete lootel esinevate SNP-de efekt pole tegelikult täpselt teada. Lisaks esineb tänapäeval pakutavate mitteinvasiivsete testide puhul siiski ka võimalus valepositiivsete või valenegatiivsete tulemuste saamiseks.
Erinevate geneetiliste häirete kandjaid ühendavad grupid on tõstatanud küsimuse juba olemasolevate haigete hoolduse ja tugisüsteemide kvaliteedi kohta. Eelkõige tuntakse muret selle pärast, et kui tulevikus on võimalik välistada nende häirete esinemine täielikult, siis väheneb ka nende uurimine ning juba olemasolevatele haigetele ei pakuta enam niivõrd kvaliteetset hooldust.[18]
Vaata ka[muuda | muuda lähteteksti]
Viited[muuda | muuda lähteteksti]
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 1,7 1,8 Chiu, R. W. K, Lo, Y. M. D. (2011). Non-invasive prenatal diagnosis by fetal nucleic acid analysis in maternal plasma: the coming of age. Semin. Fetal. Neonat. M. 16: 88–93
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 2,7 Go, A. T. J. I, van Vugt, J. M. G. Oudejans, C. B. M. (2011). Non-invasive aneuploidy detection using free fetal DNA and RNA in maternal plasma: recent progress and future possibilities. Hum. Reprod. Update. Vol. 17, No.3: 372 – 382
- ↑ Ustav, E.L., Asser, K., Haldre, K., Muru, K., Ridnõi, K., Buts, K., Rajasalu, L., Reimand, T. (2016). SÜNNIEELSE DIAGNOSTIKA JUHEND:LOOTE KROMOSOOMHAIGUSTE SÕELUURIMINE JA DIAGNOOSIMINE. LOOTE ULTRAHELIUURINGUD. Ravijuhend.
- ↑ Russo, Melissa L.; Blakemore, Karin J. (juuni 2014). "A historical and practical review of first trimester aneuploidy screening". Seminars in Fetal and Neonatal Medicine. 19 (3): 183–187. DOI:10.1016/j.siny.2013.11.013. ISSN 1744-165X.
- ↑ 5,0 5,1 Bianchi, Diana W.; Parker, R. Lamar; Wentworth, Jeffrey; Madankumar, Rajeevi; Saffer, Craig; Das, Anita F.; Craig, Joseph A.; Chudova, Darya I.; Devers, Patricia L.; Jones, Keith W.; Oliver, Kelly; Rava, Richard P.; Sehnert, Amy J. (27. veebruar 2014). "DNA Sequencing versus Standard Prenatal Aneuploidy Screening". New England Journal of Medicine (inglise). 370 (9): 799–808. DOI:10.1056/NEJMoa1311037. ISSN 0028-4793.
- ↑ Lo, Y M Dennis; Corbetta, Noemi; Chamberlain, Paul F; Rai, Vik; Sargent, Ian L; Redman, Christopher WG; Wainscoat, James S (1997). "Presence of fetal DNA in maternal plasma and serum". The Lancet (inglise). 350 (9076): 485–487. DOI:10.1016/S0140-6736(97)02174-0.
- ↑ 7,0 7,1 "Types of NIPT Technology | Whole-genome sequencing vs targeted". emea.illumina.com (inglise). Vaadatud 19. aprillil 2024.
- ↑ van Prooyen Schuurman, Lisanne; Sistermans, Erik A.; Van Opstal, Diane; Henneman, Lidewij; Bekker, Mireille N.; Bax, Caroline J.; Pieters, Mijntje J.; Bouman, Katelijne; de Munnik, Sonja; den Hollander, Nicolette S.; Diderich, Karin E.M.; Faas, Brigitte H.W.; Feenstra, Ilse; Go, Attie T.J.I.; Hoffer, Mariëtte J.V. (2022). "Clinical impact of additional findings detected by genome-wide non-invasive prenatal testing: Follow-up results of the TRIDENT-2 study". The American Journal of Human Genetics. 109 (6): 1140–1152. DOI:10.1016/j.ajhg.2022.04.018. ISSN 0002-9297. PMC 9247828. PMID 35659929.
{{ajakirjaviide}}: CS1 hooldus: PMC vormistus (link) - ↑ Juul, Laura A.; Hartwig, Tanja S.; Ambye, Louise; Sørensen, Steen; Jørgensen, Finn S. (2020). "Noninvasive prenatal testing and maternal obesity: A review". Acta Obstetricia et Gynecologica Scandinavica (inglise). 99 (6): 744–750. DOI:10.1111/aogs.13848. ISSN 0001-6349.
- ↑ Heesterbeek, Catharina J.; Aukema, Sietse M.; Galjaard, Robert-Jan H.; Boon, Elles M.J.; Srebniak, Malgorzata I.; Bouman, Katelijne; Faas, Brigitte H.W.; Govaerts, Lutgarde C.P.; Hoffer, Mariëtte J.V.; den Hollander, Nicolette S.; Lichtenbelt, Klaske D.; van Maarle, Merel C.; van Prooyen Schuurman, Lisanne; van Rij, Maartje C.; Schuring-Blom, G. Heleen (1. august 2022). "Noninvasive Prenatal Test Results Indicative of Maternal Malignancies: A Nationwide Genetic and Clinical Follow-Up Study". Journal of Clinical Oncology. 40 (22): 2426–2435. DOI:10.1200/jco.21.02260. ISSN 0732-183X.
- ↑ Levy, Brynn; Hoffmann, Eva R.; McCoy, Rajiv C.; Grati, Francesca R. (2021). "Chromosomal mosaicism: Origins and clinical implications in preimplantation and prenatal diagnosis". Prenatal Diagnosis (inglise). 41 (5): 631–641. DOI:10.1002/pd.5931. ISSN 0197-3851. PMC 8176867. PMID 33720449.
{{ajakirjaviide}}: CS1 hooldus: PMC vormistus (link) - ↑ Malvestiti, Francesca; Agrati, Cristina; Grimi, Beatrice; Pompilii, Eva; Izzi, Claudia; Martinoni, Lorenza; Gaetani, Elisa; Liuti, Maria Rosaria; Trotta, Anna; Maggi, Federico; Simoni, Giuseppe; Grati, Francesca Romana (2015). "Interpreting mosaicism in chorionic villi: results of a monocentric series of 1001 mosaics in chorionic villi with follow-up amniocentesis: Interpreting mosaicism in chorionic villi". Prenatal Diagnosis (inglise). 35 (11): 1117–1127. DOI:10.1002/pd.4656.
- ↑ Heinaru, A., 2012. Kromosoomide organisatsioon ja geeniekspressioon, p. 476 – 488. In Heinaru, A., Geneetika, Tartu Ülikooli Kirjastus
- ↑ "Haigekassa hakkas rahastama NIPT testi | Tervisekassa". www.tervisekassa.ee. 10. jaanuar 2020. Vaadatud 19. aprillil 2024.
- ↑ 15,0 15,1 15,2 "Arhiivikoopia". Originaali arhiivikoopia seisuga 22. märts 2014. Vaadatud 28. septembril 2014.
{{netiviide}}: CS1 hooldus: arhiivikoopia kasutusel pealkirjana (link) - ↑ "Non-Invasive Prenatal Test free for all women in the Netherlands". www.amsterdamumc.org (Ameerika inglise). 6. aprill 2023. Vaadatud 19. aprillil 2024.
- ↑ 17,0 17,1 Jayashankar, Siva Shantini; Nasaruddin, Muhammad Luqman; Hassan, Muhammad Faiz; Dasrilsyah, Rima Anggrena; Shafiee, Mohamad Nasir; Ismail, Noor Akmal Shareela; Alias, Ekram (2. august 2023). "Non-Invasive Prenatal Testing (NIPT): Reliability, Challenges, and Future Directions". Diagnostics (inglise). 13 (15): 2570. DOI:10.3390/diagnostics13152570. ISSN 2075-4418. PMC 10417786. PMID 37568933.
{{ajakirjaviide}}: CS1 hooldus: PMC vormistus (link) - ↑ 18,0 18,1 Malorye, A. (2013). Genomic testing reaches into the womb. Nat. Biotechnol. Vol. 31, No. 7:595 – 601
- ↑ Mazloom, A.R. et al (2013). Noninvasive prenatal detection of sex chromosomal aneuploidies by sequencing circulating cell-free DNA from maternal plasma. Prenat. Diagn. Jun;33(6):591-7
- ↑ "NIFTY by GenePlanet". nipt-geneplanet.com. Vaadatud 19. aprillil 2024.
- ↑ "NIPTIFY • Complete Genome NIPT". NIPTIFY (Ameerika inglise). Vaadatud 19. aprillil 2024.
- ↑ "Panorama test". Kliinik Elite. Vaadatud 19. aprillil 2024.
- ↑ "Vistara Overview". Natera (Ameerika inglise). Vaadatud 19. aprillil 2024.
- ↑ "VERAgene | Non Invasive Prenatal Testing | Peek A Baby" (Briti inglise). Vaadatud 19. aprillil 2024.
- ↑ "Arhiivikoopia". Originaali arhiivikoopia seisuga 10. oktoober 2014. Vaadatud 2. oktoobril 2014.
{{netiviide}}: CS1 hooldus: arhiivikoopia kasutusel pealkirjana (link)
Viitamistõrge: <references>-siltide vahel olevat <ref>-silti nimega "itk" ei kasutata eelnevas tekstis.
<references>-siltide vahel olevat <ref>-silti nimega "“tervelaps”" ei kasutata eelnevas tekstis.
