Cis-trans-isomeeria: erinevus redaktsioonide vahel
P r2.7.3) (Robot: lisatud fr:Isomérie cis-trans |
Resümee puudub |
||
| 2. rida: | 2. rida: | ||
[[Pilt:Cis-2-butene.PNG|right|frame|''cis''-2-buteen ehk Z-buteen]] [[Pilt:Trans-2-butene.PNG|right|frame|''trans''-2-buteen ehk E-buteen]] |
[[Pilt:Cis-2-butene.PNG|right|frame|''cis''-2-buteen ehk Z-buteen]] [[Pilt:Trans-2-butene.PNG|right|frame|''trans''-2-buteen ehk E-buteen]] |
||
''''' |
[[orgaaniline keemia|Orgaanilises keemias]] on '''''cis''-''trans''-isomeeria''' (ehk '''tsiss-trans-isomeeria''' ehk '''geomeetriline isomeeria''') [[stereoisomeeria]] vorm, mis johtub aatomite või aatomirühmade asetusest molekulis sisalduva kaksiksideme või tsüklitasandi suhtes. Seega on tegu kaksiksideme või tsükli süsinikuaatomitega seotud asendusrühmade üksteise suhtes ruumilise paiknemise erinevustega cis- ja trans isomeeri korral. Seejuures cis tähendab, et asendusrühmad on kaksiksideme või alitsüklilise ringi „samal pool” ja trans tähendab „vastaspooltel”. Ka anorgaaniliste kompleksühendite korral esineb cis-trans-isomeeria. |
||
cis ja trans deskriptorite kasutamine on ülevaatlik ja selge lihtsamate (kahe asendusrühmaga) ühendite korral. Kui kaksiksideme või tsükliga on seotud mitu erinevat asendusrühma, siis nende täpsemaks määratlemiseks kasutatakse deskriptoreid E (saksa entgegen) ja Z (saksa zusammen). Seejuures võrreldakse asendusrühmade vanemust: kui kaks kõige vanemat rühma on samal pool võrdlustasandit, siis on tegemist Z-isomeeriga, kui eri pooltel, siis E-isomeeriga. Paljude lihtsamate ühendite korral on kokkulangevad cis- ja Z-isomeer ning trans- ja E-isomeer. |
|||
''Cis''-''trans''-isomeerias on kaks isomeeri vormi: ''cis'' ja ''trans''. Kui asendusrühmad on orienteeritud mõlemad samas suunas, siis on tegemist ''cis'' vormiga. Kui asendusrühmad on orienteeritud aga vastassuundades, siis on tegemist ''trans'' vormiga. |
|||
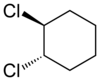
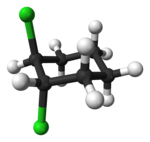
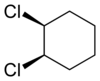
Ka tsükliliste ühendite puhul on ''cis''-''trans''-isomeeria võimalik. Juhul kui mõlemad asendusrühmad asuvad tsükli tasandi ühel poolel on tegemist ''cis'' vormiga. Kui asendusrühmad on aga tsükli tasandi erinevatel pooltel on tegu ''trans'' vormiga. |
|||
{| class="wikitable" style="margin: 1em auto 1em auto" |
{| class="wikitable" style="margin: 1em auto 1em auto" |
||
| 14. rida: | 12. rida: | ||
| ''cis''-1,2-dikloroheksaan || ''trans''-1,2-dikloroheksaan |
| ''cis''-1,2-dikloroheksaan || ''trans''-1,2-dikloroheksaan |
||
|} |
|} |
||
cis-trans-isomeeria tuleneb asjaolust, et molekulis nii kaksiksideme kui ka tsükliga kaasneb nendega seotud asendusrühmade ruumis vaba pöörlemise takistus, mis hoiab need rühmad üksteise suhtes fikseerituna. |
|||
cis- ja trans-isomeerid enamasti mingil määral erinevad oma füüsikalistelt ja keemilistelt omadustelt. Paljudel juhtudel on trans-isomeer stabiilsem kui cis. |
|||
==Vaata ka== |
|||
*[[Stereoisomerism]] |
|||
*[[Alkeenid]] |
|||
*[[Alitsülkilised ühendid]] |
|||
[[Kategooria:Orgaaniline keemia]] |
[[Kategooria:Orgaaniline keemia]] |
||
Redaktsioon: 22. oktoober 2012, kell 09:23
See artikkel vajab toimetamist. (Mai 2008) |
See artikkel ootab keeletoimetamist. |
Orgaanilises keemias on cis-trans-isomeeria (ehk tsiss-trans-isomeeria ehk geomeetriline isomeeria) stereoisomeeria vorm, mis johtub aatomite või aatomirühmade asetusest molekulis sisalduva kaksiksideme või tsüklitasandi suhtes. Seega on tegu kaksiksideme või tsükli süsinikuaatomitega seotud asendusrühmade üksteise suhtes ruumilise paiknemise erinevustega cis- ja trans isomeeri korral. Seejuures cis tähendab, et asendusrühmad on kaksiksideme või alitsüklilise ringi „samal pool” ja trans tähendab „vastaspooltel”. Ka anorgaaniliste kompleksühendite korral esineb cis-trans-isomeeria.
cis ja trans deskriptorite kasutamine on ülevaatlik ja selge lihtsamate (kahe asendusrühmaga) ühendite korral. Kui kaksiksideme või tsükliga on seotud mitu erinevat asendusrühma, siis nende täpsemaks määratlemiseks kasutatakse deskriptoreid E (saksa entgegen) ja Z (saksa zusammen). Seejuures võrreldakse asendusrühmade vanemust: kui kaks kõige vanemat rühma on samal pool võrdlustasandit, siis on tegemist Z-isomeeriga, kui eri pooltel, siis E-isomeeriga. Paljude lihtsamate ühendite korral on kokkulangevad cis- ja Z-isomeer ning trans- ja E-isomeer.
  |
|
| cis-1,2-dikloroheksaan | trans-1,2-dikloroheksaan |
cis-trans-isomeeria tuleneb asjaolust, et molekulis nii kaksiksideme kui ka tsükliga kaasneb nendega seotud asendusrühmade ruumis vaba pöörlemise takistus, mis hoiab need rühmad üksteise suhtes fikseerituna.
cis- ja trans-isomeerid enamasti mingil määral erinevad oma füüsikalistelt ja keemilistelt omadustelt. Paljudel juhtudel on trans-isomeer stabiilsem kui cis.