Hessi seadus
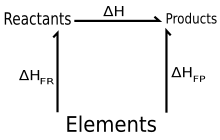
Hessi seadus on füüsikalise keemia põhiseadus, mille kohaselt keemilise reaktsiooni soojusefekt sõltub ainult süsteemi alg- ja lõppolekust, mitte reaktsiooni käigust (vahestaadiumidest).
Teiste sõnadega, Hessi seadus väidab, et mitmes staadiumis toimuva reaktsiooni korral kogu protsessi entalpia muutus (tähistatakse ΔH) on reaktsiooni vaheetappide entalpia muutuste summa (eeldusel, et füüsikalised tingimused lähte- ja lõppolekul on samad).
Hessi seadus on energia jäävuse seaduse erijuhtum keemiliste protsesside korral. See seadus võimaldab arvutada reaktsioonide soojusefekte, mis ei ole otseselt määratavad. Nimetatud seaduse avaldas Germain Hess 1840. a.
