Peptiidisünteesi aktivaatorid
Peptiidisünteesi aktivaatorid on ained, mida kasutatakse karboksüülrühma aktiveerimiseks. Karboksüülrühm muudetakse keemiliselt aktiivseks estriks, atsüülkloriidiks, asiidiks, anhüdriidiks vms ühendiks, mis aitab reaktsiooni läbi viia. Selleks seotakse omavahel ühe aminohappe karboksüülrühm ja teise aminohappe aminorühm, et tekiks peptiidside ehk amiidside.[1]
Peptiidisünteesi kiire, tõhus, suure saagisega ja väheste kõrvalsaadustega läbiviimine sõltub kaitserühma ja aktivaatori omavahelisest õigest kombineerimisest ning mitmest muust tegurist. Selles reaktsioonis on oluline, et tekiks hea lahkuv rühm.
Tahke faasi peptiidisünteesil kasutatavaid aktivaatoreid on välja töötatud lugematu hulk. Uusi aktivaatoreid sünteesitakse ja arendatakse pidevalt ning iga aktivaator on erinevate omadustega. Ei ole aktivaatorit, mis annaks väga häid tulemusi kõikide aminohappe derivaatidega reageerides, igal on eelised ja puudused.
Enim levinud ja enim kasutatavad aktivaatorid on: karbodiimiidid, fosfooniumi reagendid ja amiiniumi/urooniumi reagendid. Lisaks kasutatakse peptiidisünteesis lisaaineid nagu triasoolid ja oksüma (Oxyma Pure) lisandid ja alused.[1]
Karbodiimiidid[muuda | muuda lähteteksti]
Karbodiimiide on peptiidisünteesis kasutatud juba aastakümneid, sest reaktsioon on üldjuhul kiire ja annab keskmisi saagiseid. Karbodiimiidide korral tekib vaheprodukt O-atsüül isouurea, mida võib vaadelda ka kui karboksüülestri aktiveeritud lahkuvat rühma. Tekkinud vaheprodukt reageerib amiiniga, tekitades soovitud peptiidsideme. Karbodiimiidide kasutamisel tekivad kõrvalproduktid. Lisaks sellele on diimiidide kasutamine raskendatud nende mürgisuse, kantserogeensuse ja suure niiskustundlikkuse tõttu. Selle tõttu on eelaktivatsiooni ajal vajalik kasutada inertgaasi atmosfääri, mis aitab vältida diimiidi hüdrolüüsi õhuniiskuse toimel. Karbodiimiidide hulka kuuluvad näiteks DCC ja DIC. DCC-d ehk ditsükloheksüülkarbodiimiidi on kasutatud aktivaatorina juba 1955. aastast ja kasutatakse ka tänapäeval.[2][3][4]
Paraku tekib DCC-ga peptiidisünteesi tahke faas palju kõrvalsaadust DCU (ditsükloheksüüluurea), mis langetab reaktsiooni saagist. Lisaks ei ole see lisaprodukt reaktsioonisegust väga lihtsasti eemaldatav, seega otsitakse sellele alternatiive.
DIC-d ehk diisopropüülkarbodiimiidi on lihtsam käsitseda kui DCC-d, sest tegemist on vedelikuga. Lisaks lahustub DIC enamikus orgaanilistes lahustes, seega hiljem on seda reaktsioonisegust kergem eemaldada.[5][6]
Kuigi karbodiimiidid on peptiidisünteesis head aktivaatorid, on neil mitmeid miinuseid. Lisaks kõrvalproduktide tekkele on karbodiimiidide liiga suure reaktsioonivõimekuse põhiliseks probleemiks ka ratsemisatsioon. Seega on saaduseks tihti ratseemilised segud. Selleks, et karbodiimiidide reaktsioonil peptiidide ratsemisatsiooni vähendada, said need lisaained.
-
DCC struktuurivalem
-
DIC struktuurivalem
Lisaained triasoolid ja oksüma[muuda | muuda lähteteksti]

Epimerisatsiooni vähendamiseks tutvustasid W. Koenig ja R. Grieger HOBt-i (1-hüdroküsü-1-H-bensotriasool) kui lisaainet, millega kasvas ka produkti saagis.[7][8] HOBt ja HOAt (1-hüdroksü-7-asobensotriasool) annavad karbodiimiidi reaktsioonil tekkinud O-atsüüli isouureaga reageerides Obt või OAt aktiivestri, mis suurendab reaktiivsus võimet. Triasoolid HOBt ja HOAt on enamasti hüdraatkujul. Nende reaktsioonimehhanism ja -võimelisus on sarnased. Mitmed fosfooniumi ja urooniumi/amiiniumi soolad sisaldavad lahkuva rühmana HOBt-i või HOAt-d. Aktivaatorite väljatöötamine põhinebki hea lahkuva rühma ja karbokatiooni kombineerimisel. Oksümarühm (Oxyma Pure) on lisaainetest üks uuemaid reagente, hea reaktsioonivõimekusega ja lisaks ka hinnalt soodne. Kuna viimasel ajal on triasoole peetud teatud tingimustel plahvatusohtlikeks, on oksüma HOBt-i ja HOAt-i asendamiseks sobiv alternatiiv. Oksümat kombineeritakse samamoodi aktivaatorite väljatöötamisel, kasutades seda lahkuva rühmana.[1]

Alused[muuda | muuda lähteteksti]
Reaktsiooni paremaks ja kiiremaks läbiviimiseks kasutatakse aluseid nagu DIPEA (diisopropüülamiin), NMM (N-metüülmorfoliin) ja kollidiin. DIPEA on amiin, mida orgaanilises keemias kasutatakse alusena. Aine struktuur (lämmastik, mis on seotud kahte isopropüül- ja etüüliga) on selline, et ainult vesinik on piisavalt väike sinna mahtumiseks ehk sellega reageerimiseks. DIPEA on tugev alus, aga nõrk nukleofiil. Peale peptiidisünteesi kasutatakse seda ka sekundaarsetest amiinidest tertsiaarsete amiinide saamiseks.[1]
Amiiniumi/urooniumi soolad[muuda | muuda lähteteksti]
Amiiniumi/urooniumi soolad on tihti kombineeritud triasoolidega ja viimasel ajal ka oksümaga. Urooniumi ja amiiniumi isomeerid on struktuurselt identifitseeritud ning nende vorm sõltub vastavast solvendist, isolatsioonimeetodist ja lahkuvast rühmast. Urooniumi vorm on O-vorm ja amiinium on N-vorm. Eelistatud on O-vorm, mis on reaktsioonivõimelisem. Üldjuhul tekivad reaktsioonis alati mõlemad vormid. Enim levinud amiiniumi/urooniumi soolad on näiteks TBTU, HCTU, HATU, HDMC, COMU.
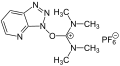
HATU ehk 1-[bis(dimetüülamino)metüleen]-1H-1,2,3-triasoolo[4,5-b]püridiinium 3-oksiid heksafluorofosfaat – on sidestumisreagent, mida kasutatakse peptiidsünteesi keemias karboksüülhappest aktiivse estri saamiseks. Sellega koos kasutatakse DIPEA-d peptiidsidemete moodustamiseks.
HBTU ehk O-(Bensotriasool-1-ül)-N,N,N’,N’-tetrametüüluroonium heksafluorofosfaat ja TBTU ehk 2-(1H-Bensotriasooll-1-ül)-1,1,3,3-tetrametüülamiinium tetrafluoroboraat erinevad teineteisest vaid aktivaatori vastasiooni poolest (BF4-, PF6-). Neil on sarnased keemilised omadused. Kõik tekkivad kõrvalproduktid on vees või põhilistes orgaanilistes lahustes lahustuvad, seega kergesti eemaldatavad. See tähendab head vastupidavust ratsemisatsioonile. Seda kasutatakse selle kerge aktivatsiooni omaduste pärast.
HCTU ehk O-(1H-6-klorobensotriasool-1-ül)-1,1,3,3-tetrametüüluroonium heksafluorofosfaat on mittetoksiline, mitteärritatav ja mittekorrodeeritav ühend, mida kasutatakse peptiidisünteesis. HOBt-i rühma asendamine 6-kloro-HOBt-iga viib raskete peptiidide sünteesimisel suurema reaktsioonimäärani ning täiustatud tulemusteni. HCTU efektiivsus on võrdne HATU omaga ja HCTU-ga saab puhtamat peptiidi kui HBTU, PyBOP ja TBTU-ga.[9]
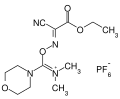
COMU (1-tsüano-2-etoksü-2-oksoetüülideenaminooksü)dimetüülamino-morfolino-karbeenium heksafluorofosfaat) karbokatiooniks on morfoliinorühm ja lahkuvaks rühmaks on oksüma. Tegemist on n-ö kolmanda generatsiooni uroonium-tüüpi aktivaatoriga, mille korral tekib vaid O-vorm ja N-vorm ei teki[10]. Lisaks heale lahkuvale rühmale on head omadused ka morfoliinirühmal, mis tõstavad aine lahustuvust, stabiilsust ja reaktsioonivõimet. Lisaks sellele on väike ratsemisatsioonivõimelisus. Ka tekkivad kõrvalproduktid on kergesti eemaldatavad.
-
HATU struktuurivalem
-
HBTU struktuurivalem
-
HCTU struktuurivalem
-
COMU struktuurivalem
Fosfooniumsoolad[muuda | muuda lähteteksti]
Fosfooniumsoolade karbokatioonid sisaldavad fosforit, sellest ka nimetus. Nende eeliseks on, et kõrvalproduktina ei teki guanidiiniumi.
PyBOP ehk bensotriasool-1-ül-oksü-tris-pürrolidino-fosfoonium heksafluorofosfaat on vajalik BOP-i reagenti asendamiseks, et vältida kantserogeensete kõrvalproduktide tekkimist.
PyOxim ehk [etüültsüano(hüdroksüimiino)atsetaat-O2]tri-1-pürrolidinüülfosfoonium heksafluorofosfaat on hiljuti arendatud sidestumisreagent, milles asendati plahvatusohtlik HOBt-i rühm oksümarühmaga. See parandus teeb käsitlemise ohutumaks, suurendab reaktsioonivõimelisust ning vähendab võimalikke allergiaid. See on potentsiaal, mis teeb PyOxim-i üheks kõige paremaks sidestumisreagentiks tahkefaasilise sünteesi jaoks. Ainsaks puuduseks on kõrvalreaktsioon, mille käigus tekib tris-pürrolidinofosfamiid, mis võib tekitada probleeme aine eraldamisel või puhastamisel.
PyClock ehk 6-kloro-bensotriasool-1-üloksü-tris-pürrolidinofosfoonium heksafluorofosfaat on 6-kloro PyBOP-i analoog. See on suurepärane sidestumisreaktsiooni aktivaator, kui reaktsioon on pikatoimeline (nt tsükleerimine). Selle reaktsiooniga saadud aktiivestrid on reaktsioonivõimelisemad kui need, mis on saadud PyBOP-iga või HBTU-ga.[1]
-
PyOxim-i struktuurivalem
-
PyBOP-i struktuurivalem
Viited[muuda | muuda lähteteksti]
- ↑ 1,0 1,1 1,2 1,3 1,4 Coupling reagents and additives offered by BACHEM, Global Marketing, Bachem Group, November 2015
- ↑ J. C. Sheehan and G. P. Hess, J. Am. Chem.Soc. 77, 1067 (1955)
- ↑ G. W. Anderson and F. M. Callahan, J. Am. Chem. Soc. 80, 2902 (1958)
- ↑ I.Schon and L.Kisfaludy, Synthesis 303 (1986).
- ↑ A. Williams and I. T. Ibrahim, Chem. Rev. 81,589 (1981)
- ↑ L. A. Carpino, A. El-Faham, Tetrahedron 55,6813 (1999)
- ↑ W. Konig and R. Geiger, Chem. Ber. 103, 788 (1970)
- ↑ W. Konig and R. Geiger, Chem. Ber. 103, 2024 (1970)
- ↑ Journal of Peptide Science J. Pept. Sci. 2008; 14: 97–101
- ↑ Ayman El-Faham and Fernando Albericio (2010), COMU: A third generation of uronium-type coupling reagents, Volume 16 (1), p 6–9, Journal of Peptide Science