Orgaanilised pooljuhid
Orgaanilised pooljuhid on pooljuhi omadustega orgaanilised materjalid. Juhtivad võivad olla nii üksikud molekulid, oligomeerid kui polümeerid. Et polümeerid elektrit juhiksid, peavad elektronid saama vabalt liikuda, s.t olema nõrgalt seotud konkreetsete aatomitega. Sellist olukorda võimaldavad saavutada konjugeerunud sidemed.
Niisuguste ainete hulka kuuluvad näiteks polüatsetüleen, polü(p-fenüleenvinüleen) (PPV) ja rubreen. Orgaaniliste polümeeride elektrijuhtivust saab mõjutada dopeerimisega.
Orgaanilisi polümeere kasutatakse valgusdioodides (OLED), päikesepaneelides, pinnakatetes jm rakendustes.
Ajalugu[muuda | muuda lähteteksti]
20. sajandi keskel leiutatud transistori tulekuga hakkasid pooljuhid germaanium ja räni elektroonikas domineerima seni kasutatud metallide üle. Samal ajal toimus areng elektrovaakumseadiseid (elektronlampi, elektronkiiretoru) kasutavast elektroonikast pooljuhtseadistele (diood, transistor). Tänu sellele muutusele on pooljuhttehnoloogia jõudnud kõikjal inimeste igapäevaellu. 21. sajandi alguses hakkas hoogsalt arenema ka orgaaniliste pooljuhtide tehnoloogia.
Orgaaniliste pooljuhtide uurimine algas juba 20. sajandi alguses, kui uuriti antratseenkristallide fotojuhtivust. Tegu oli orgaaniliste pooljuhtide prototüübiga. Siiski ei suudetud neis rakendustes saavutada kuigi suurt voolutihedust, valguse genereerimist ega seadise stabiilsust. Põhilisteks probleemideks olid kõrge tööpinge vajadus, mis tulenes kristalli paksusest (mõni mikromeeter kuni mõni millimeeter), suutmatusest kristalle suuremates kogustes valmistada ning ebaefektiivsetest kontaktidest.
1970ndatel edukalt sünteesitud ja dopeeritud konjugeeritud polümeerid tähistasid uue orgaaniliste polümeeride klassi sündi. Selle eest saadi 2000. aastal ka Nobeli keemiaauhinna. Koos orgaaniliste fotojuhtidega (molekulaarselt dopeeritud polümeerid) olid need juhtivpolümeerid esimesed juhtivad pinnakatted orgaanilistest materjalidest.
Huvi mittedopeeritud orgaaniliste pooljuhtide vastu elavnes 1980ndatel. Põhjuseks oli efektiivse orgaanilist p- ja n-juhtivate materjalide liitekohta omava fotoelemendi demonstratsioon. Lisaks ajendas uurimistööd ka esimese konjugeeritud polümeeridest ja oligomeeridest valmistatud õhukese kiletransistori valmistamine. Peapõhjuseks oli aga kõrge efektiivsusega molekulaarkiledest ja konjugeeritud polümeeridest elektroluminestsentsdioodide esitlemine.
Tänapäeval on OLEDide tehnoloogia kiiresti arenemas ning neile on lisandunud ka orgaanilised väljatransistorid (OFET).[1]
Materjalid[muuda | muuda lähteteksti]
Orgaanilised pooljuhid jagunevad kahte gruppi: väikese molekulmassiga materjalid ja polümeerid. Mõlemal on sarnased pz-orbitaalidest moodustunud konjugeeritud π-elektronsüsteemid. Võrreldes σ-sidemetega, mis hoiavad suuremalt jaolt molekuli koos, on π-sidemed palju nõrgemad. Selle tõttu toimuvad madalaimad elektronergastused konjugeeritud molekulides π-π*-siiretes. Keelutsoon jääb tüüpiliselt 1,5 ja 3 eV vahele, mille juures on võimalik valguse kiirgumine ja neeldumiseni nähtavas spektris. Keelutsooni suurust saab juhtida konjugeeritusega.[1]
| Nimetus | Molekuli valem |
Lülide arv |
Molaarmass | CAS number | Struktuur |
|---|---|---|---|---|---|
| Benseen | C6H6 | 1 | 78,11 g/mol | 71-43-2 | 
|
| Nafteleen | C10H8 | 2 | 128,17 g/mol | 91-20-3 | 
|
| Antratseen | C14H10 | 3 | 178,23 g/mol | 120-12-7 | 
|
| Tetratseen | C18H12 | 4 | 228,29 g/mol | 92-24-0 | 
|
| Pentatseen | C22H14 | 5 | 278,35 g/mol | 135-48-8 | 
|
| Heksatseen | C26H16 | 6 | 328,41 g/mol | 258-31-1 | 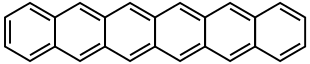
|
| Heptatseen | C30H18 | 7 | 378,46 g/mol | 258-38-8 | 
|
Taoliste molekulide keemiline manipuleerimine loob mitmeid võimalusi, et mõjutada orgaaniliste pooljuhtmaterjalide optoelektroonilisi omadusi.[1]
Oluline erinevus eelmainitud kahe klassi vahel seisneb nendest õhukeste kilede valmistamise tehnoloogias. Väikeseid molekule sadestatakse pinnale gaasifaasist sublimatsiooni või aurustamise teel. Konjugeeritud molekulidest valmistatakse kilesid aga lahusest vurrkatmise või printimistehnikatega.[1][2]

Põhilised omadused[muuda | muuda lähteteksti]
Orgaaniliste pooljuhtide ehitus on anorgaaniliste pooljuhtide omast fundamentaalselt erinev. Orgaaniliste molekulaarkristallide vahel mõjuvad van der Waalsi jõud. Selle tõttu on jõud orgaaniliste kristallide vahel palju nõrgemad kui kovalentseid jõude omavates, Si- või GaAs-kristallides. Sellest tuleneb näiteks orgaaniliste pooljuhtide väiksem kõvadus ja madalam sulamistemperatuur. Vast kõige tähtsam erinevus seisneb aga elektroonsete lainefunktsioonide nõrgemas delokaliseerumises, millel on otsene mõju optilistele ja laengusidestusomadustele.[1]
Optilised omadused[muuda | muuda lähteteksti]
Tänu nõrgale elektroonsele delokalisatsioonile, on orgaanilised pooljuhid anorgaanilistest pooljuhtidest erinevad kahel viisil. Orgaanilistes pooljuhtides esinevad kindlalt piiritletud spinnolekud (singlet ja triplet) nagu eraldiseisvates molekulides. See avaldab olulist mõju nende materjalide fotofüüsikale, ent seab ka piirangu OLEDide elektroluminestsentsi kvantefektiivsusele.
Teine tähtis orgaaniliste pooljuhtide omadus on see, et optilised eksitonid on harilikult lokaliseeritud ühte molekuli ja seega omavad seoseenergiat tüüpiliselt 0,5 ja 1 eV vahel. Seega tuleb fotoelementides see energia ületada enne positiivse ja negatiivse laengukandjate iseseisva paari tekitamist.[1]
Laengukandjate transport[muuda | muuda lähteteksti]
Rääkides laengukandjate liikumisest orgaanilistes pooljuhtides, tuleb arvesse võtta, et kirjeldatakse ioonseid molekulaarolekuid. Seega augu tekitamiseks, peab elektron olema eemaldatud neutraalsest molekulist M, et tekitada radikaalkatioon M+. See auk (defektelektron) saab liikuda ühelt molekulilt teisele.
Laengukandjate liikuvus sõltub suuresti orgaaniliste pooljuhtide puhtusastmest. Seetõttu pööratakse nende materjalide valmistamisel suurt tähelepanu ettevalmistusele ja kasvutingimustele.
Laengukandjate tiheduse suurendamiseks on mitmeid võimalusi:
- (elektro)keemiline dopeerimine
- kontaktidest laengukandjate juurdetoomine
- laengukandjate fotogenereerimine
- väljaefekti rakendamine dopeerimisel[1][3]
Rakendused[muuda | muuda lähteteksti]
OLED[muuda | muuda lähteteksti]
 Pikemalt artiklis Orgaaniline valgusdiood
Pikemalt artiklis Orgaaniline valgusdiood
OLED on valgusdiood, milles valgust kiirgab orgaanilise pooljuhi kiht. Orgaanilisi pooljuhte kasutatakse OLEDi katoodi ja anoodi vahelises kihis. Algupärased OLEDid kasutasid elektroodide vahel vaid ühte orgaanilise pooljuhi kihti. Efektiivsuse parandamiseks hakati kasutama mitut kihti. Praegusaegsetes OLEDides on elektroodide vahel kaks kihti: juhtiv ja kiirgav kiht. Harilikult on vähemalt üks elektroodidest läbipaistev.

Orgaaniline väljatransistor[muuda | muuda lähteteksti]
Orgaaniline väljatransistor (OFET) on väljatransistor, mille kanalis on orgaaniline juhtiv materjal. Harilikult valmistatakse niisuguseid transistore kas väikestest molekulidest vaakumaurustamisega, väikestest molekulidest ja polümeeridest lahuse vormi viimisega või õhukese monokristallilise kihi kandmisega alusele.

Vaata ka[muuda | muuda lähteteksti]
Viited[muuda | muuda lähteteksti]
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 Brütting, Wolfgang (2005). Physics of Organic Semiconductors. Winheim: Wiley-VCH Verlag GmbH & Co.
- ↑ "What are organic semiconductors". Organic Semiconductor World. 2015. Originaali arhiivikoopia seisuga 22.12.2015. Vaadatud 12.12.2015.
- ↑ Coropceanu, Veaceslav; Cornil, Jerome; da Silva Filho, Demetrio A.; Oliver, Yoann; Silbey, Robert; Bredas, Jean-Luc (2007). "Charge Transport in Organic Semiconductors" (PDF). Chem. Rev.: 926-952. Originaali (PDF) arhiivikoopia seisuga 2015-11-23. Vaadatud 2015.
{{cite journal}}: kontrolli kuupäeva väärtust:|accessdate=(juhend)
