Siirdeseisund: erinevus redaktsioonide vahel
Eemaldatud sisu Lisatud sisu
Resümee puudub |
PResümee puudub |
||
| 10. rida: | 10. rida: | ||
==Vaata ka== |
==Vaata ka== |
||
*[[Reaktsioonikoordinaat]] |
*[[Reaktsioonikoordinaat]] |
||
*[[Aktivatsioonienergia]] |
|||
[[Kategooria:Keemilised reaktsioonid]] |
[[Kategooria:Keemilised reaktsioonid]] |
||
Redaktsioon: 30. juuli 2014, kell 11:12
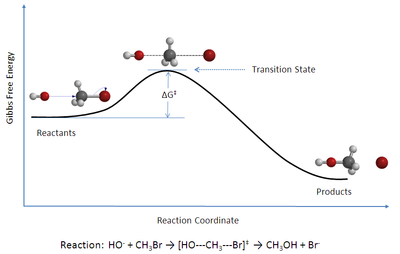

Siirdeseisund ehk siirdeolek on keemilises reaktsioonis reageerivate ainete aatomitevaheliste sidemete ja konfiguratsiooni teatud ümberkujunemine piki reaktsioonikoordinaati. See on lähteainete produktideks üleminekuseisund ja vastab süsteemi kõrgeimale energiale reaktsioonikoordinaadil, seega on tegu energeetilise barjääri ületamise momendiga.
Näide on kõrvaloleval skeemil: bromoetaani SN2 reaktsioon hüdroksiidiooniga; kandilistes sulgudes on kujutatud selle protsessi siirdeseisund.
Märkus. Siirdeseisund on põhimõtteliselt erinev intermediaadist: esimest iseloomustab reaktsioonikoordinaadil energia maksimum, teist mõningane energia miinimum.
