Alfaviirus
Alfaviirus (Alphavirus) on viiruste perekond sugukonnast Togaviridae (togaviirused). Alfaviirused kuuluvad vastavalt genoomistruktuuril põhinevale Baltimore'i klassifikatsioonisüsteemile IV rühma ja neil on üheahelaline positiivse polaarsusega RNA. Kokku on teada umbes 30 liiki alfaviirusi, mis nakatavad nii inimesi, suuremaid loomi (hobused), närilisi, linde, kalu kui ka selgrootuid. Alfaviiruste levimine liikide ja isendite vahel toimub peamiselt moskiitode abil, seetõttu kuuluvad nad arboviiruste (lülijalgsetega levivate viiruste) hulka. Alfaviirustel on ümbris, nad on kujult sfäärilised ja vähesel määral pleomorfsed. Virionide diameeter on umbes 70 nm, nukleokapsiid on 40 nm suurune ja isomeetriline. Partiklid on ikosaeedrilised, T=4-sümmeetriaga.
Genoom[muuda | muuda lähteteksti]
Alfaviiruste genoomiks on üheahelaline positiivse polaarsusega RNA molekul. Genoomi pikkus on umbes 11 000–12 000 nukleotiidi ja selle 5’ otsas on müts ning 3’ otsas polü(A)-saba. Alfaviiruste genoomis on kaks regiooni: mittestruktuurne ja struktuurne. Esimene asub 5'-otsas ja on umbes 7000 nukleotiidi pikk[1], seega võrdne genoomi kahe kolmandikuga. Sellest transleeritakse mittestruktuursete valkude prekursor (eelvalk) P1234, millest proteolüütilise töötluse teel moodustuvad mittestruktuursed valgud nsP1, nsP2, nsP3 ja nsP4. Need proteiinid on alfaviiruste transkriptsioonikompleksi põhilised komponendid, lisaks vastutavad need rakulise sünteesi pärssimise eest. Teine regioon on umbes 4000 nukleotiidi pikk[1] ning asub genoomi 3'-otsa-poolses kolmandikus. See on kollineaarne alfaviiruste subgenoomse RNA-ga, millest transleeritakse struktuursed proteiinid: nukleokapsiidivalk C, ümbrisevalk E1 ja prekursor P62.
Struktuursed valgud[muuda | muuda lähteteksti]
P62 eelvalgu proteolüütilise töötluse käigus moodustuvad valgud E2 ja E3. Koos E1-proteiiniga osalevad nad virioni pinna moodustamises. E1 ja E2 (mõnikord ka E3) glükoproteiinid on liitunud ogasarnasteks E1-E2-heterodimeerideks või E1-E2-E3-heterotrimeerideks, kus E2 on oga keskosas, E1 asub ogatippude vahel ja E3 (kui esineb) asub oga distaalses osas.[2] Need struktuurid paiknevad membraani lipiidses kaksikkihis. E2-glükoproteiin läbib membraankesta ning tema nukleokapsiidipoolne domeen interakteerub nukleokapsiidvalguga vahekorras üks ühele. E2 välisdomeeni ülesandeks on seonduda rakupinna retseptoritega. Rakku tungimisel stimuleerib alfaviirus endosoomi moodustumist, selle happelises keskkonnas E1 dissotsieerub E2-valgust ja moodustab E1-homotrimeeri. See struktuur mängib põhilist rolli rakumembraani ja viiruse membraani ühinemises. Alfaviiruste glükoproteiin E1 on II klassi viiruslik fusioonivalk ja see erineb struktuurselt I klassi fusioonivalkudest, mis leiduvad gripiviirustes ja HIV-is.[3] Perifeerne E3-glükoproteiin kaob enamikul alfaviirustest viiruspartiklite moodustumise käigus. Erandiks on Semliki metsa viirus, kus E3 jääb membraani koosseisu. Nukleokapsiid sisaldab 240 kapsiidvalgu koopiaid.
Mittestruktuursed valgud[muuda | muuda lähteteksti]
P1234 proteolüütilise töötluse käigus moodustuvad valgud nsP1, nsP2, nsP3 ja nsP4. Igal proteiinil on tsütoplasmas toimuvas viirusliku RNA transkriptsioonis ja rakulise sünteesi takistamises oma kindel ülesanne. nsP1 mängib rolli miinusahelalise RNA sünteesi algatamises ning on metüültransferaasse ja guanülüültransferaasse aktiivsusega. Tavaliselt on see seondunud raku sisemembraanidele. nsP2-valgul on RNA-helikaasne ja proteaasne toime. Põhiliselt paikneb see proteiin rakutuumas – seal asub umbes 50% kogu nsP2 hulgast. nsP3-valgu ülesandeid on veel vähe uuritud. Oletatakse, et selle C-domeen vastutab vektori ja peremeesraku äratundmise eest. nsP4-valgul on RNA-polümeraasne toime.[4][5]
Taksonoomia[muuda | muuda lähteteksti]
E1- ja E2-valgud on põhilised sihtmärgid mitmesugustes seroloogilistes reaktsioonides ja testides, näiteks neutralisatsioonireaktsioonis ja hemaglutinatsiooni pidurdusreaktsioonis, mida kasutatakse viiruse määramiseks. Seroloogiliselt on alfaviirustel suur antigeenne varieeruvus, mille alusel eristatakse seitset antigeenset kompleksi, 30 liiki ning mitmeid subtüüpe ja varieteete.
- Barmah Foresti viiruse kompleks
- Ida hobuste entsefaliidi kompleks
- Middelburgi viiruse kompleks
- Ndumu viiruse kompleks
- Semliki metsa viiruse kompleks
- Bebaru viirus
- Chikungunya viirus
- Mayaro viirus
- Subtüüp Una viirus
- O’nyong'nyongi viirus
- Subtüüp Igbo-Ora viirus
- Ross Riveri viirus
- Subtüüp Bebaru viirus
- Subtüüp Getahi viirus
- Subtüüp Sagiyama viirus
- Semliki metsa viirus
- Subtüüp Me Tri viirus
- Venezuela hobuste entsefaliidi kompleks
- Lääne hobuste entsefaliidi kompleks
- Rekombinantsed viirused
- Klassifitseerimata
- Lõheliste alfaviirus
- Rainbow trout sleeping disease'i viirus
- Lõuna-lonthüljeste viirus
- Tonate'i viirus
Märkused[muuda | muuda lähteteksti]
Alfaviiruste perekond tekkis Vanas Maailmas ja selle eelkäijateks olid taimeviirused, mille levik toimus lülijälgsete vahendusel.[6] Alfaviiruste lahknemine Uue ja Vana Maailma viirusteks toimus umbes 2000–3000 aastat tagasi.[7] Barmah Foresti viirus on Semliki metsa viirusega suguluses. Middelburgi viirus, mida klassifitseeritakse iseseisvaks kompleksiks, võib kuuluda Semliki metsa viiruse kompleksi. Venezuela hobuste entsefaliidiviiruse ja ida hobuste entsefaliidiviiruse omavaheline lahknemine toimus umbes 1400 aastat tagasi.[8] Sindbisi viirus, mis on pärit Lõuna-Ameerikast, on hobuste entsefaliidiviiruste sugulasliik.[9] Lõuna-lonthüljeste viirus on ilmselt Sindbisi viiruse klaadi sugulane. Kalade viirused moodustavad arvatavasti teistele alfaviiruste liikidele basaalse klaadi. Lääne hobuste entsefaliidiviirus on rekombinantne viirus, mis tekkis ida hobuste entsefaliidiviiruse ja Sindbisi viiruse rekombinatsiooni tulemusena. Sellel viirusel on Sindbisi viirusest pärit E1- ja E2-valgud ning geneetilised regioonid, mis vastavad ida hobuste entsefaliidiviirusele.[4]
Patogeensus ja immuunvastus[muuda | muuda lähteteksti]
| Viirus | Sümptomid inimestel | Selgroogsed peremehed | Regioon |
|---|---|---|---|
| Barmah Foresti viirus | Palavik, halb enesetunne, lööve, artralgia, müalgia | Inimesed | Austraalia |
| Chikungunya viirus | Lööve, artriit | Primaadid, inimesed | Aafrika, India, Kagu-Aasia |
| Mayaro viirus | Lööve, artriit | Primaadid, inimesed | Lõuna-Ameerika |
| O'nyong'nyong'i viirus | Lööve, artriit | Primaadid, inimesed | Aafrika |
| Ross Riveri viirus | Lööve, artriit | Imetajad, inimesed | Austraalia, Okeaania |
| Semliki metsa viirus | Lööve, artriit | Linnud | Aafrika |
| Sindbisi viirus | Lööve, artriit | Linnud | Euroopa, Aafrika, Austraalia |
| Una viirus | Lööve, artriit | Primaadid, inimesed | Lõuna-Ameerika |
| Ida hobuste entsefaliidiviirus | Entsefaliit | Linnud | Ameerika |
| Tonate'i viirus | Entsefaliit | Inimesed | Lõuna-Ameerika |
| Venezuela hobuste entsefaliidiviirus | Entsefaliit | Närilised, hobused | Ameerika |
| Lääne hobuste entsefaliidiviirus | Entsefaliit | Linnud, imetajad | Põhja-Ameerika |
Alfaviirused on levinud üle kogu maailma ja paljud neist nakatavad ka inimest. Kõige tavalisemad sümptomid, mida nad põhjustavad, on artriit, entsefaliit, lööve ja palavik. Haigestumine võib lõppeda surmaga. Alfaviiruste peremeesteks olevad suuremad loomad, nagu inimesed ja hobused, on tavaliselt tupikperemehed ja ei mängi olulist rolli viiruse levimises. Ainult Venezuela hobuste entsefaliidiviiruse puhul on leitud, et hobused on viiruse võimendajateks. Teiste alfaviiruste looduslikud reservuaarid on peamiselt moskiitod, närilised ja linnud.
Alfaviirused võivad üle kanduda lülijalgsete, näiteks moskiitode vahendusel. Pistel tungib viirus vereringesse, põhjustades vireemiat. Alfaviirused võivad siseneda ka kesknärvisüsteemi, kus nad paljunevad neuronites. Näiteks Semliki metsa viiruse puhul põhjustab see entsefaliiti, mis lõpeb halvematel juhtudel letaalselt. Immuunsüsteemis kutsuvad alfaviirused esile interferoonide sünteesi. Lisaks sellele on immuunvastuses kaasatud antikehad ja T-rakud, mis mängivad olulist rolli viirusliku infektsiooni kõrvaldamises ja edasise arengu takistamises.
Diagnoosimine ja tõrje[muuda | muuda lähteteksti]
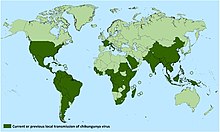
Diagnoosimine põhineb kliinilistel proovidel, kust on võimalik viirust isoleerida ja identifitseerida. Haigestunute suremus on märkimisväärne: 30–70% Chikungunya viiruse puhul ja umbes 70% ida hobuste entsefaliidiviiruse puhul. Infektsioon levib eelkõige laste ja vanade inimeste hulgas, kellel on nõrgem immuunsüsteem (eriti lastel). Alfaviirused põhjustavad pikaajaliste antikehade tootmist, mis kaitsevad organismi kogu elu.[4] Praegu puuduvad alfaviiruste vastu vaktsiinid, seetõttu on lahenduseks putukate peletamine tõrjevahendite abil, kaitserõivaste kandmine ja viiruse siirutajate (näiteks moskiitode) paljunemiskohtade hävitamine.
Teadustöö[muuda | muuda lähteteksti]
Alfaviirusi kasutatakse biomeditsiinilistes uuringutes. Näiteks Ross Riveri viirust, Sindbisi viirust, Semliki metsa viirust ja Venezuela hobuste entsefaliidiviirust kasutatakse viirusvektorite arendamises, mida on võimalik rakendada geeniteraapias, onkoteraapias ja huvipakkuvate valkude sünteesis.[10] Samuti pakkuvad huvi kimäärsed viirused, mille struktuuris on alfaviiruste ümbris ja retroviiruse nukleokapsiid – niinimetatud pseudotüüpi viirused. Sellised retroviiruste ja ka lentiviiruste pseudotüübid on võimelised sisestama oma geene peremeesrakku, mille tunnevad ära ja millesse aitavad siseneda alfaviiruse valgud E1 ja E2. Viiruse geenide stabiilset integreerumist peremehe genoomi vahendab retroviiruse nukleokapsiid. Alfaviiruste kasutust geeniteraapias piirab nende puudulik võime sihtmärkrakke eristada. Seda probleemi on lahendatud E2-valgu struktuuri muutlike antikehadomeenide sisestamisega, et viirus nakataks kindlat rakupopulatsiooni.
Teiseks takistuseks alfaviiruste kasutamisel on see, et mitmed alfaviiruste valgud põhjustavad apoptoosi. See ei puuduta aga retroviiruste ja lentiviiruste pseudotüüpe, millel on alfaviirustest pärit ümbrised. Sindbisi viiruse puhul on leitud, et ka selle ümbrisevalgud võivad apoptoosi põhjustada, mistõttu võivad ka Sindbisi viiruse ümbrist kasutavad pseudotüübid rakusurma põhjustada. Sindbisi viiruse ümbrise tsütotoksilisus võib olla põhjuseks, miks Sindbisi viiruse pseudotüüpe tootvatest rakukultuuridest saadakse väga madalaid viirustiitreid.
Alfaviirustel on suur potentsiaal ka vaktsiinide arendamises. Need on sobivad agendid replikonvektorite moodustamiseks, mille ülesandeks on humoraalse ja T-rakulise immuunvastuse indutseerimine. Neid võiks teoreetiliselt kasutada viiruslike, bakteriaalsete ja algloomade põhjustatud haiguste ning tuumorite antigeenide vastu vaktsineerimises.
Viited[muuda | muuda lähteteksti]
- ↑ 1,0 1,1 Wagner EK, Hewlett MJ (2004). Basic virology. Second edition. Blackwell Publishing
- ↑ Vénien-Bryan C, Fuller SD (February 1994). "The organization of the spike complex of Semliki Forest virus". J. Mol. Biol. 236 (2): 572–83.doi:10.1006/jmbi.1994.1166PMID 8107141
- ↑ Lescar J, Roussel A, Wien MW, Navaza J, Fuller SD, Wengler G, Wengler G, Rey FA (April 2001). "The Fusion glycoprotein shell of Semliki Forest virus: an icosahedral assembly primed for fusogenic activation at endosomal pH". Cell 105 (1): 137–48.doi:10.1016/S0092-8674(01)00303-8PMID 11301009
- ↑ 4,0 4,1 4,2 Mahy BWJ, van Regenmortel MHV (2008). Encyclopedia of virology. Thirf edition. Elsevier Inc. Academic Press.: Powers AM. Togaviruses:Alphaviruses
- ↑ Strauss JH, Strauss EG (1994). The Alphaviruses: Gene Expression, Replication and Evolution. Microbiological Reiviews. 58(3): 491–462
- ↑ Powers AM, Brault AC, Shirako Y, Strauss EG, Kang W, Strauss JH, Weaver SC (2001) Evolutionary relationships and systematics of the alphaviruses. J Virol 75(21):10118-10131
- ↑ Weaver SC, Hagenbaugh A, Bellew LA, Netesov SV, Volchkov VE, Chang GJ, Clarke DK, Gousset L, Scott TW, Trent DW, et al (1993) A comparison of the nucleotide sequences of eastern and western equine encephalomyelitis viruses with those of other alphaviruses and related RNA viruses. Virology 197(1):375–390
- ↑ Weaver SC, Rico-Hesse R, Scott TW (1992) Genetic diversity and slow rates of evolution in New World alphaviruses. Curr name Top Microbiol Immunol 176:99–117
- ↑ Lundström JO, Pfeffer M (2010) Phylogeographic structure and evolutionary history of Sindbis virus. Vector Borne Zoonotic Dis 10(9):889–907
- ↑ Atkins GJ, Fleeton MN, Sheahan BJ (2008) Therapeutic and prophylactic applications of alphavirus vectors. Expert reviews in molecular medicine, Vol.10, e33
Välislingid[muuda | muuda lähteteksti]
- Viralzone: Alphavirus
- Virus Pathogen Database and Analysis Resource (ViPR): Togaviridae
- Togaviridae of Arthropod-Borne Viruses Infection
- Alphavirus vectors: from protein production to gene therapy
- Alphavirus vectors and vaccination
- Alphaviral cytotoxicity and its implication in vector development
- Chapter 54 – Alphaviruses (Togaviridae) and Flaviviruses (Flaviviridae)

