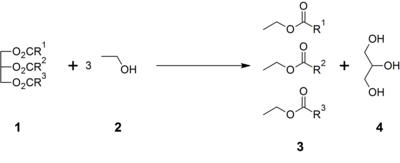Glütserool
See artikkel ootab keeletoimetamist. |
See artikkel vajab toimetamist. |
| Glütserool | |
|---|---|
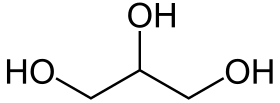 Glütserooli struktuurivalem | |
| Üldised omadused | |
| Keemiline valem | C3H8O3 |
| Välimus | läbipaistev vedelik, hügroskoopne |
| Füüsikalised omadused | |
| Molekuli mass | 92,09 amü |
| Sulamistemperatuur | 290,95 K (17,8 °C) |
| Keemistemperatuur | 563,15 K (290 °C) |
| Tihedus | 1,261 kg/m³ |
| Kasutatakse SI-süsteemi ühikuid. Kui pole teisiti öeldud, eeldatakse normaaltingimusi. | |
Glütserool (ehk glütseriin) on lihtne värvitu, lõhnatu ja viskoosne polüoolne ühend, mida kasutatakse laialdaselt farmaatsiatööstuses.
Glütserooli kolm hüdroksüülrühma tingivad tema lahustuvuse vees ja hügroskoopsed omadused. Glütseroolne tsenter on ühtede oluliste lipiidide, triglütseroolide, selgrooks. Vaba glütserool on magus ja vähe toksiline.
Tootmine[muuda | muuda lähteteksti]
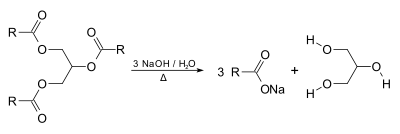
Glütserool on seebitootmise kõrvalsaadus, mis tekib rasvade seebistamisel.
Seda tekib ka kõrvalsaadusena biodiislikütuse tootmisel. Sel meetodil saadud glütserool on tihti välimuselt tume ning paksu, siirupitaolise kontsistentsiga. Triglütseriidid reageeritakse alkoholiga (nt etanool) aluselise katalüsaatori juuresolekul. Saaduseks on rasvhapete etüülestrid ja glütserool.
Glütserooli toodetakse ka eri meetodeid kasutades propüleenist. Kõige tähtsamaks neist on epiklorohüdriini protsess. Selle käigus klooritakse propüleen, mille tulemusel tekib allüülkloriid, mis oksüdeeritakse hüpokloritiga diklorohüdriiniks. Saadus reageeritakse omakorda tugeva alusega ja saadakse epiklorohüdriin, mille hüdrolüüsi saaduseks on glütserool.
Kuna tänapäeva ravimi- ja hügieenitööstuses on nõudlus vaid puhta glütserooli järele, kasutatakse mainitud sünteetilist tootmisviisi suhteliselt vähe. Valdav osa toorainest on orgaanilise päritoluga – loomsed rasvad (nt veiserasv) ja taimeõlid (nt kookose- ja sojaõli).[1] Aastas toodetakse USAs ja Euroopas umbes 950 000 tonni glütseroooli.[2] Tootmine suureneb vastavalt EU direktiivile 2003/30/EC, mis sätestab, et 5,75% naftasaadustest toodetud kütustest asendadaks biokütusega. On kavandatud, et 2020. aastaks ületab tootmine nõudluse kuuekordselt.
Kasutusvaldkonnad[muuda | muuda lähteteksti]
Toidutööstus[muuda | muuda lähteteksti]
Toitudes ja jookides kasutatakse glütserooli niisuti, lahusti ja magusainena ning see võib olla abiks toitude säilitamisel. Seda kasutatakse ka täiteainena toitudes, mis valmivad masstoodanguna (nt küpsistes) ja paksendajana liköörides. Glütserooli ja vett kasutatakse teatud tüüpi lehtede säilitamisel.[3] Suhkruasendajana sisaldab see ligikaudu 27 kilokalorit teelusika kohta (suhkur sisaldab 20) ja on 60% ulatuses sama magus kui sahharoos. See ei toida bakterit, mis tekitab hambakattu ja põhjustab hambaauke. Toidulisandina on glütserooli tähis E422.
Glütserooli kasutatakse nii mono- ja diglütseroolide tootmisel, mida kasutatakse emulgaatoritena, kui ka polüglütserooli estrites, mida kasutatakse margariini tootmisel.
Seda kasutatakse ka niisutina (koos propüleenglütserooliga E1520 ja/või E422) mokatubakas.
Ravimi- ja hügieenitööstus[muuda | muuda lähteteksti]
Glütserooli kasutusalad ravimi- ja hügieenitööstuses on valdavalt toodete pehmuse ja määrdevõime parandamine ning niisutamine. Seda võib leida allergiaravimites, köhasiirupites, eliksiirides ja rögaeritust soodustatavates ravimites, hambapastas, suuvees, nahahooldustoodetes, raseerimisvahus, juuksetoodetes, seepides ja veepõhistes libestites. Glütserooli kasutatakse tahkena ka ravimitableti kattena.
Glütserool on glütseroolseepide üks koostisosa. Eeterlikke õlisid lisatakse aroomiainetena. Glütseroolseepe kasutavad inimesed, kellel on tundlik ja kergesti ärritatav nahk, kuna see aitab vältida naha kuivust oma niisutavate omadustega.
Glütserooli saab kasutada nii kõhulahtistina kui ka annustada pärasoolde väikestes (2–10 ml) kogustes klistiiriga; see ärritab päraku limaskesta ja tekitab hüperosmootilise efekti.
Puhas või peaaegu puhas glütserool on tõhus ravim kergemate põletuste, putukahammustuste, löövete, lamatiste ja konnasilmade vastu. Seespidisel manustamisel aitab glütserool halva hingeõhu vastu, kuna toimib bakteritega kokkupuutel niiskust imava ainena.[4]
Juurviljaglütserooli kasutatakse elektroonilistes sigarettides nikotiini ja maitsemolekulide suspensioonina.
Pinnateadus[muuda | muuda lähteteksti]
Glütserool vähendab hõõrdumiskoefitsienti polümeerkaetud pindade puhul mitme suurusjärgu võrra. Seda põhjustab glütserooli-vee suurendatud viskoossus võrreldes puhta veega.[5]
Taimsed ekstraktid[muuda | muuda lähteteksti]
Glütserool takistab tanniinidel sadestumast taimede etanooliekstraktides (tinktuurides), kui seda kasutatakse tinktuuri meetodil ekstraheerimisel, eriti 10% lahusena. Seda kasutatakse ka alternatiivina lahustina kasutatavale etanoolile taimsete ekstraktide valmistamisel. Selle ekstraheerivad omadused on halvemad, kui seda kasutatakse tavalisel tinktuuri metoodikal. Glütserool imendub kehas ligikaudu 30% aeglasemalt, põhjustades väiksema vere glükoosisisalduse. Alkoholil põhinevatest tinktuuridest võib ka alkoholi eemaldada ja asendada glütserooliga selle säilitavate omaduste tõttu. Vedelate ekstraktide tootjad ekstraheerivad taimi kuumas vees, enne kui lisavad glütseriini, et teha glütseriite.[6][7]
Glütserooli kasutatakse ka innovaatilistes alkoholivabades "dünaamilistes" ekstraheerimismetoodikates, kus glütserool on näidanud väga head botaanilist mitmekülgsust mitmete koostisosade ja keeruliste molekulide eraldamise näol. Puhas glütserool on pea sama heade ekstraheerivate omadustega kui alkohol või alkoholi-vee segud. Glütserooli ekstraheerivate omaduste põhjuseks on tema kolmeaatomiline struktuur, mida kasutatakse dünaamiliste meetoditega, vastupidi passiivsetele tinktuurimetodoloogiatele, mis sobivad paremini alkoholi diatomaarsele struktuurile. Vastupidi alkoholidele ei denatureeri või muuda glütserool taimseid koostisosi inertseteks. Samuti on ta stabiilne maatriks ekstraheerimissaaduste säilitamiseks, kuna glütserool ei lase osküdatsiooni ega reduktsioonireaktsioonidel toimida. Glütserool on lisaks ka bakteriostaatiline, st ei lase bakteritel kasvada.[8][9][10]
Antifriis[muuda | muuda lähteteksti]
 Pikemalt artiklis antifriis
Pikemalt artiklis antifriis
Nagu etüleenglükool ja propüleenglükool, on glütserool mitteiooniline kosmotroop, mis moodustab veemolekulidega tugevaid vesiniksidemeid, mis võistlevad vesi-vesi vesiniksidemetega. See segab veekristallide moodustamist, kui temperatuuri oluliselt ei alandata. Madalaim saavutatav külmumistemperatuur on −37,8 °C, mis vastab 60–70% glütseroolilahusele vees.
Ajalooliselt kasutati glütserooli autodes, kuni see asendati etüleenglükooliga, mille külmumistemperatuur on madalam. Kuigi glütserooli vesilahuse külmumistemperatuur on kõrgem kui etüleenglükooli vesilahusel, ei ole glütserool toksiline ning selle kasutuselevõttu kaalutakse taas.[11][12]
Laboris kasutatakse seda ensüümisolventides, mida ladustatakse alla 0 °C, kuna glütserool madaldab vastavate lahuste külmumistemperatuuri. Glütserooli kasutatakse ka bakterite, embrüote, ümarusside ja muude organismide kaitseks, mida hoitakse külmutatud lahustes, kuna glütserool vähendab jääkristallide kahjustavat toimet säilitatavatele organismidele.
Keemiline vaheühend[muuda | muuda lähteteksti]
Glütserooli kasutatakse nitroglütseriini tootmisel, mis on suitsuvaba püssirohu, erinevate lõhkeainete (nt dünamiidi) ja propellantide (nt kordiidi) põhiline koostisosa. Teise maailmasõja ajal oli raske suurendada glütseriini tootmist nii, et see vastaks sõjaaegsele nõudlusele, kuna seda saadi vaid seebi tootmisel kõrvalsaadusena. Siiski olid sünteetilise glütseriini protsessid juba enne Teist maailmasõda riikliku kaitse prioriteediks. Nitroglütseriini kasutatakse angiini ravimiseks, annustades keelealuste tablettide või aerosoolse pihusena.
Palju tehakse teadustööd selle nimel, et üritada toota väärtuslikke saadusi toorglütseroolist (tavaliselt sisaldab 20% vett ja esterfikatsiooni katalüsaatori jäänukeid), mis on tekkinud kõrvalsaadusena biodiislikütuse tootmisel. Uuritakse ka toorglütserooli kui biomassi lisandi kasutamist uue taastuvenergia allikana.
- vesiniku tootmise üksus[13]
- glütseriinatsetaat (potentsiaalne kütuselisand)[14]
- muutmine propüleenglükooliks[15]
- muutmine akroleiiniks[16][17]
- muutmine etanooliks[18]
- muutmine epiklorohüdriiniks,[19] epoksüvaikude toormaterjal
Kütus[muuda | muuda lähteteksti]
Üks Briti ettevõte on väitnud, et glütserooli võib kasutada diislikütuse alternatiivina.[20]
Teater[muuda | muuda lähteteksti]
Mõned teatritrupid kasutavad glütserooli näitleja näol pisarate illusiooni tekitamiseks. Glütserooli kasutatakse ka mõnes teatraalses udus.[21]
Metabolism[muuda | muuda lähteteksti]
Glütserool on triatsüülglütseroolide ja fosfolipiidide sünteesi prekursor maksas. Kui keha kasutab rasvu energiakandjana, lastakse glütserool ja rasvhapped vereringesse. Mõnes organismis muudetakse glütserool maksas glükoosiks, mis varustab rakke energiaga.
Enne kui glütserool saab glükolüüsi või glükogenaasi metabolismiradadele siseneda, peab selle muutma glütseeraldehüüd-3-fosfaadiks järgmiste etappidega:
| Glütserool | Glütserool kinaas | Glütserool-3-fosfaat | Glütserool-3-fosfaat dehüdrogenaas | Dihüdroksüatsetoon fosfaat | Triosefosfaat isomeraas | Glütseeraldehüüd-3-fosfaat | |||
| ATP | ADP | FAD | FADH2 | 
|

| ||||
|

|

| |||||||
| NAD+ | NADH |
||||||||
Ensüümi glütserool kinaas leidub vaid maksas. Rasvkoes sünteesitakse glütserool-3-fosfaati dihüdroksüatsetoon fosfaadist ensüümi glütserool-3-fosfaat dehüdrogenaas abil.
Suu kaudu manustamisel on glütserooli toksilisus väga väike; oraalne LD50 doos on rottidel 12 600 mg/kg, hiirtel 8700 mg/kg.[22]
Viited[muuda | muuda lähteteksti]
- ↑ The OPTIM™ Advantage. the DOW Chemical Company.
- ↑ Nilles, Dave (2005). "A Glycerin Factor". Biodiesel Magazine. Originaali arhiivikoopia seisuga 8. november 2007. Vaadatud 15. detsembril 2012.
- ↑ Stevens, Alan. "Preserving flowers and decorative foliages with glycerin and dye" (PDF). Originaali (PDF) arhiivikoopia seisuga 24. märts 2020. Vaadatud 15. detsembril 2012.
- ↑ "In-vitro growth inhibition of periodontitis-associated species by Lactobacillus reuteri".
- ↑ Nalam, Prathima C.; Clasohm, Jarred N.; Mashaghi, Alireza; Spencer, Nicholas D. (2009). "Macrotribological Studies of Poly(L-lysine)-graft-Poly(ethylene glycol) in Aqueous Glycerol Mixtures". Tribology Letters. 37 (3): 541. DOI:10.1007/s11249-009-9549-9.
- ↑ Long, Walter S. (1917). "The Composition of Commercial Fruit Extracts". Transactions of the Kansas Academy of Science. 28: 157–161. DOI:10.2307/3624347. JSTOR 3624347.
- ↑ "Does Alcohol Belong In Herbal Tinctures?". Originaali arhiivikoopia seisuga 12. oktoober 2007. Vaadatud 15. detsembril 2012.
- ↑ GLYCEROL AND THE GLYCOLS – Production, Properties and Analysis by, James W. Lawrie, Ph.D. (1928 The Chemical Catalog Company, Inc., New York, NY)
- ↑ GLYCERIN – Its Industrial and Commercial Applications, by Georgia Leffingwell, Ph.D. and Miton Lesser, B.S. (1945 Chemical Publishing Co., Inc., Brooklyn, NY)
- ↑ The Manufacture of GLYCEROL – Vol. III (1956 The Technical Press, LTD., London, UK)
- ↑ Hudgens, R. Douglas; Hercamp, Richard D.; Francis, Jaime; Nyman, Dan A.; Bartoli, Yolanda (2007). "An Evaluation of Glycerin (Glycerol) as a Heavy Duty Engine Antifreeze/Coolant Base". DOI:10.4271/2007-01-4000.
{{cite journal}}: viitemall journal nõuab parameetrit|journal=(juhend) - ↑ Proposed ASTM Engine Coolant Standards Focus on Glycerin. Astmnewsroom.org. Vaadatud 15.08.2012.
- ↑ Marshall, A. T. and Haverkamp, R. G. (2008). "Production of hydrogen by the electrochemical reforming of glycerol-water solutions in a PEM electrolysis cell". International Journal of Hydrogen Energy. 33 (17): 4649–4654. DOI:10.1016/j.ijhydene.2008.05.029.
{{cite journal}}: CS1 hooldus: mitu nime: autorite loend (link) - ↑ Melero, Juan A.; Van Grieken, Rafael; Morales, Gabriel; Paniagua, Marta (2007). "Acidic mesoporous silica for the acetylation of glycerol: Synthesis of bioadditives to petrol fuel". Energy Fuels. 21 (3): 1782–1791. DOI:10.1021/ef060647q.
- ↑ "Dow achieves another major milestone in its quest for sustainable chemistries". Dow Chemical Company. 15.03.2007.
- ↑ Ott, L.; Bicker, M.; Vogel, H. (2006). "The catalytic dehydration of glycerol in sub- and supercritical water: a new chemical process for acrolein production". Green Chemistry. 8 (2): 214–220. DOI:10.1039/b506285c.
- ↑ Watanabe, Masaru; Iida, Toru; Aizawa, Yuichi; Aida, Taku M.; Inomata, Hiroshi (2007). "Acrolein synthesis from glycerol in hot-compressed water". Bioresource Technology. 98 (6): 1285–1290. DOI:10.1016/j.biortech.2006.05.007. PMID 16797980.
- ↑ Yazdani, S. S. and Gonzalez, R. (2007). "Anaerobic fermentation of glycerol: a path to economic viability for the biofuels industry". Current Opinion in Biotechnology. 18 (3): 213–219. DOI:10.1016/j.copbio.2007.05.002. PMID 17532205.
{{cite journal}}: eiran tundmatut parameetrit|laydate=, kasuta parameetrit (|lay-date=) (juhend); eiran tundmatut parameetrit|laysource=, kasuta parameetrit (|lay-source=) (juhend); eiran tundmatut parameetrit|laysummary=, kasuta parameetrit (|lay-url=) (juhend); viite koodis on kasutusel iganenud parameeter|lay-source=(juhend); välislink kohas|laysummary= - ↑ "Dow Epoxy advances glycerine-to-epichlorohydrin and liquid epoxy resins projects by choosing Shanghai site". Dow Chemical Company. 26. märts 2007. Originaali arhiivikoopia seisuga 9. mai 2008.
- ↑ Is glycerine primed to end fossil fuel domination? on Environmental Expert. Environmental-expert.com (03.08.2011). Retrieved on 15.08.2012.
- ↑ "Material Safety Data Sheet" (PDF). La Maitre Special Effects Inc. Originaali (PDF) arhiivikoopia seisuga 12. juuli 2012. Vaadatud 15. detsembril 2012.
- ↑ Safety data for glycerol https://web.archive.org/web/20111130084558/http://msds.chem.ox.ac.uk/GL/glycerol.html