Areenid
| See artikkel räägib orgaaniliste ühendite klassist; sõna teiste tähenduste kohta vaata artiklit Areen. |
See artikkel vajab toimetamist. (August 2014) |
See artikkel vajab ajakohastamist. |
Areenid ehk aromaatsed süsivesinikud on süsivesinikud, mis sisaldavad üht või mitut benseenituuma. Benseenituumas moodustavad 6 süsiniku aatomit rõnga ja neid ühendavad omavahel vaheldumisi üksik- ja kaksiksidemed.
Termin "aromaatsed süsivesinikud" tekkis enne aromaatsuse mehhanismi avastamist. Niisugune termin mõeldi välja sellepärast, et paljudel sellesse ainerühma kuuluvatel ühenditel on magus või meeldiv lõhn.
Termin "benseenituum" on nimetatud kõige lihtsama aromaatse süsivesiniku, kõigest 6 süsiniku aatomist koosneva aine benseeni järgi.
Aromaatsed süsivesinikud võivad olla nii monotsüklilised (ehk sisaldavad üht benseenituuma) kui polütsüklilised (ehk sisaldavad mitut benseenituuma).
Aromaatseteks ühenditeks nimetatakse ka mõningaid benseenil mittepõhinevaid aineid, kui nad järgivad Hückeli reeglit. Monotsükliliste ainete korral peab nende π-elektronide arv olema 4π+2, kus π on naturaalarv. Niisugusi aineid nimetatakse heteroareenideks. Nendes on vähemalt üks süsiniku aatom asendunud võõraatomi, näiteks hapniku, lämmastiku või väävli aatomiga. Heteroareenide hulka kuuluvad näiteks furaan, kus on 5 aatomist koosnev rõngas, mis koosneb 4 süsiniku ja 1 hapniku aatomist, ning püridiin, mille 6 aatomist koosnevas rõngas on üks lämmastiku aatom.
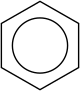
Kõige lihtsam aromaatne süsivesinik on benseen ja see ka avastati neist esimesena. Selle eraldas ja tuvastas eraldi ainena 1825 Michael Faraday. 1865 avaldas Friedrich August Kekulé artikli, milles oletas, et benseeni struktuur on niisugune, nagu seda tänapäeval tuntakse. Igal süsiniku aatomil on neli sidet, millest üks läheb vesiniku aatomisse ja ülejäänud kolm lähimatesse süsiniku aatomitesse. Ühe naabriga ühendab teda üksikside ja teisega kaksikside. Üksik- ja kaksikside vahetavad oma asukohti nii kiiresti, et konkreetsel hetkel ei saagi nende asukohti õigupoolest kindlaks teha ja seda väljendatakse ringiga süsinikurõnga sees. Esimesena pakkus selle võimaluse välja Johannes Thiele 1899.
π-elektronide delokalisatsiooni benseeni molekulis kujutavad kolm alternatiivset struktuurivalemit:

|

|
|
Areene ühendavad järgmised omadused:
- Neil ilmneb aromaatsus.
- Vesinike aatomeid on võrreldes süsinike aatomitega suhteliselt vähe. Pole haruldane, et vesinike aatomeid on vähemgi kui süsinike aatomeid.
- Suure süsinikusisalduse tõttu põlevad nad kollaka tahmase leegiga.
- Neile on iseloomulikud elektrofiilne ja nukleofiilne aromaatne asendusreaktsioon.
Areenide sünteesimine[muuda | muuda lähteteksti]
Areenide sünteesimist mitteareenidest nimetatakse aromatiseerimiseks. Selleks on palju laboratoorseid meetodeid. Paljud neist põhinevad tsükli tekitamise reaktsioonidel. Alküünide trimeriseerimine põhineb kolme alküüni molekuli (harilikult sama aine molekuli) omavahelisel reageerimisel. Dötzi reaktsiooni korral on lähteained alküün, süsinikmonooksiid ja kroomi karbeenkompleks. Dielsi-Alderi reaktsiooni korral reageerib alküün pürooni või tsükloheksaaniga, kusjuures eraldub süsinikmonooksiid või süsinikdioksiid. Bergmani tsükliseerimine lähtub enediüünist ja vajab vesinikudoonorit.
Areenide sünteesi meetodite teine rühm lähtub tsükloheksaanist või mõnest muust alifaatsest tsüklist. Veel läheb vaja hüdrogeenimise juures kasutatavaid katalüsaatoreid, näiteks plaatina, pallaadiumi ja niklit, samuti kinoone, väävlit ja seleeni.
Areenide keemilised omadused[muuda | muuda lähteteksti]
Areenidele on tüüpilised asendusreaktsioonid, milles üks asendusrühm, tavaliselt vesinik, asendub teise asendusrühmaga. Selliste reaktsioonide kaks tüüpi on elektrofiilne ja nukleofiilne asendusreaktsioon vastavalt sellele, kas aktiivne reagent on elektrofiil või nukleofiil. Radikaal-nukleofiilse asendusreaktsiooni üks reagentidest on vaba radikaal.
Sidestusreaktsioon toimub metallkatalüsaatori juuresolekul. Selle käigus tekib tavaliselt uus süsinik-süsinik-side, haruldasemad on süsinik-lämmastik-side (aniliinidel) või süsinik-hapnik-side.
Areenide hüdrogeenimine tekitab küllastunud tsüklitega aineid.
Tsüklite lisandumise reaktsioonid, näiteks Diels-Alderi reaktsioon, ei ole nii tavalised.
Benseenituum mõjub laengutele stabiliseerivalt. Seda on näha näiteks fenooli juures, mille hüdroksüülrühm -OH on happeliste omadustega, sest benseenituum osalt stabiliseerib hapniku aatomi negatiivse laengu.
Valik areene[muuda | muuda lähteteksti]
- Areenide esindajaid
-
p-ksüleen
-
m-ksüleen
-
Bifenüül ehk difenüül ehk fenüülbenseen
-
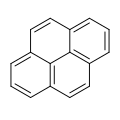
Benso[a]püreen
-
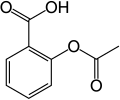
Aspiriin ehk atsetüülsalitsüülhape
-
Paratsetamool ehk atsetaminofeen
Polütsüklilised areenid[muuda | muuda lähteteksti]
Kõige lihtsam polütsükliline areen on naftaleen, mis koosneb kahest benseenituumast. Seevastu grafeenis võivad benseenituumad katta suuri kahemõõtmelisi lehti.
Polütsüklilised areenid esinevad naftas, kivisöes ja tõrvas. Nad tekivad kõrvalsaadustena kütuse põlemisel, niihästi fossiilkütuse kui ka biomassi põlemisel. Saasteainetena tuleb neile tähelepanu pöörata, sest mõned neist on leitud olevat kantserogeensed ehk vähki tekitavad, mutageensed ehk mutatsioone tekitavad või teratogeensed ehk väärarenguid tekitavad. Polütsüklilisi areene leidub küpsetatud toidus, eriti kõrgel temperatuuril küpsetatud, näiteks grillitud või röstitud lihas, samuti suitsutatud kalas. Kuid polütsüklilisi areene on avastatud ka avakosmosest, komeetidest ja meteoriitidest.
Polütsükliliste areenide maailma hüpoteesi järgi tekkis elu polütsüklilistest areenidest. Katsed on näidanud, et sellistes tingimustes, mis valitsesid Maal miljardite aastate eest, võivad suhteliselt kiiresti iseeneslikult tekkida keerukad süsinikuühendid, mis mõneti meenutavad RNA molekule.
Areenide nimetused[muuda | muuda lähteteksti]

Kuna areenide keemia arenes oluliselt varem kui orgaanilise keemia nomenklatuur, siis kasutatakse areenide nimetamisel väga palju mittesüstemaatilisi ehk triviaalnimetusi, mille näiteid on ülaltoodud galeriis.
Monoasendatud benseeni derivaatide nimetamisel kasutatakse lõppliidet -benseen (nt klorobenseen, nitrobenseen). Alküülasendatud benseeni derivaatide nimetamisel lähtutakse alküülahela pikkusest: kui ahelas on rohkem kui 6 süsinikuaatomit, siis valitakse tüviühendiks alküülahel (nt fenüülheptaan).
Diasendatud benseeni nimetamisel kasutatakse eesliiteid orto- (o-), meta- (m-) ja para- (p-), vastavalt 1,2-, 1,3- ja 1,4-diasenduse kirjeldamiseks. Tri- ja enamasendatud benseeni korral nummerdatakse tsükkel, andes asendajatele väikseimad võimalikud kohanumbrid.
Vaata ka[muuda | muuda lähteteksti]
| Pildid, videod ja helifailid Commonsis: Aromaatsed süsivesinikud |












![Benso[a]püreen](http://upload.wikimedia.org/wikipedia/commons/thumb/f/fa/Benzo-a-pyrene.svg/120px-Benzo-a-pyrene.svg.png)